Аминокислотно-заместительная терапия. Кому. Когда. Зачем.
Что такое коллаген
Кожа, как известно, состоит из нескольких слоев: эпидермиса, дермы и подкожно-жировой клетчатки.
АЗТ- и PRP-терапия направлены главным образом на дерму, которая отвечает за толщину и эластичность кожи, в дерме происходит огромное количество параллельных процессов синтеза и распада. Лучше пытаться влиять на эту деятельность , хорошо представляя себе патогенетические механизмы, протекающие в коже.
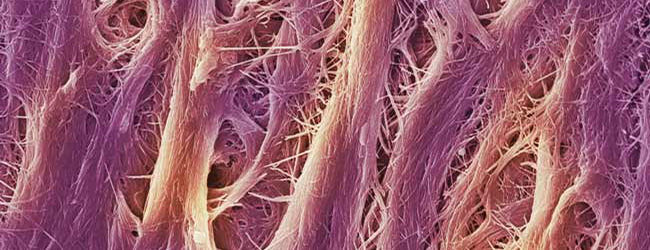
Основной компонент дермы – это коллаген, органическое соединение из группы фибриллярных белков. Сосочковый слой дермы образован более мелкими пучками волокон коллагена, в нем преобладает большое количество клеток (фибробласты, фиброциты, тучные клетки, Т-лимфоциты), в то время как сетчатый слой характеризуется более крупными пучками, формирующими характерную сеть, обеспечивающую прочность кожи, отсюда и название слоя – сетчатый.
Коллаген:
- Основной белок дермы
- Волокна переплетены в правозакрученную спираль, состоящую из трех полипептидных цепей
- Производится фибробластами и расщепляется коллагеназой
- Обеспечивает упругость и эластичность кожи
Синтез коллагена
Фибробласты – основные клетки дермы, которые производят как коллаген, так и другие белки и некоторые энзимы. В разные периоды жизни человека дерма претерпевает изменения. Так, в юном возрасте она характеризуется высокой активностью фибробластов и состоит из небольших ярко-красных пучков коллагеновых волокон. С возрастом активность фибробластов снижается, уменьшается их количество, пучки коллагеновых волокон утолщаются и приобретают бледно-розовую окраску.
Молекула коллагена состоит из трех полипептидных цепей, скрученных в виде правой тройной спирали и состоящих из аминокислотных остатков (как правило, это остатки глицина, пролина и лизина). Трёхспиральная структура коллагена придает молекуле прочность.
На одном из концов молекула «сшита» поперечными связями из остатков лизина, что придает волокнам высокую степень упругости.
Особую роль в регуляции синтеза коллагена играют гормоны. Глюкокортикоиды тормозят синтез коллагена, что проявляется уменьшением толщины дермы, а также атрофией кожи в местах продолжительного введения этих гормонов (Zöller et al.).
На синтез коллагена влияют также половые гормоны, рецепторы к которым обнаружены в фибробластах. Синтез коллагена зависит от содержания эстрогенов, что подтверждает тот факт, что у женщин в менопаузе снижается содержание коллагена в дерме (Calleja-Agius et al.).
Основные типы коллагена в дерме
Существует 19 типов коллагена, в разных тканях преобладают разные его типы, что в свою очередь определяется той ролью, которую коллаген играет в конкретном органе или ткани.
В дерме, в основном, содержится коллаген I (сетчатый слой) и III (сосочковый слой) типов. Тип I составляет от 80 до 85 % матрикса дермы и отвечает за эластичность. Коллаген типа I является главным «союзником» старения. Как было установлено Nelson et al., в результате фотостарения содержание коллагена в коже снижается. Тип III второй по важности, составляет от 10 до 15 % матрикса. Волокна отличаются меньшим диаметром в сравнении с волокнами коллагена типа I и формируют более мелкие пучки, обеспечивая коже гибкость.
Тип IV является структурной составляющей базальной мембраны.
Тип V диффузно распространен в дерме и составляет от 4 до 5 % матрикса.
Тип VII участвует в образовании заякоренных фибриллов.
Тип XVII локализуется в гемидесмосомах, которые связывают клетки эпителия с лежащей под ними базальной мембраной.
В молодой коже преобладают волокна коллагена типов I (80 %) и III (15 %), что составляет 6:1. С возрастом происходит уменьшение содержания коллагена типа I, что ведет к утолщению и нарушению связей между волокнами.
Коллаген и старение
Старение характеризуется такими изменениями кожи, как появление морщин и потеря упругости. Это связано с уменьшением количества волокон коллагена в дерме. Поскольку коллаген является важнейшей «опорой» кожи, неудивительно, что если уровень его снижается, то кожа начинает «проседать», терять эластичность, а взамен приобретать морщины. Установлено, что каждый год происходит снижение уровня коллагена в тканях на 2 % (Fenske et al.).
Важную роль играет и гликация, процесс, в ходе которого лишняя молекула сахара (глюкоза) присоединяется к белковой молекуле (в частности, к молекуле коллагена), как бы склеивая ее. «Склеенные» волокна коллагена теряют способность к сокращению, что затрудняет их способность к регенерации и снижает упругость.
Как мы можем контролировать процессы синтеза и распада коллагена?
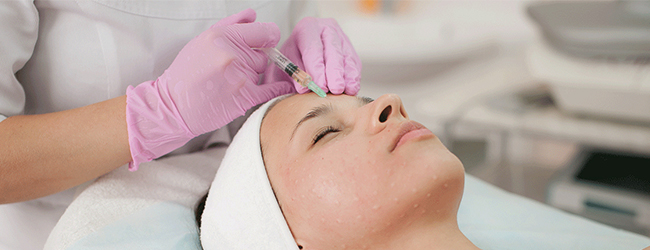
В настоящее время эстетическая медицина может предложить современные и эффективные методики созданию пула веществ для наиболее эффективного и контролируемого синтеза коллагена. В первую очередь это аминокислотно-заместительная терапия (АЗТ) и PRP-терапия (плазмотерапия).
АЗТ представляет собой инъекционное введение аминокислот (глицин, L-пролин, L-лизин моногидрохлорид, L-лейцин), которые ответственны за выработку коллагена.
Недавнее исследование Avantaggiato et al. показало, что совместное инъекционное введение ацетилцистеина и аминокислот привело к улучшению внешнего вида кожи, замедлило ее старение и обезвоживание.
На российском рынке хорошо зарекомендовал себя препарат JALUPRO® (Италия).
Практические аспекты использования AЗТ мы выяснили у Дианы Юдиной, доктора-косметолога, которая давно и очень успешно использует аминокислотно-заместительную терапию в своих комплексных программах.
Каким пациентам Вы назначаете АЗТ? Почему?
В первую очередь применение АЗТ показано при:
- хроностарении кожи лица средней и сильной степени выраженности, возраст 35+;
- дегидратированной коже, рубцах постакне, стриях;
- подготовке и реабилитации после эстетических процедур (пластическая операция, фракционный фототермолиз, радиоволновой или ультразвуковой лифтинг, электропорация, мезотерапия, IPL)
На сегодняшний день известно о множестве механизмов старения кожного покрова. Большинство из них связаны со снижением функциональной активности фибробластов: с возрастом замедляется продукция и обновление компонентов межклеточного матрикса (коллагена, эластина, фибронектина, гликозамингликанов, протеогликанов), ухудшается его организация и заживление ран.
По данным последних исследований, особенность первичной структуры α-цепей коллагена заключается в том, что 33,7 % всех аминокислотных остатков в молекуле коллагена приходится на глицин, 13,3 % – на пролин, 9,7 % – на гидроксипролин, 11,6 % – на аланин. В полипептидной цепи коллагена доминируют характерные триплеты гли-X-Y, где в положении «X» и «Y» могут быть любые аминокислоты, но чаще в положении «X» находится пролин, а в положении «Y» – гидроксипролин или гидроксилизин.
Клинически доказано, что АЗТ обеспечивает хемотаксис и деление фибробластов, имеет синергический эффект, усиливая функциональную активность кератиноцитов и фибробластов, оптимизирует процессы рубцевания, сокращает реабилитационный период (до 40 %) после эстетических процедур, увеличивает толщину и эластичность, снижает рельефность кожи.
Может ли АЗТ стать заменой классической биоревитализации?
С моей точки зрения, эти две процедуры дополняют друг друга, классическая ревитализация обеспечивает максимальную среду для функциональной активности фибробластов, для их синтеза, хемотаксиса, миграции и пролиферации.
АЗТ стимулирует неоколлагенез, усиливает активность кератиноцитов, процессы метаболизма, восстанавливает структуру коллагена.
Плазмолифтинг™ – методика, которую разработали отечественные ученые Ренат Ахмеров и Роман Зарудий. Во всем мире метод известен, как PRP-терапия (platelet rich plasma) или плазмотерапия, и основан он на использовании плазмы крови пациента.
Богатая тромбоцитами плазма вводится в проблемные зоны и активизирует механизм обновления клеток.
После введения плазмы фибробласты начинают синтезировать коллаген, эластин и гиалуроновую кислоту, за счет чего улучшается состояние и внешний вид кожи. Для получения плазмы осуществляется забор крови у пациента в специальную пробирку. Затем кровь очищается и помещается в центрифугу, где разделяется на три фракции, из которых выбирается наиболее обогащенная активированными тромбоцитами плазма. Вся процедура занимает около часа и требует лишь местного обезболивания (при необходимости).
Основным преимуществом плазмотерапии является безопасность и патогенетическая обоснованность метода.
Показания к терапии:
- Возрастные изменения кожи (морщины, птоз);
- Пониженный тургор;
- Сухость и шелушение;
- Растяжки;
- Фотостарение;
- Увеличение эффекта от других терапевтических процедур;
- Подготовка кожи к хирургическому вмешательству;
- Акне;
- Выпадение волос.
Мы задали несколько вопросов ведущему специалисту по аутологичной плазме Олесе Алексеевне Чирковой.
Чиркова Олеся Алексеевна
Хирург-косметолог, Главный специалист компании «Плазмолифтинг» по направлению эстетическая медицина в России, Европе,странах Балтии и СНГ. Ассистент кафедры косметологии Института ДПО ИПХиФК
Может ли PRP-терапия считаться аминокислотно-заместительной в полной мере?
Вопрос невероятно сложный, потому как имеет не один ракурс рассмотрения. Если диагноз АК-недостаточности установлен, определены кислоты в дефиците, процент их дефицита и форма, то в данном случае мы можем предположить, что введение плазмы не будет являться вариантом первого выбора, а станет лишь сопутствующей терапией при введении АК в составе мезо- или фармпрепарата, так как является источником транспортных белков. Это обеспечит более рациональный подход, так как эффективность при местном введении плазмы и прочих веществ повышает их биодоступность.
Однако если мы возьмем в качестве примера обратившегося к врачу эстетической медицины среднестатистического пациента с признаками старения, но без четкого диагноза и цифр по аминокислотам, то в данном случае PRP-терапия будет самым быстрым, простым и беспроигрышным вариантом по компенсации витальных потребностей.
Какой группе пациентов однозначно нужна аминокислотно-заместительная терапия?
Учитывая данные диетологов о том, что на планете проживает до 80 % белково-дефицитных людей, то – всем. Совершенно серьезно стоит подойти к аминокислотной коррекции большинству пациентов, так как это обеспечит фундамент для последующих процедур, эффективность которых возрастет на фоне предварительной коррекции.
Источник
Краткий обзор некоторых кофакторов, участвующих в синтезе коллагена
Качественные коллагеновые волокна — одна из основных составляющих здоровой кожи. Поэтому большое количество косметологических методов направлено на восстановление ее коллагенового каркаса. Как витамины и микроэлементы могут влиять на синтез коллагена? И почему для достижения стойкого эффекта необходимо учитывать их количественный состав в организме?
Ежегодно создаются новые методики и препараты для улучшения синтеза коллагена с целью профилактики инволюционных процессов в организме и уменьшения выраженности возрастных изменений.
Но за стремлением повлиять на коллагеногенез извне порой забывают о тех веществах, без достаточного количества которых в самом организме синтез коллагена крайне затруднен. Никто не будет отрицать, что продукция этого жизненно важного белка зависит от гормонов, гормоны, в свою очередь, от присутствия металлов, усвоение металлов — от витаминов; и эту цепочку можно продолжать долго, тем более что она замкнутая. Осветить все нюансы в одной статье не представляется возможным, но сделать шаг навстречу пониманию некоторых процессов — в наших силах. Синтез и процессинг (созревание) коллагена включает в себя несколько этапов:
- транскрипция генов, кодирующих коллагены, в которой участвуют десятки магнийи кальцийзависимых белков;
- синтез препроколлагена на рибосоме, поддерживаемый магний- и кальцийзависимыми белками;
- транспорт цепи препроколлагена в эндоплазматический ретикулум посредством сигнального пептида на N-концевом участке аминокислотной цепи;
- удаление сигнального пептида в препроколлагене посредством фермента пептидазы;
- гидроксилирование аминокислотных остатков пролина с участием Fe2+ и аскорбат-аниона в качестве кофакторов;
- гликозилирование моносахаридами аминокислотных остатков лизина в препроколлагене в присутствии ферментов, содержащих ионы марганца;
- сборка тройной спирали проколлагена из 3 аминокислотных цепей препроколлагена;
- внесение необходимых конформационных изменений в проколлаген посредством изомеризации остатков цистеина и пролина;
- упаковка проколлагена в транспортный везикул, перенос во внеклеточный матрикс;
- вне клетки модификация молекулы проколлагена с помощью протеиназ проколлагена, нуждающихся в ионах Zn2+ как кофакторе;
- формирование коллагеновых фибрилл из тропоколлагена посредством лизилоксидазы, кофакторами которой являются ионы Cu+ и тирозил-хинон (рис. 1) [1].
Всем известно об участии магния и кальция в синтезе соединительной ткани и коллагена, но о железе, цинке, меди, витаминах С и D часто забывают. Именно эти кофакторы рассмотрим в статье.
Железо
Железодефицитная анемия в той или иной степени присутствует у 40–60 % женщин детородного возраста по всему миру [2, 26]. И это при том, что железо — один из важнейших микроэлементов, необходимых для нормального функционирования биологических систем организма. Оно требуется для осуществления функции дыхания, кроветворения, участвует в иммунобиологических и окислительно-восстановительных реакциях.
Причины дефицита железа:
- недостаточное поступление в организм железа из-за нарушения режима питания (например, при вегетарианской диете);
- снижение всасываемости железа в кишечнике (рис. 3);
- нарушение регуляции обмена витамина С;
- избыточное поступление в организм фосфатов, оксалатов, кальция, цинка, витамина Е;
- поступление в организм железосвязывающих веществ;
- усиленное расходование железа (в периоды интенсивного роста и беременности);
- потери железа, связанные с травмами, кровопотерями во время операций, обильными менструациями, язвенными болезнями, донорством, занятиями спортом;
- нарушение функции щитовидной железы;
- различные системные и опухолевые заболевания [21].
Учитывая высокую распространенность дефицита железа в популяции, сложно говорить о нормальном синтезе коллагена при таких состояниях.
Цинк — единственный металл, представленный в небелковой части ферментов каждого класса, и никаким другим металлом цинк не может быть заменен. Несмотря на малую концентрацию цинка в крови, стабильные связи с макромолекулами делают его доступным для всех тканей организма, что в дальнейшем позволяет удовлетворять потребности в нем белков и ферментов, выполняющих различные биологические функции [28].
Распространенность дефицита цинка в мире не менее значительная, чем железа и витамина С, и составляет до 60% [29].
Для транспорта эритроцитами кислорода и углекислого газа абсолютно необходим цинк, и большая часть цинка крови содержится именно в эритроцитах в составе цинковых металлоферментов — карбоангидраз. Карбоангидразы катализируют превращения углекислого газа в угольную кислоту (угольная кислота участвует в поддержании pH крови в физиологическом диапазоне (7,25–7,35). В капиллярах легких эти процессы идут в обратном направлении: угольная кислота распадается на углекислый газ и воду, и углекислый газ удаляется наружу [18].
Без нормального дыхания ни одна клетка не способна осуществлять свои функции.
В мире распространенность дефицита меди в организме, приводящего, наряду с железом, к анемии, составляет до 30%. А ведь этот микроэлемент крайне необходим для нормальной физиологии организма.
Если говорить о коже, то медь играет ключевую роль в ангиогенезе, синтезе и стабилизации белков внеклеточного матрикса [3].
В физиологически значимых концентрациях (2 мг — средняя суточная потребность) медь ускоряет заживление ран [16].
Ионы меди, которые являются кофакторами лизилоксидазы, принимают участие в последнем этапе синтеза коллагена. Медь имеет важное значение для формирования внутри- и межмолекулярных поперечных связей в коллагене, а соответственно, и прочности коллагеновых и эластиновых фибрилл [8, 13, 15]. Недостаток меди ухудшает формирование сшивок коллагена и приводит к тяжелой патологии костей, легких и сердечно-сосудистой системы [12].
Компенсация дефицита этого микроэлемента, бесспорно, улучшает синтез коллагена, в том числе в коже (рис. 4) [7, 10].
Аскорбиновая кислота (витамин С)
Аскорбиновая кислота играет в организме фундаментальную роль — нет фактически ни одного физиологического процесса, в котором бы она не принимала участия.
Роль витамина С в организме
Аскорбиновая кислота в организме человека оказывает влияние на множество важнейших биологических процессов:
- образование кортикостероидов (при стрессе в несколько раз возрастает уровень потребления витамина С тканями и органами) [20];
- обмен тирозина (влияние на обмен гормонов щитовидной железы) [22];
- трансформация дофамина в норадреналин [25];
- превращение токсичных соединений ванадия в безвредные [23];
- превращение фолиевой кислоты в ее активную форму — тетрагидрофолат [27];
- активация мРНК ацетилхолинового рецептора [20];
- образование активных форм витамина D (транспортной формы [25(OH)D] — в печени и активной гормональной формы [1,25(ОН)2D] — в почках), что служит основным фактором профилактики остеопороза [20];
- потенцирование всасывания железа [24].
Распространенность дефицита витамина С в мире по разным данным составляет 20–40% [14, 15].
В последнее время много исследований посвящено аскорбиновой кислоте и ее биодоступности для кожи [9]. При недостатке витамина С в организме его нанесение на кожу не будет иметь ожидаемого эффекта, так как не сможет восполнить нутритивный дефицит. В ходе проведенных исследований выяснилось, что витамин С ускоряет заживление ран, участвует в активизации синтеза коллагена I типа (рис. 5) и снижении параметров окислительного стресса. Никаких значимых побочных эффектов при добавлении витамина С в питание в ходе проведенных исследований выявлено не было [5, 6].
Синтез коллагена зависит от гормонов, гормоны, в свою очередь, от присутствия металлов, усвоение металлов — от витаминов, и эту цепочку можно продолжать долго, тем более что она замкнутая.
Витамин D
Распространенность дефицита витамина D в российской популяции составляет более 90% (в мире 50–60%) [19]. Этот витамин стимулирует увеличение синтеза секретируемых белков TGF-β (регулируют деление
и дифференцировку различных типов клеток, включая фибробласты и кератиноциты) и их связывание с рецепторами на мембране клеток. Поэтому при его дефиците происходит нарушение активности сигнальных каскадов TGF-β, что ухудшает заживление кожи после любой травмы (включая косметологические манипуляции). Например, во время термолифтинга часть коллагеновых волокон дермы сжимается и уменьшается в объеме. Это приводит к повышению зернистости базального слоя и при достаточном количестве витамина D создает благоприятные условия для воздействия его активных форм на экспрессию TGF-β1, который и способствует обновлению соединительной ткани [11].
Выводы
Мы кратко обсудили лишь некоторые кофакторы, участвующие в синтезе коллагена. Но даже этот незначительный пласт информации позволяет судить о зависимости синтеза коллагена от нутритивного статуса организма, чем не следует пренебрегать, решая многие эстетические задачи. Изменение синтеза коллагена происходит постепенно и усугубляется нутритивным дефицитом [19].
Источник