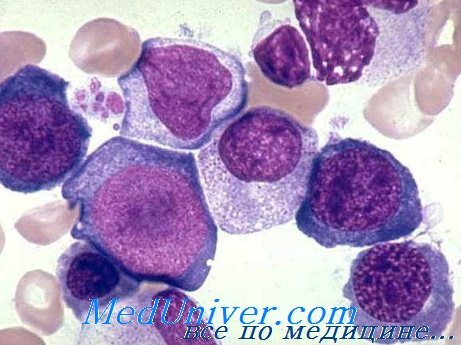
Анемия Бирмера
Анемия Бирмера (анемия Аддисона-Бирмера, бирмеровская анемия) — хроническое заболевание аутоимунной природы, являющееся наследственной формой мегалобластных анемий. Протекает циклически – рецидив сменяется ремиссией.
Раньше это заболевание называли прогрессивным злокачественным малокровием, поскольку оно всегда приводило к летальному исходу, но теперь благодаря лечению этого не случается, поэтому анемию называют по имени ее исследователей. А после того, как доказали роль витамина В12 в ее возникновении, бирмеровскую анемию называют одной из форм (пернициозной) В12-дефицитной анемии, при которой поражаются кроветворная функция, пищеварительная и нервная системы. Обычно болеют женщины в возрасте 50-60 лет.
Признаки
Анемия начинается постепенно и очень незаметно. Появляются жалобы на быструю утомляемость, слабость, головные боли, головокружение, сердцебиение и одышку при движениях. Иногда основными признаками являются диспептические явления (понос, отрыжка, тошнота, жжение в кончике языка). Иногда появляются такие нарушения нервной системы, как парестезии (спонтанно возникающие неприятные ощущения «мурашек», онемения, покалывания), похолодание конечностей, шаткость походки.
Цвет кожи – бледный с лимонным оттенком, склеры немного желтушны, лицо одутловато, иногда отечны голени и стопы. Грудина болезненна при поколачивании. Температура субфебрильная (чуть выше 37), но в период рецидива повышается до 38—39°.
При изменениях в пищеварительном тракте появляется глоссит Гентера (появление на языке красноватых неправильно очерченных, зудящих пятен). Язык иногда болит и жжется, постепенно становится гладким (полированным). У половины больных увеличивается печень и у пятой части — селезенка.
При поражении сердечно-сосудистой системы появляются тахикардия (учащенный пульс), гипотония (пониженное давление), увеличение размеров сердца, глухость тонов и т.д.
Со стороны нервной системы и психики — адинамия (резкий упадок сил).
Описание
Доказано, что природа болезни Аддисона-Бирмера – аутоиммунная. Она бывает у больных такими аутоиммунными заболеваниями, как диффузный токсический зоб, первичная надпочечниковая недостаточность, хронический лимфоцитарный тиреоидит (эутиреоидный или гипотиреоидный), витилиго и гипопаратиреоз.
Важную роль играет также наследственность — родственники людей с бирмеровской анемией чаще страдают этим заболеванием
Бирмеровская анемия может быть связана с атрофией слизистой оболочки желудка. Причина этой анемии — нарушение выработки желудком особого белка — гастромукопротеина (внутренний фактор Касла), который обеспечивает всасывание в кишечнике витамина B12. Такие дефицитные анемии возникают при сифилисе, полипозе, раке, лимфогранулематозе и других патологических процессах в желудке, а также при его удалении. Они возможны при глистных заражениях широким лентецом, спру, после удаления тонкой кишки, при лечении некоторыми лекарственными препаратами, а также при беременности.
Прием глюкокортикоидов вызывает ремиссию – временное ослабление или исчезновение признаков заболевания.
Диагностика
Диагностировать заболевание можно по клиническим признакам дефицита витамина В12. Кроме того, проводятся морфологические исследования крови, костного мозга и определяется кислотность желудочного сока.
Лечение
Лечение наследственных форм мегалобластных анемий проводится после установления диагноза и специального обследования больного в специализированных гематологических клиниках. Наиболее эффективным средством лечения является витамин В12. Его правильное применение полностью и навсегда устраняет нарушения, вызванные дефицитом витамина В12, если до лечения не возникли необратимые изменения в нервной ткани. Но больные остаются уязвимыми к появлению аденоматозных полипов желудка и раза в два чаще болеют раком желудка. Им показано наблюдение, включающее регулярное проведение специальной пробы, а также, если нужно, дополнительных исследований.
В случаях пернициозно-анемической комы немедленно переливается кровь (не более 150—200 мл) или (что лучше) эритроцитарная масса (иногда повторная) вместе с ударными дозами витамина B12.
Если причиной бирмеровской анемии является широкий лентец, то вылечивают ее дегельментизацией.
Если причиной стал сифилис, назначается специфическое лечение.
Больные анемией Бирмера в период ремиссии находятся на диспансерном учете. Им систематически проводятся ежемесячный анализ периферической крови и периодические исследования нервной системы, а также рентгеноскопия желудка для исключения рака, который возможен при бирмеровской анемии.
Профилактика
Анемия Аддисона-Бирмера занимает 2-е место по важности и частоте в группе дефицитных анемий. Для ее профилактики необходимо вовремя:
- лечить гастриты (с повышенной и пониженной кислотностью);
- лечить паразитарные заболевания (глистные и т.д.);
- применять витамин В12 после резекций желудка, при хронических поносах, воспалительных заболеваниях или пороках развития тонкого кишечника;
- лечить алкоголизм;
- контролировать функцию печени;
- при имеющейся наследственности или аутоиммунных заболеваниях принимать препараты или поливитамины, содержащие витамин В12.
- не использовать длительное время препараты, уменьшающие кислотность желудка.
С целью профилактики рецидивов больным систематически вводят витамин B12 (1-2 раза в месяц) или камполон (2 раза в месяц). В весенне-осенние месяцы, когда рецидивы учащаются, инъекции делают 1 раз в неделю. Больные анемией должны понимать, что ремиссия – это не выздоровление, и поэтому все рекомендации врача нужно строго выполнять.
Источник
Анемия Аддисона-Бирмера
Анемия Аддисона-Бирмера (В12-дефицитная анемия)– заболевание, при котором нарушен процесс кроветворения по причине дефицита витамина В12 в организме.
Анемия Аддисона-Бирмера развивается при дефиците витамина В12, причиной которого может быть:
— Нарушение питания (голодание, строгая диета, вегетарианство),
— Недостаточная выработка фактора Касла, который помогает витамину В12 всасываться в кишечнике;
— Хирургические операции на органах ЖКТ;
— Период беременности и лактации;
Симптомы анемии Аддисона-Бирмера
Все симптомы заболевания объединены в три синдрома: анемический, гастроэнтерологический и неврологический.
При анемическом синдроме пациенты жалуются на быструю утомляемость, головокружения, шум в ушах, точки перед глазами, учащенное сердцебиение и одышку.
Гастроэнтерологический синдром при анемии Аддисона-Бирмера проявляется тошнотой, запорами, похудением и другими нарушениями работы ЖКТ. Язык больного приобретает красный или малиновый оттенок, а его поверхность становится гладкой.
К неврологическому синдрому относятся судороги, онемение конечностей, мышечная слабость.
Диагностика анемии Аддисона-Бирмера
Чтобы поставить точный диагноз и узнать причину заболевания, больному необходимо обратиться к врачу, который проведет осмотр и изучит анамнез жизни пациента, и сдать анализы крови.
При анемии Аддисона-Бирмера в крови снижено количество эритроцитов, ретикулоцитов и тромбоцитов, а также уровень гемоглобина в крови.
При биохимическом анализе крови наблюдается повышенное количество билирубина, образующегося при распаде эритроцитов, и железа, т.к. снижено его использование при образовании эритроцитов.
Пункция костного мозга определяет наличие увеличенных эритроцитов с остатками ядер. Также проводится ЭКГ, показывающее у больного нарушение ритма сердца.
Лечение анемии Аддисона-Бирмера
Лечебная терапия имеет несколько направлений: лечение заболевания, ставшего причиной анемии, устранение провоцирующих факторов и нормализация уровня витамина В12.
Больному внутримышечно вводят витамин В12, чтобы восстановить его нормальный уровень в организме. Пациенту следует придерживаться диеты, рацион которой богат белком и витамином В12. В пищу рекомендуется употреблять мясо, печень, рыбу, яйца и молочные продукты. Рацион должен быть сбалансированным и включать в себя все витамина и минералы, необходимые организму для нормальной работы.
В случаях, когда присутствует угроза жизни пациента, проводится переливание эритроцитарной массы.
При своевременном и правильном лечении анемия Аддисона-Бирмера хорошо поддается лечению.
Профилактика анемии Аддисона-Бирмера заключается в правильном питании, при котором рацион должен быть богат всеми необходимыми элементами для нормальной жизнедеятельности организма.
РАСПИСАНИЕ ТАБ щитовидной железы апрель 2021 г.
Уважаемые пациенты!
ТАБ щитовидной железы проходит по предварительной записи :09.04.21 с 15.00, 14.04.21 с 16.00, 15.04.21 с 16.00, 17.04.21 с 16.00, 21.04.21 с 17.00, 22.04.21 с 16.00, 24.04.21 с 16.00, 26.04.21 с 16.00, 28.04.21 с 16.00, 30.04.21 c 16.00 ТАБ проходит под контролем УЗИ. Готовность исследования- до 5 рабочих дней (с учетом праздничных дней). Стоимость- 2300 руб. Если Вам дополнительно требуется сдать анализы крови на гормоны или какие-либо другие исследования крови (клинические, биохимические), то просим быть в медцентре за 15 мин.до назначенного времени ТАБ. Анализы крови оплачиваются отдельно. У нас своя лаборатория.
подробнее »
Анализ на антитела IgG к COVID-19
Уважаемые пациенты!
По Вашим многочисленным просьбам, мы расширили список проводимых исследований:
-а/т IgG (количественно)после вакцинации или перенесенного заболевания; общий анализ мокроты и посев мокроты на аэробную и и факультативно-анаэробную флору с определением чувствительности к антибиотикам; ананализ крови на а/т IgA, IgG, IgM к Chlamydia trachomatis.
подробнее »
Источник
Ведущей причиной развития анемии аддисона бирмера является дефицит витамина
Болезнь Бирмера (Аддиссона-Бирмера) или «злокачественная анемия» наиболее частая и лучше изученная форма дефицита витамина В12.
История болезни начинается описанием Аддиссоном (1885) «генуинной» анемии у хорошо питающихся лиц; о желудочных дегенеративных поражениях высказывал предположение Флинт (1860), что, в дальнейшем было подтверждено Fenwick (1870) на секционном материале, в то время как бескислотность, доказанная Cohn и Mehring уже в 1886 г. лишь спустя несколько десятков лет была признана в качестве обязательного симптома болезни.
Бирмеру мы обязаны анатомоклиническим описанием «злокачественной анемии» (1868—1872), хотя большинство рассмотренных им случаев видимо в действительности, составляли виды анемии за счет недостатка фолиевой кислоты (Castle, 1970).
Описание мегалобласта Эрлихом в 1908 г. заложило основу морфологического диагноза, увенчавшегося в дальнейшем практикой костномозговых пункций.
Начало патофизиологического этапа отмечено успешным применением пероральной гепатотерапии (Minot и Murphy), после чего, постепенно, путем очистки печеночных экстрактов, удалось выделить витамин В12 и синтезировать его. В 1938 г. Castle доказал роль внутреннего фактора в патогенезе этого заболевания. На последующих этапах были достигнуты большие успехи в изучении метаболизма витамина В12 и его взаимосвязь с другими метаболическими процессами, к тому же был приведен ряд аргументов, в пользу высказывания об аутоиммунном патогенезе с описанием нескольких генетических болезней, касающихся ферментов, которые зависят от витамина В12.
На основе современных знаний болезнь Бирмера можно определить как болезненное состояние, характеризующееся изменениями мегалобластического вида клеток периферической крови и костного мозга и дегенеративными поражениями слизистых оболочек пищеварительного тракта и нервной системы в связи с недостаточным поглощением витамина В12 по причине отсутствия внутреннего фактора, что, видимо создается каким-то аутоиммунным механизмом на наследственном фоне.
Частота заболевания значительно колеблется в зависимости от географической области при этом болезнь чаще в странах, населенных «северными расами» (Голландия, Скандинавский полуостров, Англия, США, Канада), чем на востоке и юге Европы и совсем редко встречается на Дальнем Востоке и среди негроз (Gummert). Более высокий показатель частоты у женского пола (5:2) не подтвержден всеми авторами.
По возрастным группам наиболее высокий показатель приходится на группу 45—55 лет, однако процент заболевших растет неуклонно в последующих группах.
Экономические и трудовые (профессиональные) условия не оказывают существенного влияния на показатель частоты этого заболевания «эндогенного детерминизма» (в отличие от мегалобластической анемии за счет недостатка фолиевой кислоты).
В болезни Бирмера роль строения и наследственности была выявлена при описании первых случаев (Аддисон). В дальнейшем высказывалось предположение о взаимосвязи с определенными соматическими, нервными или эндокринными строениями, была отмечена частота отдельных соматических черт (широкое лицо, отдаленные глаза, белесный цвет волос, раннее появление седины и пр.), которые, в, настоящее время, не считаются показательными.
Более важным представляется рост частоты полностью развившегося заболевания или его частичного проявления в семье больного.
По материалам Вернера (цит. Бегеманном), проводившего исследования в ряде семей страдающих, у 9% обследованных были отмечены иные явные случаи заболевания, а в 15% — частичные проявления [скрытые или исходные признаки болезни]. Среди близких родственников больного наиболее часто наблюдались заниженность или отсутствие кислотности (19%), желудочно-кишечные расстройства (33%), холе-цистопатия (15%) (реже — 8%—изменения языка), парестезия (25%) (в некоторых семьях наблюдалось развитие заболевания в сопровождении невропатии); из числа гематологических сдвигов отмечены мокроцитоз, овалицотоз, гиперсегментирование (примерно в 23% случаев).
Болезнь Бирмера описана и у одножелточных близнецов (Arbo и Mohr).
Другими аргументами, выступающими за генетический детерминизм болезни являются значительная частота антител против пристеночных клеток и сокращение ВФ у родственников больного (Ардеман и сотр.), также возможно, существенно увеличенная частота кровяной группы А (II) у страдающих бирмеровской анемией. К тому же выявлены (Асталди и сотр.,) количественные и качественныз изменения хромосом (непостоянные, нехарактерные).
По одному из предложенных генетических объяснений болезнь передается посредством гена, вовлеченного в процесс образования внутреннего фактора, при этом дефицит передается доминантным способом, но с небольшой проницаемостью; гомозитотное состояние видимо обусловливает ювенильную форму заболевания (при врожденном отсутствии внутреннего фактора), в то время как для проявления болезни в гетерозиготных условиях (обычной у взрослых) предполагается необходимым образование, во времени, атрофических поражений слизистой оболочки желудка (под воздействием каких-то эпигенетических факторов).
Вероятность наличия полигенетического механизма подсказывается относительно большой частотой случаев «конституционной гипохромной анемии» (с заниженным выделением желудочного сока, воспалением слизистой оболочки языка и пр.) среди родственников больного.
Второй основной вопрос патогенеза болезни Бирмера связан с нали чием аутоиммунных антител у большинства больных.
В сыворотке примерно 40% страдающих имеются антитела против ВФ, в то время как у примерно 90% — антитела против пристеночных клеток. Последние (примерно в размере 30% случаев) выявляются и при других заболеваниях аутоиммунного патогенеза, таких как тиреоз Хашимото, тиреотоксикоз, генуинная недостаточность надпочечной железы (Ирвине и сотр.). С другой стороны у 40—50% страдающих отмечается наличие противощитовидных антител.
Однако антитела против пристеночных клеток встречаются и при простом атрофическом гастрите (60%) или даже у лиц, страдающих невыявимыми заболеваниями (5—8%), особенно у женщин старше 60 лет (Ирвине и сотр.). Поставлен вопрос о том, не составляет ли развитие этих аутоантител вторичное явление изменению антител клеточных структур.
Антитела против внутреннего фактора находятся в разной пропорции в слюне и желудочном соке страдающих бирмеровской болезнью; их роль в сокращении поглощения витамина В1а доказана. Что касается роли антител против пристеночных клеток в патогенезе поражения слизистой оболочки желудка вопрос остается еще невыясненным (участвуют иммунологические механизмы гуморального и клеточного видов в обстановке разных эндо- и экзогенных факторов).
С диагностической точки зрения в случае мегалобластической анемии присутствие антител против пристеночных клеток указывает, с большой вероятностью, на наличие болезни Бирмера, в то время как выявление антител против внутреннего фактора свидетельствует о развитии этого заболевания почти с достоверностью (Williams).
Другим аргументом в пользу аутоиммунного патогенеза болезни Бирмера служит способность глюкокортикостероидов обусловливать (временно) регрессию поражений слизистой желудка и понижение коэффициента антител против внутреннего фактора (Robro и сотр.).
На сонове этих аргументов, выступающих, с одной стороны, за наследственный характер болезни, а с другой, за аутоиммунный фактор патогенеза в настоящее время многие авторы склонны рассматривать болезнь Бирмера как результат генетического недостатка, вызывающего иммунологическое нарушение, которое заключается в низкой иммуной переносимости в отношении клеток желудочного эпителия (и других клеток одинакового эмбриологического происхождения), в связи с чем проявляются аутоантитела (под воздействием добавочных факторов).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник