Неврологические проявления дефицита витамина В12
- КЛЮЧЕВЫЕ СЛОВА: витамин, дефицитарные состояния, миелоз, энцефалопатия, деменция, гипергомоцистеинемия, диагностика, лечение, Нейробион
Витамин B12 – водорастворимый витамин, который в природе вырабатывается микроорганизмами, а в организме человека не синтезируется. Средняя суточная потребность в витамине B12 составляет 2,4 мкг для мужчин и небеременных женщин, 2,6 мкг для беременных, 2,8 мкг – для кормящих [1].
Основной источник витамина B12 – белки животного происхождения (мясо, печень, почки, рыба, молочные продукты, яичные желтки). Запасы витамина В12 в организме взрослого человека составляют примерно 2000–5000 мкг. Витамин B12 депонируется в основном в печени (1 мкг в 1 г ткани печени), в меньшем количестве – в почках и скелетных мышцах. В12 выделяется с желчью и калом, в сутки теряется 0,1% общего количества депонированного витамина. Существует кишечно-печеночный кругооборот витамина В12 – около 3/4 выделенного с желчью витамина вновь реабсорбируется в кишечнике через систему воротной вены печени (энтерогепатическая циркуляция). Этим объясняется развитие клинических проявлений дефицита В12 через 1–3 года после полного прекращения его поступления в организм [2].
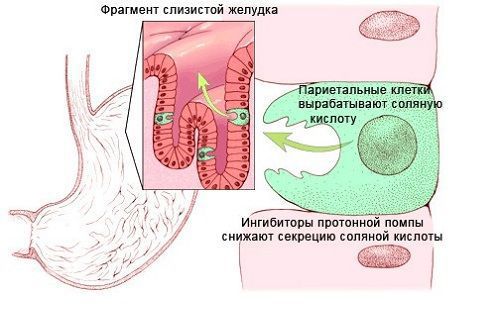
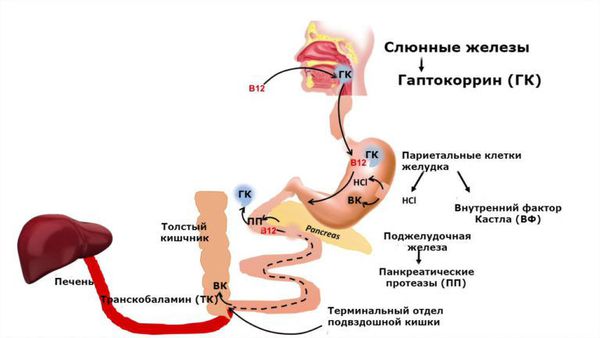
В продуктах питания В12 обычно содержится в форме кофермента дезоксиаденозилкобаламина или метилкобаламина и связан с белками. На первом этапе метаболизма витамина В12 происходит его протеолиз в желудке при низком pH, в результате чего он высвобождается из пищевого белка и связывается с белком R желудочного сока. Париетальные клетки желудка вырабатывают внутренний фактор Касла – гликопротеид, который вместе с белковым комплексом «кобаламин – R» поступает в двенадцатиперстную кишку. Комплекс внутреннего фактора Касла и кобаламина в подвздошной кишке связывается с рецепторами внутреннего фактора кобаламина, расположенными на микроворсинках клеток слизистой оболочки подвздошной кишки. При нейтральном рН и в присутствии ионов кальция комплекс «кобаламин – фактор Касла» распадется, кобаламин попадает в энтероцит, переносится на транскобаламин II (голотранскобаламин) и в комплексе с ним попадает в кровоток. При наличии большого количества витамина В12 около 1% может проникать в кровь за счет пассивной диффузии [1, 2].
B12 участвует во многих ключевых процессах метаболизма липидов, углеводов и белков, играет центральную роль в гемопоэзе. В организме человека витамин В12 служит кофактором для работы двух ферментов – метилмалонил-коэнзим A (CoA)-мутазы в митохондриях и метионинсинтетазы (MeCbl) в цитоплазме. Витамин В12 участвует в синтезе нуклеиновых кислот: связанный с MeCbl, он облегчает удаление метильной группы из метилфолата с образованием гомоцистеина (HCYS), который превращается в метионин. Витамин B12 необходим для клеточного дыхания и поддержания энергии, поскольку задействован в цикле Кребса. B12 участвует в процессах миелинизации и нормального формирования нервной трубки на этапе эмбриогенеза, синтезе нуклеиновых кислот, белковых и липидных структур миелиновой оболочки нервного волокна, холина и нейротрансмиттеров [2, 3].
Причины развития дефицита витамина В12
Причин развития дефицита витамина В12 много. Их можно разделить на несколько групп.
Недостаточное поступление витамина В12 с пищей
К дефициту В12 может привести недостаточное употребление белков животного происхождения в силу различных причин (пожилой возраст, низкий социальный статус, в частности у лиц, страдающих хроническим алкоголизмом). Большинство вегетарианцев получают только 0,25–0,5 мкг кобаламина в день. Не случайно распространенность дефицита витамина B12 среди них достигает 40–80% [3].
Нарушение всасывания и метаболизма витамина В12 в желудочно-кишечном тракте
Подобные состояния имеют место у пациентов после операций на желудке или тонком кишечнике, в том числе после бариатрических операций по поводу патологического ожирения, лиц, страдающих атрофическим гастритом (чаще пожилых людей), пациентов с заболеваниями тонкой кишки, недостаточностью поджелудочной железы и синдромом мальабсорбции, целиакией, глистными инвазиями, дивертикулярной болезнью. Дефицит В12 нередко развивается при ожоговой болезни или тяжелых травмах на фоне заместительной почечной терапии, а также при хроническом воздействии токсигенной плесени и микотоксинов (чаще встречаются в поврежденных водой зданиях). К нарушению всасывания и метаболизма витамина В12 могут приводить генетические дефекты, при которых нарушается синтез переносчиков кобаламина [2, 4].
Повышенная потребность в витамине В12
Беременные, кормящие женщины, дети раннего возраста, пациенты с ВИЧ/СПИДом, гемолитической анемией испытывают повышенную потребность в витамине B12.
Снижение содержания витамина B12 относится к этиологическим факторам ряда врожденных пороков. Речь прежде всего идет о дефектах формирования нервной трубки.
Низкие концентрации витамина В12 ( 12 мкмоль/л и MMК > 0,4 мкмоль/л. Однако ориентироваться только на эти показатели не следует, поскольку повышенный уровень HCYS имеет место при дефиците фолатов, витамина В6, гипотиреозе, а повышенный уровень ММК – при печеночной и почечной недостаточности [22, 24].
Еще одним методом диагностики дефицита В12 является определение уровня холотранскобаламина в сыворотке крови. В норме концентрация холотранскобаламина составляет от 19–42 до 134–157 пмоль/л. К преимуществу метода определения концентрации холотранскобаламина относится то, что его уровень в крови достаточно стабилен и практически не подвержен колебаниям при различных физиологических состояниях организма (беременность, прием некоторых лекарственных препаратов) [22].
Таким образом, на текущий момент золотого стандарта лабораторной диагностики дефицита витамина В12 не существует. Для точной постановки диагноза его дефицита необходима комплексная оценка клинических проявлений и лабораторных данных (общий уровень В12 в плазме и ликворе, уровень сывороточного холотранскобаламина, гомоцистеина и ММК).
На рисунке представлен возможный алгоритм диагностики дефицита витамина В12 у взрослых [25].
Терапия неврологических проявлений дефицита витамина В12
Целями терапии В12-дефицитных состояний являются нормализация лабораторных показателей крови и постепенный регресс неврологического дефицита. Одновременно с медикаментозным восполнением дефицита витамина В12 необходимы обследование, тщательный сбор анамнеза для выявления причины развития дефицитарного состояния и ее устранения или коррекции. Прогноз функционального восстановления зависит от исходной степени поражения нервной системы: при легких нарушениях и раннем начале лечения возможно полное или практически полное восстановление, при более тяжелых остаточный неврологический дефицит неизбежен.
Пациенты с доказанным дефицитом витамина В12 могут получать терапию в виде пероральных форм витамина, а также парентерально (главным образом внутримышечно), что зависит от тяжести неврологических проявлений, остроты развития заболевания и причины дефицита.
Как правило, пациентам в отсутствие нарушений всасывания в желудочно-кишечном тракте (ЖКТ) в случае постепенного развития неврологического дефекта и легкой или средней тяжести его выраженности показан прием пероральных препаратов, содержащих 1 мг кобаламина, ежедневно. При тяжелой степени неврологического дефекта и остром развитии заболевания, а также при состояниях, потенциально способных нарушать всасывание витамина В12 в ЖКТ, целесообразно начинать терапию с парентеральных форм витамина и его внутримышечного введения в дозе 1 мг [26, 27].
Единого мнения об оптимальных дозах витамина В12, направленных на коррекцию неврологических и гематологических проявлений дефицита, не существует.
В исследовании сравнивали эффективность лечения различными дозами перорального витамина B12 у пожилых больных с дефицитом В12. Установлено, что оптимальная доза перорального витамина B12, необходимая для снижения уровня ММК на 80–90%, составляет 647–1032 мкг/сут [28].
Начальные схемы лечения и продолжительность витаминотерапии в разных исследованиях, медицинских учреждениях и странах различаются.
Одна из предлагаемых схем лечения предполагает внутримышечные инъекции кобаламина – 8–10 инъекций в течение двух месяцев с последующими ежемесячными инъекциями по 1 мг препарата. Другие схемы включают пероральное введение кобаламина ежедневно в течение десяти дней, затем еженедельно в течение четырех недель с последующим ежемесячным приемом препарата внутрь. Британский национальный формуляр рекомендует использовать 1 мг витамина B12 внутримышечно три раза в неделю в течение двух недель, а затем один раз каждые три месяца для пациентов с мегалобластной анемией без неврологических синдромов. При наличии неврологических симптомов целесообразно внутримышечное введение 1 мг В12 через день в течение трех недель. Лечение может быть продолжено в зависимости от клинической ситуации. Пациентам с дефицитом витамина В12, причины которого невозможно устранить, как правило, требуется пожизненное лечение для предотвращения рецидива заболевания [26].
В руководстве по гематологии [27] для лечения В12-дефицитной анемии предложена следующая схема: цианокобаламин 1000 мкг внутримышечно ежедневно в течение 4–6 недель, после нормализации показателей крови 1000 мкг внутримышечно один раз в неделю, затем пожизненно 1000 мкг один раз в месяц, если устранить причину дефицита витамина В12 невозможно. Подобная схема применима и при тяжелых неврологических нарушениях, обусловленных дефицитом витамина В12. Пациенты, получающие лечение по поводу дефицита витамина B12, каждые несколько месяцев проходят лабораторный контроль уровня гемоглобина и витамина В12 [27].
При приеме цианокобаламина перорально в высоких дозах (1000–2000 мкг) возможно пассивное (за счет диффузии) всасывание 1% потребляемой дозы. В ряде исследований показано, что прием препаратов витамина В12 внутрь в высоких дозах по эффективности не уступает внутримышечному введению [24, 28]. В руководстве по гематологии также предложена альтернативная внутримышечному введению витамина В12 схема лечения: ежедневный прием препарата в дозе 2000–4000 мкг в течение 4–6 недель, затем 1000 мкг цианокобаламина один раз в месяц пожизненно [27].
В России единственной лечебной формой витамина В12 является цианокобаламин, который входит в состав комбинированных поливитаминных препаратов в таблетированной форме в дозах 200–500 мкг. Неинъекционных средств для специфического лечения дефицита витамина В12 в настоящее время нет.
Среди препаратов, содержащих витамин В12, следует отметить Нейробион (Австрия), который более 50 лет применяется в разных странах для лечения пациентов с заболеваниями нервной системы. Нейробион представляет собой комбинацию нейротропных витаминов: тиамина (витамин В1), цианокобаламина (витамин В12) и пиридоксина (витамин В6). Препарат выпускается в двух лекарственных формах – пероральной (таблетки) и парентеральной (раствор для инъекций). Одна таблетка Нейробиона содержит тиамина дисульфид 100 мг, пиридоксина гидрохлорид 200 мг и цианокобаламин 240 мкг. Одна ампула Нейробиона также содержит три витамина группы B: тиамин 100 мг, пиридоксин 100 мг и цианокобаламин 1 мг.
Как правило, лечение тяжелых форм поражения центральной и периферической нервной систем начинается с парентерального введения комплекса витаминов группы В. Инъекции Нейробиона проводят глубоко внутримышечно по 3 мл (одна ампула) один раз в сутки в течение десяти дней. Затем в качестве поддерживающей терапии Нейробион применяется в таблетированной форме. Стандартный лечебный курс для взрослых и детей старше 15 лет предполагает прием одной таблетки три раза в сутки на протяжении 1–3 месяцев в зависимости от тяжести клинических проявлений [29].
Пациенты с неврологическими нарушениями, обусловленными дефицитом витамина В12, помимо восполнения его дефицита в зависимости от конкретной патологии нуждаются в ноотропной и метаболической терапии, антиоксидантах (препараты альфа-липоевой кислоты). Им также назначаются реабилитационные мероприятия (массаж, лечебная физкультура, физиопроцедуры). Описана эффективность ритмической транскраниальной магнитной стимуляции при поражении спинного мозга на фоне фуникулярного миелоза [20].
Скорее всего распространенность дефицита витамина В12 в популяции значительно выше, чем принято считать. Это обусловлено увеличением продолжительности жизни и соответственно доли лиц пожилого и старческого возраста, высокой популярностью различных видов диет и вегетарианства, широким применением препаратов, способных нарушать всасывание и метаболизм витамина В12, и рядом других причин. Клинические проявления дефицита витамина В12 весьма разнообразны и включают в себя широкий спектр нарушений – от классической макроцитарной анемии до выраженных когнитивных и психических расстройств. Из-за отсутствия четких схем диагностики и недоступности в ряде случаев лабораторных исследований дефицит витамина В12 часто остается недиагностированным.
Ранняя диагностика неврологических проявлений дефицита витамина В12 и своевременное начало терапии крайне важны, поскольку позволяют сделать процесс неврологического дефицита обратимым.
Таким образом, проблема дефицита В12 требует дальнейшего изучения. Необходимо разработать четкие алгоритмы диагностики и лечения данной патологии.
Источник
В12-дефицитная анемия — симптомы и лечение
Что такое в12-дефицитная анемия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Слесарчук О. А., гематолога со стажем в 15 лет.
Определение болезни. Причины заболевания
B12-дефицитная анемия (B12ДА) — это заболевание, при котором снижается уровень эритроцитов и гемоглобина из-за недостатка в организме витамина В12.
Синонимы: анемия Аддисона — Бирмера, мегалобластная, пернициозная анемия.
Витамин B12 участвует в образовании всех клеток крови (эритроцитов, лейкоцитов, тромбоцитов), клеток желудочно-кишечного тракта и обеспечивает нормальное функционирование клеток нервной системы. Поэтому при анемии, связанной с дефицитом витамина B12, часто наблюдаются признаки поражения желудочно-кишечного тракта и нервной системы, а в анализе крови снижается уровень тромбоцитов и лейкоцитов [3] .
Распространённость
B12ДА встречается у 1500 человек на 1 миллион населения, как у детей, так и у взрослых. Однако чаще болеют люди старше 60 лет. У женщин заболеваемость выше, чем у мужчин: соотношение 10:7 [1] [2] .
Причины B12-дефицитной анемии
Причинами развития B12ДА являются недостаточное поступление витамина в организм, нарушение его высвобождения из пищи, нарушение всасывания, транспорта, обмена (метаболизма) или повышенное его расходование. Разберём подробнее каждую причину.
1. Недостаточное поступление. Витамин B12 содержится только в продуктах животного происхождения. Если с пищей поступает мало витамина В12 или не поступает совсем, например при вегетарианстве или веганстве, через 2-4 года развивается B12ДА. У грудных детей дефицит может развиться при сниженном содержании B12 в грудном молоке из-за дефицита витамина у матери [1] [2] [3] [4] [8] .
2. Нарушение высвобождения В12 из пищи может быть вызвано следующими причинами:
- Утратой или повреждением париетальных клеток желудка. Витамин B12 в пище присутствует в белковой форме. В желудке В12 высвобождается из пищи под воздействием соляной кислоты и ферментов желудочного сока, расщепляющих белок. Соляная кислота вырабатывается париетальными клетками желудка. Причинами нарушения её продукции может быть утрата или повреждение париетальных клеток в результате:
- Хирургического вмешательства на желудке: тотальной или субтотальной резекции, например при раке желудка.
- Атрофического гастрита — хронического воспаления желудка. В том числе аутоиммунного гастрита, при котором иммунная система ошибочно распознаёт париетальные клетки желудка как чужеродные и разрушает их с помощью специфических антител.
- Рака или полипоза желудка, которые повреждают и вытесняют париетальные клетки слизистой оболочки.
- Недостатком ферментов поджелудочной железы. После высвобождения из пищевых белков витамин В 12 связывается с белком слюны гаптокоррином, который защищает витамин от кислой среды желудка. В двенадцатиперстной кишке В12 высвобождается под воздействием ферментов поджелудочной железы. Причинами нехватки ферментов может быть недостаточность поджелудочной железы, хронический панкреатит или синдром Золлингера — Эллисона (опухоль поджелудочной железы) [17] .
3. Нарушение всасывания витамина в тонком кишечнике. Возможные причины:
- Недостаток внутреннего фактора Кастла. После высвобождения витамина из белков слюны В12 связывается с внутренним фактором Кастла — белком, который вырабатывают париетальные клетки желудка. Только благодаря этой связи витамин может всасываться в тонком кишечнике. Причины недостатка внутреннего фактора Кастла:
- Врождённый дефицит внутреннего фактора Кастла — наследственное заболевание, которое характеризуется дефектом гена, ответственного за образование этого фактора.
- Утрата париетальных клеток желудка.
- Врождённые и приобретённые болезни кишечника:
- Синдром Имерслунд — Гресбека — редкое наследственное заболевание, вызванное нарушением работы рецептора сubam в подвздошной кишке. С помощью этого рецептора происходит всасывание витамина В12.
- Целиакия — непереносимость глютена, при которой повреждается слизистая оболочка тонкого кишечника.
- Болезнь Крона — хроническое воспалительное заболевание кишечника.
- Опухоли тонкого кишечника, в том числе лимфомы.
- Резекция участка подвздошной кишки.
- Длительный приём некоторых лекарственных препаратов: ингибиторов протонной помпы, аминосалициловой кислоты, метформина, колхицина, неомицина, бигуанидов, циметидина, оральных контрацептивов и др. [1][2][3][4][6][9][10]
4. Нарушение транспорта. После всасывания в кишечнике витамин B12 поступает в кровь, где связывается с белком-транспортёром транскобаламином II. Он доставляет витамин клеткам-потребителям. Врождённый дефект белка-транспортёра либо появление к нему антител приводит к нарушению транспорта витамина B12 и к его дефициту [11] .
5. Нарушение метаболизма. Проникая из крови в клетки, витамин B12 принимает участие в сложных биохимических процессах, приводящих к синтезу ДНК, делению и созреванию клеток, обмену жирных кислот и гомоцистеина. Врождённые и приобретённые дефекты ферментов, обеспечивающих эти процессы, могут приводить к развитию B12ДА [2] [4] .
6. Повышенное расходование витамина В12. Может быть вызвано [4] :
- Состояниями, связанными с повышенным потреблением: многоплодная беременность [18] , тиреотоксикоз[19] , онкогематологические заболевания (множественная миелома, миелопролиферативные заболевания).
- Конкурентным потреблением витамина: бактериями, например при дивертикулёзе и синдроме «слепой петли»; паразитами — при дифиллоботриозе и власоглаве [3] .
Симптомы В12-дефицитной анемии
При дефиците внутреннего фактора, дефиците транспортного белка, нарушении внутриклеточного метаболизма и некоторых других врождённых состояниях симптомы B12ДА могут появиться у детей в первые месяцы или годы жизни. При недостаточности поступления с пищей или нарушении всасывания симптомы развиваются постепенно, обычно у детей в возрасте старше 7 лет и у взрослых.
Все проявления B12ДА можно разделить на 3 группы:
- симптомы, связанные со снижением гемоглобина — анемический синдром;
- симптомы поражения желудочно-кишечного тракта — гастроэнтерологический синдром;
- симптомы поражения нервной системы — нейропсихический синдром.
Каждая из этих групп симптомов может присутствовать по отдельности, а может встречаться их сочетание.
Анемический синдром
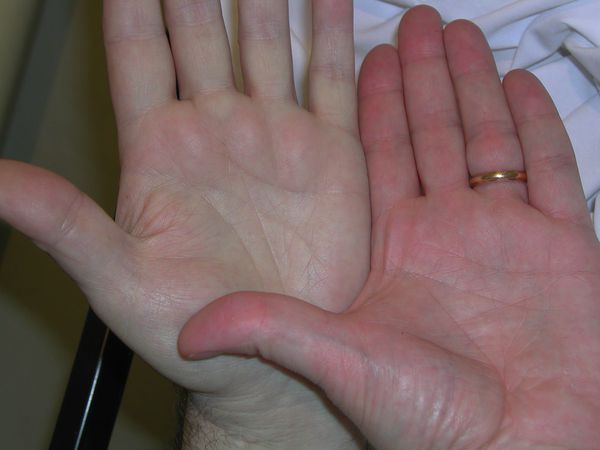
При B12ДА, как и при любой анемии, наблюдается бледность кожи, иногда с желтушным оттенком. Может беспокоить общая слабость, повышенная утомляемость, сонливость, одышка при незначительной физической нагрузке.
Возможно учащённое сердцебиение, шум в ушах, головокружение, потемнение в глазах, мелькание «мушек» перед глазами. Обращает на себя внимание снижение памяти, работоспособности, успеваемости в школе или ВУЗе. У детей на фоне анемического синдрома возможно нарушение роста и развития.
Симптомы поражения желудочно-кишечного тракта
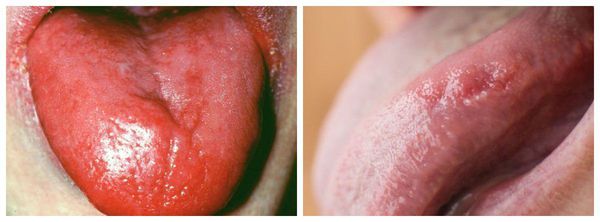
Для больных B12ДА специфичным симптомом является воспаление языка, которое сопровождается неприятными ощущениями и болями. При этом язык ярко-красного цвета, со сглаженными сосочками («лакированный язык», Гунтеровский глоссит), участками воспаления, трещинами и изъязвлениями. Может наблюдаться появление язвочек в углах рта и болей в деснах и губах.
Возможно снижение аппетита и, как следствие, потеря веса, ощущение тяжести в животе, диарея. Иногда незначительно увеличивается печень и селёзенка, что может быть выявлено при пальпации живота врачом либо при УЗИ органов брюшной полости.
Симптомы поражения нервной системы
Поражение нервной системы при B12ДА называется фуникулярным миелозом. Он затрагивает задние и боковые столбы спинного мозга, а также периферические нервы. Чаще встречается у мужчин. Это состояние проявляется онемением, парестезиями (ощущением ползанья мурашек), слабостью в ногах и нарушением походки. Реже наблюдаются подобные жалобы со стороны рук, при этом возникает трудность при выполнении точных движений.
Иногда нарушается слух, обоняние, зрение, возникают психические нарушения от раздражительности до тяжёлой деменции и психоза. Могут возникнуть такие неврологические проявления, как недержание мочи и непроизвольная дефекация. У детей раннего возраста симптомами поражения нервной системы могут быть мышечная слабость, дрожание, непроизвольные сокращения мышц. Возможна задержка психомоторного развития и потеря навыков [1] [2] [3] [4] [6] [7] .
Патогенез В12-дефицитной анемии
Витамин B12 поступает в организм с продуктами животного происхождения: мясные продукты, яйца, сыр, молоко. Из связи с белками пищи витамин высвобождается сначала под воздействием кулинарной обработки, а затем соляной кислоты и ферментов желудочного сока.
В двенадцатиперстной кишке витамин B12 соединяется с внутренним фактором Кастла, который синтезируется париетальными клетками желудка. Благодаря фактору Кастла витамин B12 поступает в клетки слизистой оболочки подвздошной кишки. После этого он связывается с транспортным белком транскобаламином II и переносится кровью клеткам-потребителям, в основном в печень и костный мозг.
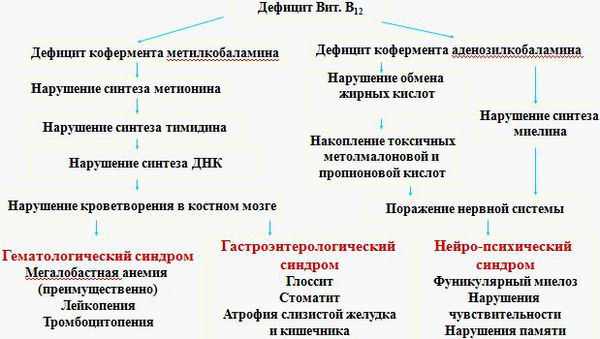
В клетке витамин B12 преобразуется в два кофермента: метилкобаламин и аденозилкобаламин . Коферменты — это соединения, необходимые для функционирования ферментов.
Метилкобаламин является коферментом для фермента метионинсинтазы, который преобразует одну аминокислоту — гомоцистеин в другую — метионин. При сбое этого процесса в организме накапливается гомоцистеин, не образуются пиримидиновые основания, необходимые для формирования ДНК. В результате нарушается синтез ДНК и процессы деления клеток. К этому изменению особенно чувствительны быстроделящиеся клетки — кроветворные клетки костного мозга, из которых образуются клетки крови, а также эпителиальные клетки желудочно-кишечного тракта. Отсюда появление таких изменений в анализе крови, как анемия, лейкопения (снижение количества лейкоцитов), тромбоцитопения (снижение количества тромбоцитов), а также атрофия слизистых оболочек.
Второй кофермент — аденозилкобаламин — принимает участие в обмене жирных кислот, который необходим для метаболизма миелина (вещества, образующего оболочку нервных волокон). Неправильный обмен жирных кислот вследствие недостатка витамина B12 приводит к накоплению токсичных для нервной системы кислот — метилмалоновой и пропионовой. Нарушается синтез миелина в задних и боковых столбах спинного мозга. Как следствие, появляется клиника поражения нервной системы [1] [2] [3] [4] [6] .
Классификация и стадии развития В12-дефицитной анемии
Классификация В12ДА по причинам развития:
- Наследственные (врождённые) формы. Описаны у детей с генетическими аномалиями, которые приводят к нарушению транспорта и метаболизма витамина B12.
- Приобретённые формы:
- первичная форма обусловлена аутоиммунной причиной дефицита витамина B12, то есть наличием антител к париетальным клеткам желудка или к фактору Кастла. Зачастую первичная форма B12ДА осложняет течение таких заболеваний, как аутоиммунный тиреоидит, витилиго или сахарный диабет 1 типа[6] .
- Вторичная форма возникает на фоне строгой веганской диеты [3][7][11] .
Стадии развития B12ДА:
- Начальная — латентный дефицит. Уровень витамина в сыворотке крови снижен, однако число эритроцитов и уровень гемоглобина остаются в норме. Клинических проявлений на данной стадии может не наблюдаться. Лабораторно возможно выявить изменение параметров эритроцитов: увеличение среднего объёма эритроцита (параметр MCV в анализе крови) и среднего содержания гемоглобина в эритроците (параметр MCH).
- Стадия клинических проявлений. Наблюдается при снижении уровня гемоглобина, когда появляются симптомы анемии, и при поражении нервной системы.
Степени тяжести В12ДА:
- Лёгкая — снижение уровня гемоглобина до 90 г/л.
- Средней тяжести — уровень гемоглобина в пределах 90-70 г/л.
- Тяжёлая — уровень гемоглобина ниже 70 г/л.
Осложнения В12-дефицитной анемии
Задержка роста и развития у детей возможна в результате снижения гемоглобина при B12ДА.
Сердечная недостаточность. У пожилых пациентов анемия может ухудшить течение сопутствующей сердечно-сосудистой патологии в виде развития сердечной недостаточности [14] .
Потеря массы тела может стать результатом снижения аппетита и проявлений со стороны желудочно-кишечного тракта.
Присоединение инфекционных осложнений возможно при развитии глубокой лейкопении (низкого уровня лейкоцитов). Снижение тромбоцитов, как правило, незначительное и не приводит к геморрагическим осложнениям.
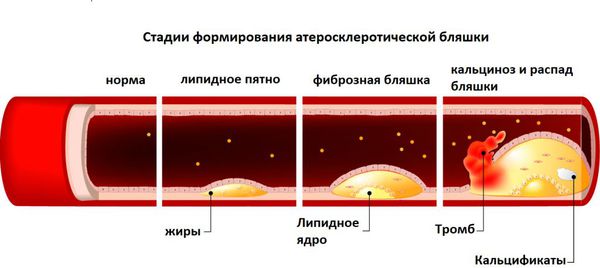
Атеросклероз, тромбоз. Повышение уровня гомоцистеина на фоне дефицита витамина B12 может вызвать атеросклероз и формирование тромбов. Накапливаясь в организме, гомоцистеин повреждает внутреннюю стенку артерий, что приводит к разрывам внутренней оболочки сосудов — эндотелия. В месте повреждения оседает холестерин и кальций — образуется атеросклеротическая бляшка, вследствие чего просвет сосуда сужается, а иногда закупоривается. Это грозит тромбозом или разрывом сосуда [15] [16] .
Также описано такое тяжёлое осложнение B12ДА, так тромботическая микроангиопатия — заболевание, в основе которого лежит поражение мелких сосудов и формирование в их просвете тромбов, что сопровождается воспалением сосудистой стенки. Как следствие, может развиваться ишемия органов и тканей.
Поражение головного и спинного мозга без лечения может привести к спастичности (чрезмерно высокому мышечному тонусу и непроизвольным движениям) и параплегии (полному параличу обеих рук или ног). С началом лечения B12ДА анемический синдром и неврологические проявления быстро купируются. Однако при выраженном дефиците витамина B12 поражение спинного мозга может быть необратимым [1] [6] [17] .
Диагностика В12-дефицитной анемии
Для правильной постановки диагноза B12ДА важен осмотр врача-гематолога. Для уточнения и коррекции проблем, связанных с работой желудочно-кишечного тракта, потребуется консультация гастроэнтеролога. Для оценки неврологических проявлений может быть необходим осмотр врача-невролога.
Осмотр пациента
При осмотре врач может обратить внимание на бледность и лёгкую желтушность кожи, увеличение частоты сердечных сокращений и расширение границ сердца. Необходимо провести осмотр полости рта, особенно языка. Невролог может оценить тонус мышц и наличие патологических рефлексов.
Лабораторная диагностика
Одним из самых важных этапов диагностики является оценка клинического анализа крови. В анализе наблюдается:
- снижение гемоглобина — анемия;
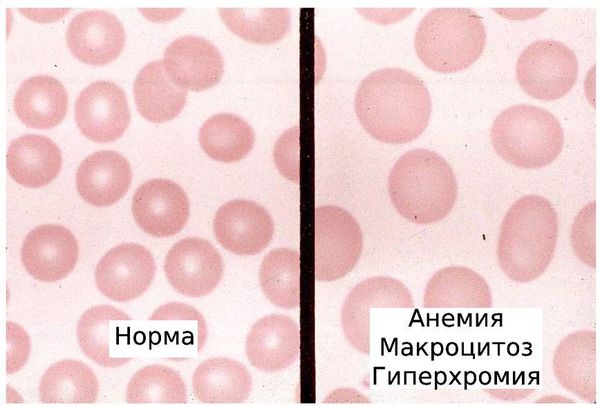
- макроцитоз — наличие в крови большого количества аномально крупных эритроцитов (макроцитов);
- гиперхромия — интенсивное окрашивание эритроцитов, вызванное повышенным количеством гемоглобина в крови;
- может наблюдаться снижение числа лейкоцитов и тромбоцитов.
Необходимо выполнение мазка крови , в котором врач-морфолог может увидеть патологические формы эритроцитов:
- овалоциты (эритроциты овальной формы) и дегенеративные формы;
- увеличение разницы эритроцитов по своему размеру (параметр RDW);
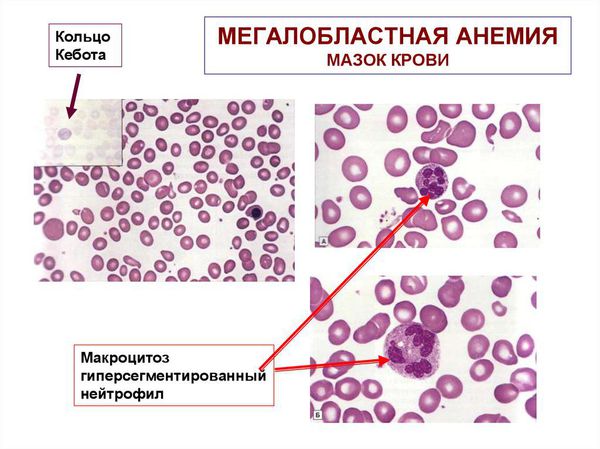
- специфические патологические включения, такие как тельца Жолли и кольца Кебота;
- мегалоциты и мегалобласты — в тяжёлых случаях.
Могут встречаться также патологические формы нейтрофилов:
- гигантские нейтрофилы;
- нейтрофилы с гиперсегментацией ядра (5 и более сегментов);
- метамиелоциты — незрелые нейтрофильные лейкоциты.
Количество молодых форм эритроцитов (ретикулоцитов), как правило, снижено. При наличии лабораторной возможности дополнительную полезную информацию могут предоставить ретикулоцитарные индексы: увеличивается средний объём ретикулоцитов и среднее содержание гемоглобина в ретикулоцитах, повышается фракция незрелых ретикулоцитов [1] [2] [4] [5] .
В биохимическом анализе крови:
- снижен уровень витамина B12;
- может быть повышен непрямой билирубин и лактатдегидрогеназа — признак раннего разрушения (гемолиза) эритроцитов в крови и распада предшественников эритроцитов в костном мозге [4] ;
- уровень железа и ферритина в норме.
Обязательно нужно оценить уровень фолиевой кислоты , поскольку изменения в клиническом анализе при дефиците B12 и фолиевой кислоты схожи, а лечение отличается. При подозрении на B12ДА, но при нормальном уровне витамина B12 и фолиевой кислоты, рекомендовано определение голотранскобаламина сыворотки (активного витамина B12). В случае дефицита B12 его содержание снижено. Может быть выявлено повышение уровня гомоцистеина и метилмалоновой кислоты в сыворотке крови [2] [3] .
В общем анализе мочи может наблюдаться стойкая протеинурия — появление белка в моче. В ряде случаев отмечается повышение уровня метилмалоновой кислоты и гомоцистеина.
Дополнительные лабораторные исследования, которые могут помочь выявить причину дефицита витамина B12:
- исследование антител к внутреннему фактору Кастла (IgG) и париетальным клеткам желудка в сыворотке крови;
- исследование желудочного сока на выявление внутреннего фактора Кастла и антител к этому фактору (IgA, синтезируются париетальными клетками желудка);
- тест Шиллинга — определяет активность внутреннего фактора Кастла и всасывание витамина B12 в кишечнике;
- тесты на мальабсорбцию (нарушение всасывания питательных веществ) [5] .
Возможна пренатальная диагностика генетически обусловленной недостаточности транспортного белка транскобаламина II, поскольку он синтезируется амниоцитами (клетками плодной оболочки).
Инструментальная диагностика
При ультразвуковом исследовании органов брюшной полости можно обнаружить незначительную гепатоспленомегалию — увеличение печени и селезёнки.
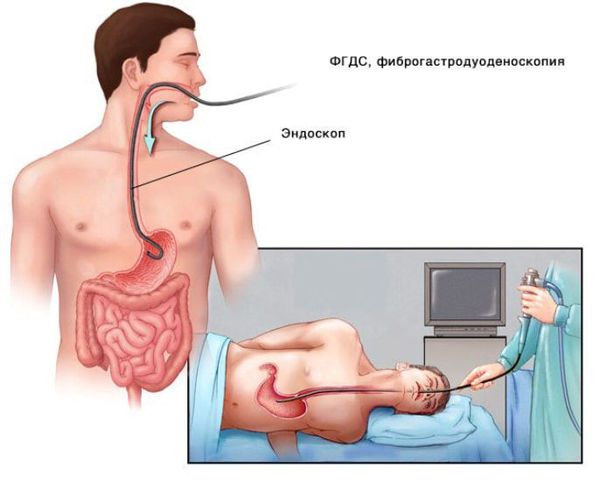
Для выявления заболеваний желудочно-кишечного тракта, которые могут нарушать всасывание витамина B12, всем пациентам с впервые выявленной B12ДА показано выполнение эндоскопических исследований — фиброгастродуоденоскопии (ФГДС) и колоноскопии. При ФГДС может быть выявлен хронический атрофический гастрит, дуоденит, может наблюдаться уменьшение желудочной секреции. При наличии патологических изменений обязательно выполнение биопсии слизистой желудка с дальнейшим гистологическим исследованием [3] [4] .
Дифференциальная диагностика
Дифференциальный диагноз при В12-дефицитной анемии, особенно со снижением лейкоцитов и тромбоцитов, проводится с такими заболеваниями системы крови:
- Миелодиспластический синдром — группа гематологических заболеваний, при которых костный мозг не производит достаточного количества одного или более типов клеток крови: тромбоцитов, лейкоцитов, эритроцитов.
- Апластическая анемия — это анемия, возникающая вследствие недостаточной продукции эритроцитов из-за уменьшения количества кроветворных стволовых клеток.
Для уточнения диагноза может потребоваться выполнение пункции костного мозга и его морфологическое исследование. При наличии B12ДА специалист морфолог описывает в костном мозге характерные изменения стволовых клеток-предшественников:
- гиперплазию (разрастание) эритроидного ростка — стволовых клеток-предшественников, из которых образуются эритроциты;
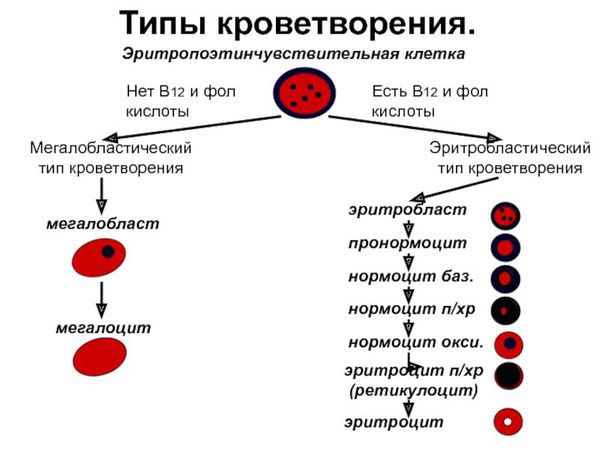
- мегалобластный тип кроветворения, при котором образуются крупные клетки с зернистыми ядрами, патологические митозы, тельца Жолли;
- нарушение созревания клеток миелоидного ряда и предшественников тромбоцитов: гигантские метамиелоциты, гиперсегментация нейтрофилов, многоядерные мегакариоциты [1][2][3][4] .
Лечение В12-дефицитной анемии
При анемии, которая связана с недостаточностью поступления витамина с пищей, лечение предполагает коррекцию диеты в комбинации с внутримышечным введением витамина B12. Диета с достаточным содержанием витамина B12 предполагает употребление продуктов животного происхождения. Овощи, фрукты, хлеб не содержат витамин B12.
При других причинах коррекция диеты будет неэффективна. Во всех случаях лечение подразумевает введение препарата витамина В12 по стандартным схемам. Дозы препарата могут отличаться в зависимости от возраста больного и от наличия неврологических симптомов.
Лечение обычно проводится в амбулаторных условиях. Показанием для госпитализации в стационар может послужить тяжёлая анемия (уровень гемоглобина менее 70 г/л) и пожилой возраст.
При подозрении на B12ДА без лабораторного её подтверждения категорически не рекомендуется начинать лечение витамином B12 либо поливитаминными комплексами, поскольку введение B12 приводит к быстрому исчезновению морфологических аномалий клеток, что в свою очередь затруднит постановку правильного диагноза. Ошибочное использование фолиевой кислоты при дефиците B12 может привести к усугублению неврологических симптомов. Поэтому очень важно начинать терапию только после лабораторного подтверждения диагноза.
Первый этап терапии — насыщение. Он длится 4-6 недель и предполагает внутримышечное введение препарата цианокобаламин в лечебной дозе. В некоторых случаях может быть эффективно использование сублингвальных форм витамина B12. Признаки улучшения состояния наблюдаются после первых 3-5 инъекций препарата.
Первым лабораторным признаком эффективности терапии является ретикулярный криз — повышение уровня ретикулоцитов в крови в 2-3 раза по сравнению с исходным на 4-7 день от начала терапии. Нормализация уровня гемоглобина достигается через 1-2 месяца, периферическая нейропатия купируется медленнее.
На фоне терапии цианокобаламином в связи с активным делением клеток-предшественников в костном мозге возможно присоединение дефицита фолиевой кислоты и железа, поэтому спустя 7-10 дней от начала терапии витамином B12 необходимо дополнительно назначить фолиевую кислоту, а при снижении уровня ферритина — препараты железа.
Второй этап — закрепляющая терапия: витамин B12 вводится в той же дозе, но кратность введения уменьшается.
Третий этап — поддерживающая терапия. Она проводится пожизненно. Переливание эритроцитарной взвеси показано при тяжёлой анемии с признаками гипоксии и недостаточности кровообращения. При развитии нейтропении (снижения количества нейтрофилов) и присоединении инфекционных осложнений может потребоваться проведение антибактериальной терапии [1] [3] [4] [6] .
Прогноз. Профилактика
Независимо от возраста больного, при ранней постановке диагноза, своевременном начале лечения и правильном наблюдении после выздоровления прогноз при B12ДА благоприятный. Ухудшению прогноза могут способствовать сопутствующие сердечно-сосудистые заболевания у пожилых больных, а также поражение нервной системы (фуникулярный миелоз).
Профилактика B12ДА сводится к коррекции рациона питания. При невозможности ликвидировать причину заболевания (например, при удалении части желудка или при недостаточности внутреннего фактора Кастла) профилактика сводится к регулярному пожизненному введению препарата витамина B12. Анализ крови необходимо контролировать 1 раз в 3-4 месяца. Больным с атрофическим гастритом рекомендовано ежегодное выполнение ФГДС, поскольку у них повышен риск новообразований желудка [3] [6] .
Источник