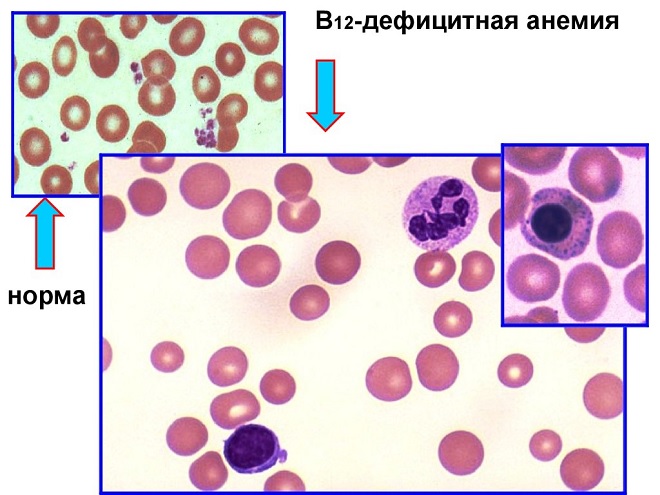
Витамин В12-дефицитная анемия
B12 анемия или, как её ещё называют пернициозная/мегалобластная – патологическое состояние, которое характеризуется нарушением процесса образования и созревания клеток крови вследствие дефицита в организма витамина B12. Последнее может быть связано с его недостаточным поступлением в человеческий организм или проблемах с усвоением. Чаще всего заболевание диагностируют у пациентов в возрасте от пятидесяти лет обоих полов. Согласно медицинским статистическим данным, его распространённость не превышает 1% в то время, как от недостатка B12 страдает не менее 10% пациентов в возрасте от семидесяти лет.
Пройти диагностику и лечение B12 дефицитной анемии в Москве предлагает отделение гематологии ЦЭЛТ. Наша многопрофильная клиника одна из первых на территории нашей страны начала предлагать платные медицинские услуги и успешно работает уже третье десятилетие. В её штате – ведущие российские специалисты, в арсенале которых имеются современные технологии и лечебно-диагностическая база. Она позволяет точно и оперативно ставить диагноз и проводить лечение по международным стандартам. Узнать стоимость услуг можно в нашем прайс-листе, уточняйте цифры у операторов нашей информационной линии: +7 (495) 788 33 88.
B12 анемия: причины
Ежедневная потребность человеческого организма в витамине В12 составляет от одного до пяти микрограммов. Она удовлетворяется за счёт его потребления с пищей: после попадания в желудок витамин отделяется от белка под воздействием ферментов. Для того, чтобы организм полноценно его усвоил, должен произойти процесс соединения с гликопротеином и другими факторами. Всасывание витамина в кровь происходит в нижней части подвздошной кишки, откуда он и поступает к тканям. Факторы, способные инициировать развитие анемии делят на две группы:
- Алиментарные – несбалансированное питание, не способное обеспечить поступление требуемого количества В12 в организм. Нередко такое случается, если пациент практикует голодание, вегетарианство или диеты, сводящие к минимуму или исключающие потребление животного белка;
- Эндогенные – сбои в процессе усвоения витамина из-за дефицита белка, связывающего витамин и переводящий его в усвояемую форму. Подобное явление может быть инициировано:
- врождённым отсутствием внутреннего фактора Касла;
- воспалительными процессами слизистой желудка в хронической форме;
- состоянием после проведения операции по иссечению желудка;
- состоянием после частичного удаления подвздошной или 12-типерстной кишки;
- воспалением тонкого кишечника (энтерит), поджелудочной железы (панкреатит);
- глютеновой энтеропатией;
- гранулёматозным воспалением отделов пищеварительного тракта (заболевание Крона);
- выпячиваниями кишечной стенки – (дивертикулами);
- новообразованиями тощей кишки злокачественной природы;
- глистными инвазиями, вызываемые разными видами гельминтов.
Причины могут крыться в физической и психической зависимости от приёма алкоголя, в применении «Колхицина», «Неомицина», а также ряда пероральных контрацептивов.
B12 анемия: симптомы
Клиническая картина мегалобластной анемии обусловлена выраженностью четырёх синдромов:
| Синдром | Клинические проявления |
| Анемический | Симптомы В12— дефицитной анемии являются неспецифическими, поскольку возникают вследствие сбоев транспортировки кислорода эритроцитами. Они заключаются в:
В долгосрочной перспективе анемия может перерасти во вторичное поражение миокарда и сердечную недостаточность. |
| Гастроэнтерологический | Одно из классических клинических проявлений – так называемый «лакированный» малиновый язык. Остальные – следующие:
Диагностика В12- дефицитной анемии выявляет атрофию слизистой оболочки желудка и снижение производства секрета. |
| Неврологический | Симптоматика этой группы обусловлена поражениями нейронов и проводящих путей, что проявляется:
Неврологический осмотр выявляет поражение периферических нервов и спинного мозга. |
Отсутствие адекватного лечения может стать причиной развития осложнения в виде анемии и дегенеративных процессов нервов вследствие повышенной чувствительности костного мозга и тканей нервной системы к недостатку в организме В12.
B12 анемия: диагностика
Перед тем, как приступить к лечению, гематологи ЦЭЛТ назначают пациенту всесторонние исследования, которые позволяют точно поставить диагноз «В12— дефицитная анемия» и выявить причины её развития. Помимо гематолога, в процессе принимают участие специалисты по неврологии и гастроэнтерологии. Диагностика заключается в следующем:
- Дефицит витамина выявляют посредством биохимического анализа;
- Общий анализ определяет дефицит эритроцитов, лейкоцитов и тромбоцитов;
- Анализ кала может обнаружить избыточное содержание жира, фрагменты гельминтов;
- Тест Шиллинга выявляет сбои при всасывании витамина;
- Гистология костного мозга и миелограмма определяют рост количества мегалобластов.
Для того чтобы выявить инициирующие факторы нарушения всасывания дефицитной анемии витамина В12 в желудочно-кишечном тракте, пациенту назначают гастроскопию и рентгенографию желудка, а также обследование толстого кишечника с применением рентгенконтрастного вещества. Получить необходимые сведения помогут и другие инструментальные методы:
B12 анемия: лечение
Тактика лечения В12-дефицитной анемии разрабатывается специалистами ЦЭЛТ согласно результатам диагностики и индивидуальным показаниям пациента. Если диагноз подтвердился, лечение будет проводиться пожизненно, а каждые пять лет потребуется эндоскопическое исследование слизистой желудка, исключающее риск развития его злокачественных новообразований.
Для того чтобы восполнить недостаток витамина, пациенту назначают его внутримышечное введение. Проводится лечение заболеваний и нарушений, которые инициировали развитие анемии:
- устранение гельминтов;
- приём пищеварительных ферментов;
- операции при дивертикулах и злокачественных опухолях;
- питание с повышенным содержанием животного белка;
- приём глюкокортикоидов при нарушениях производства внутреннего фактора.
Если начать лечение анемии своевременно, показатели крови придут в норму через полтора-два месяца. До полугода сохраняется неврологическая симптоматика, если лечение было начато на запущенной стадии, она необратима и вылечить её уже не удастся.
В отделении гематологии ЦЭЛТ ведут приём кандидаты, доктора и профессоры медицинских наук с опытом практической и научной работы от двадцати пяти лет. Записаться к ним на приём можно онлайн или обратившись к нашим операторам. Не менее опытные и квалифицированные специалисты проводят септопластику в отделении отоларингологии.
- Первичная консультация — 3 200
- Повторная консультация — 2 000
Записаться на прием
Записавшись на прием гематолога, вы сможете получить всестороннюю консультацию. В компетенции врача находится лечение различных заболеваний крови, большинство из которых можно выявить на ранних стадиях и назначить своевременное лечение, позволяющее справиться с болезнью быстро и легко.
Источник
ПЕРНИЦИОЗНАЯ АНЕМИЯ
ПЕРНИЦИОЗНАЯ АНЕМИЯ (anaemia perniciosa; лат. perniciosa гибельная, губительная; анемия; син.: злокачественная анемия, болезнь Аддисона — Бирмера, B12-дефицитная анемия, мегалобластная анемия) — тяжелая прогрессирующая анемия, возникающая при нарушении усвоения витамина B12, поступающего с пищей, вследствие пониженной (или при отсутствии) секреции внутреннего желудочного фактора.
Первое описание Пернициозной анемии под названием «тяжелое первичное малокровие» принадлежит Кумбу (J. S. Combe, 1822). Т. Аддисон в 1855 г. описал болезнь под названием «идиопатическая анемия», а А. Бирмер (см.) в 1872 г. — группу больных, страдавших «прогрессирующей пернициозной анемией».
Возможность излечения Пернициозной анемии путем назначения особой диеты (сырой печени) установлена Дж. Майнотом и У. Мерфи в 1926 г.; открытие в 1929 г. У. Каслом внутреннего желудочного фактора (см. Касла факторы) и в 1948 г. Смитом (E. L. Smith) и Риккесом (E. L. Rickes) «антипернициозного» витамина B12 — цианокобаламина (см.) способствовало выявлению патогенеза Пернициозной анемии и его успешному лечению.
Пернициозная анемия встречается гл. обр. у лиц старше 40 лет; чаще болеют мужчины. Известны редкие случаи заболевания детей на почве однообразного вскармливания козьим молоком или сухими молочными смесями. Заболеваемость П. а., по данным разных исследователей, составляет от 20 до 60 на 10 000 населения.
В классификации анемий (см.) выделяют B12— (фолиево) дефицитные анемии. В действительности комбинированный дефицит витамина B12 и фолиевой к-ты встречается редко, чаще наблюдается изолированный дефицит витамина B12 и реже — дефицит фолиевой к-ты.
Содержание
Этиология и патогенез
Ведущим фактором в этиологии П. а. является эндогенная недостаточность витамина B12, возникающая вследствие нарушения его всасывания в результате снижения или полного прекращения секреции внутреннего желудочного фактора (гастромукопротеина), необходимого для связывания и последующей абсорбции витамина B12. П. а. может возникнуть в результате поражения жел.-киш. тракта, напр, воспалительным или злокачественным процессом, а также после субтотального или тотального удаления желудка и после обширной резекции части тонкого кишечника. В редких случаях П. а. развивается при нормальной секреции внутреннего желудочного фактора и обусловлена врожденным отсутствием транскобаламина II (белка плазмы крови), с которым витамин B12 связывается и доставляется в печень и красный костный мозг, или отсутствием в кишечнике белкового акцептора витамина B12, необходимого для поступления витамина B12 из кишечника в кровеносное русло. На роль генетического фактора указывают случаи семейных заболеваний, а также возникновение П. а. на почве врожденного нарушения секреции внутреннего желудочного фактора, наследуемого по аутосомно-рецессивному типу. Об участии иммунных механизмов при П. а. свидетельствует наличие в сыворотке крови у большинства больных П. а. и их родственников антител, направленных против париетальных гландулоцитов желудка, а также антител (IgG) против внутреннего желудочного фактора, к-рые определяются как в париетальных гландулоцитах (при гастробиопсии), так и в цитоплазме плазматических клеток красного костного мозга авторадиографией (см.). О существовании аутоиммунных процессов говорят случаи сочетания П. а. с тиреоидитом Хасимото (см. Хасимото болезнь), при этом одновременно присутствуют антитиреоидные антитела и антитела к париетальным гландулоцитам желудка. Аутоиммунный генез П. а. подтверждает успешное применение кортикостероидов. В ряде случаев П. а. возникает без участия специфических антител.
Нарушение кроветворения (см.) характеризуется мегалобластозом красного костного мозга с поражением всех трех ростков кроветворения — эритроидного, гранулоцитарного и мегакариоцитарного. Особенностью мегалобластического эритроцитопоэза является его неэффективность, обусловленная резким нарушением процессов дифференциации эритроидных клеток, в результате которого в красном костном мозге происходит накопление аномальных эритроидных клеток — промегалобластов и мегалобластов. Мегалобластический эритроцитопоэз обусловлен резким снижением активности В ^-зависимых энзимов, участвующих в метаболизме фолатов (солей фолиевой к-ты), необходимых для синтеза ДНК; в частности, снижение активности метилтрансферазы сопровождается кумуляцией в клетках неактивного метилтетрагидрофолата и снижением синтеза ДНК, что приводит к нарушению клеточного деления и развитию мегалобластоза.
Повышенная «интрамедуллярная смертность» мегалобластов, выявляемая при биопсии костного мозга в виде интенсивного эритрофагоцитоза и гемосидероза (см.), ведет к резкому снижению продукции эритроцитов, т. е. к анемии. В то же время в результате повышенного распада гемоглобинизированных мегалобластов (полихроматофильных и оксифильных) возникают симптомы гемолитической анемии (см.) — не-конъюгированная гипербилирубинемия, плейохромия (увеличенное содержание пигментов) желчи, уробилинурия, повышенное выделение стеркобилина с калом. Не исключена возможность участия антител в костномозговом разрушении эрит-рокариоцитов.
Патологическая анатомия
Смертельные случаи в связи с успешным лечением П. а. встречаются крайне редко. При вскрытии умерших в остром периоде болезни выявляется общее малокровие, желтушность кожи, серозных и слизистых оболочек, жировая дистрофия миокарда, печени, почек. Кровь в сердце и крупных сосудах жидкая, водянистая. Вследствие выраженной гиперплазии кроветворных элементов и исчезновения жира костный мозг плоских костей, а также диафизов и эпифизов трубчатых костей очень сочный, малиново-красного цвета. Характерны атрофические изменения в жел.-киш. тракте.
Сосочки языка, особенно в области корня, атрофичны, сглажены. Слизистая оболочка языка содержит красноватые участки воспаления, располагающиеся чаще по краям и на кончике, иногда афтозные высыпания, трещины (картина так наз. гунтеровского глоссита). Сходные изменения могут наблюдаться в слизистой оболочке десен, щек, мягкого неба, глотки, пищевода. Постоянно выявляется атрофия слизистой оболочки желудка, наиболее выраженная в области дна; складки слизистой оболочки сглажены или не определяются, стенка желудка истончена, в некоторых случаях имеются полипозные разрастания. Атрофические изменения могут наблюдаться также в слизистой оболочке кишечника. Размеры селезенки — в пределах или несколько больше нормы. Печень увеличена незначительно, плотновата. Вследствие отложения гемосидерина ткань селезенки, печени, иногда почек на разрезе имеет ржавый оттенок. Лимф, узлы небольшие, мягкие. В некоторых: случаях макроскопически в спинном мозге выявляются мелкие очаги некроза с размягчением. Иногда находят мелкоточечные кровоизлияния в. серозных и слизистых оболочках, в коже.
Микроскопически в красном костном мозге отмечается выраженная гиперплазия клеток эритроидного ряда с наличием среди них большого количества мегалобластов — крупных клеток, имеющих нежноячеистую структуру ядра с отчетливо видимыми ядрышками и широкую зону базофильной или полихроматофильной цитоплазмы. Число клеток лейкоцитопоэза несколько снижено. Мегакариоциты содержатся в достаточном или уменьшенном количестве. Наблюдаются выраженные дистрофические изменения и распад клеток, особенно эритроидного ряда, обилие эритро-и сидерофагов. В слизистой оболочке желудка выявляется картина атрофического гастрита, имеется значительное уменьшение количества желез и железистых клеток, особенно обкладочных. Клетки уменьшены в размерах, пикнотичны, уплощены, вследствие чего просвет желез расширен. Возрастает количество слизеобразующих железистых клеток, встречаются участки кишечной метаплазии поверхностного эпителия. Строма слизистой оболочки склерозирована, инфильтрирована лимфоцитами, плазматическими клетками, единичными сегментоядерными нейтрофильными гранулоцитами (рис.). Изменения наиболее выражены в дне желудка, однако интенсивность их может варьировать в различных участках слизистой оболочки. Атрофические изменения не подвергаются обратному развитию при лечении витамином B12 и сохраняются в период ремиссии заболевания.
При биопсии слизистой оболочки тонкой кишки выявляются укорочение кишечных ворсинок, дистрофические изменения железистых клеток со снижением в них фигур митозов в криптах, лимфоидно-плазмоцитарная инфильтрация стромы. После лечения витамином B12 эти изменения могут исчезнуть. Наряду с атрофическими изменениями наблюдается дистрофия нервных волокон языка, нервных клеток подслизистого сплетения (plexus submucosus, s. Meissneri) и мышечно-кишечного сплетения (plexus myen-tericus, s. Auerbachi).
Характерны дистрофические изменения в задних и боковых столбах спинного мозга, преимущественно в шейном отделе, выражающиеся в очаговом набухании с последующим распадом миелиновых нервных волокон. Слияние мелких очагов приводит к образованию больших участков поражения. В некоторых случаях наблюдаются дистрофические изменения черепно-мозговых (черепных, Т.) и периферических нервов. Имеет место гемосидероз костного мозга, селезенки, печени, лимф, узлов, почек, выраженный в различной степени. В селезенке, лимфатических узлах нередко встречаются очаги экстрамедуллярного кроветворения.
Клиническая картина
Клиническая картина проявляется симптомами поражения жел.-киш. тракта, нервной системы и кроветворной ткани. Постепенно появляются слабость, утомляемость, сердцебиение, одышка при физической нагрузке. Многие из больных в течение ряда лет жалуются на диспептические расстройства, возникшие в результате желудочной ахилии, которая может быть обнаружена за несколько лет до развития малокровия, при этом желудочный сок не содержит внутреннего желудочного фактора. В 1 — 2% случаев П. а. начинается с явлений стенокардии.
Как правило, заболевание протекает с обострениями, за которыми следуют ремиссии. Внешний вид больного при обострении процесса характеризуется бледностью с лимонно-желтым оттенком кожи и субиктеричностыо склер. Больные склонны к ожирению. Печень, как правило, увеличена, мягкая. Иногда пальпируется плотная селезенка. Температура изредка субфебрильная. Выслушиваются функциональные (анемические) сердечные шумы; на ЭКГ — снижение зубца T во всех отведениях, уширение желудочного комплекса.
У некоторых больных обнаруживается гунтеровский глоссит: вначале преобладают воспалительные явления («ошпаренный» язык), в дальнейшем — атрофические («лакированный» язык). Воспалительно-атрофические изменения могут распространиться на десны, слизистую оболочку щек, мягкого неба, глотки и пищевода; в последнем случае возникает дисфагия (синдром Плахммера — Винсона). Эти явления, кроме ахилии, исчезают в период ремиссии. При гастроскопии (см.) выявляется гнездная, реже тотальная атрофия слизистой оболочки желудка.
Поражение ц. н. с. клинически проявляется симптомами спинального паралича (спастический парапарез с повышенными рефлексами и клонусами) и табетическими симптомами (парестезии, опоясывающие боли, снижение рефлексов вплоть до полной арефлексии, нарушение вибрационной и глубокой чувствительности, сенсорная атаксия, расстройство функций тазовых органов). Реже наблюдаются поражения черепно-мозговых нервов, гл. обр. зрительного, слухового, обонятельного. Типична центральная скотома (см.) с потерей зрения, быстро восстанавливающегося под влиянием лечения витамином B12.
При обострении П. а. в крови отмечается Гиперхромная анемия; для нее характерно уменьшение количества эритроцитов, к-рые отличаются насыщенностью гемоглобином, достигают в диам. 12—15 мкм; цветной показатель равен 1,4—1,8. Встречаются эритроциты с остатками ядер (тельца Жолли), митотического веретена (кольца Кебота), с базофильной пунктацией, поли-хроматофилы, пойкилоциты, шизоциты, а также ядерные формы эритроидных клеток — мегалобласты. Количество лейкоцитов уменьшено за счет гранулоцитопении; обнаруживаются миело- и метамиелоциты, гигантские палочко- и сегментоядерные нейтрофилы, содержащие до 12 и более сегментов. Обмечается тромбоцитопения, встречаются гигантские пластинки (мегатромбоциты). Содержание витамина B12 в крови снижено при нормальном или повышенном уровне фолатов в эритроидных клетках (так наз. метилтетрагидрофо-латный блок) и при повышенном содержании сывороточного железа. В период ремиссии картина крови постепенно нормализуется.
В случаях легкого течения П. а. у 80—90% больных, по данным М. П. Невского, наблюдаются астенические нарушения (см. Астенический синдром).
У одних больных преобладают эмоционально-гиперестетическая слабость, утомляемость, рассеянность, неустойчивость внимания, чувство разбитости, подавленно-слезливое настроение, гиперестезия; у других — раздражительность, недовольство, легкая возбудимость, повышенная требовательность. Ипохондрические высказывания у больных с П. а. (см. Ипохондрический синдром) часто связаны с реальными соматическими расстройствами. В случаях ирогредиентно текущей П. а., особенно сопровождаемой симптомами фуникулярного миелоза (см.), возникают острые и затяжные психозы, частота которых, по данным ряда исследователей, колеблется от 4 до 10%. Психозы чаще встречаются у женщин в возрасте от 40 до 60 лет. Начальные расстройства определяются астенией, продолжительность которой в случаях острого течения составляет недели, а в затяжных — месяцы. В последующем при остром течении чаще всего развивается делирий (см. Делириозный синдром), реже — сумеречное помрачение сознания (см.) или аменция (см. Аментивный синдром). Утяжеление психических нарушений приводит к развитию сопора и комы (см.).
При психозах с затяжным течением вслед за астенией возникают аффективные расстройства, чаще всего в форме депрессии (см. Депрессивные синдромы). Преобладают тревожно-ажитированные состояния с отрывочным бредом преследования и обвинения, вербальными иллюзиями (см.) и галлюцинациями (см.). В ряде случаев возникает депрессия со страхом. Реже встречаются маниакальные состояния с эйфорией и сниженной критикой (см. Маниакальные синдромы). При утяжелении клин, картины развивается галлюцинаторно-параноидное состояние (см. Параноидный синдром), при к-ром могут возникать выраженные тактильные галлюцинации. Особенность психических расстройств при П. а. заключается в изменчивости их интенсивности и смене одних расстройств другими на протяжении коротких отрезков времени. В тех случаях, когда такое «мерцание» психических расстройств отсутствует, затянувшийся психоз исчерпывается одним каким-либо состоянием, напоминая шизофрению (см.) или маниакально-депрессивный психоз (см.). На отдаленных этапах затяжных психозов могут возникать делириозные состояния. В ряде случаев их появление — признак возможного смертельного исхода, связанного с основным заболеванием. Психозы в случаях легкого течения П. а. могут смениться преходящими симптомами снижения уровня личности, а в случаях тяжелого течения наблюдается возникновение различного по тяжести и проявлениям психоорганического синдрома (см.).
Тяжелым осложнением П. а. является Пернициозная кома (coma perniciosum), возникающая вследствие быстрой анемизации, приводящей к гипоксии и ишемии головного мозга (в частности, области III желудочка). При этом наблюдается потеря сознания, арефлексия, падение температуры тела и АД, одышка, рвота, непроизвольное мочеиспускание.
Диагноз
Диагноз устанавливают на основании клин, данных, характерной картины крови и результатов исследования костномозгового пунктата.
Дифференциальный диагноз П. а. с другими мегалобластными, в частности фолиево-дефицитными, анемиями проводят на основе теста Шиллинга, заключающегося в том, что у больного П. а. введенный внутрь радиоактивный витамин B12 и одновременно парентерально не радиоактивный витамин B12 (1000 мкг) определяются в моче лишь в минимальных количествах, что указывает на нарушенную абсорбцию витамина B12, которая связана либо с нарушением секреции внутреннего желудочного фактора, либо с нарушением кишечного всасывания витамина B12; в последнем случае прием концентрата внутреннего желудочного фактора не улучшает абсорбцию витамина B12. П. а. дифференцируют с симптоматическими мегалобластными (пернициозноподобными) анемиями, возникающими при опухолях желудка, дивертикулах и опухолях тонкой и слепой кишок, а также с агастральной, анентеральной и глистной B12-дефицитной анемиями (см. Анемия), при которых мегалобластная анемия развивается в результате нарушения секреции внутреннего желудочного фактора или абсорбции витамина B12 в кишечнике. П. а. дифференцируют также с системными заболеваниями, напр, эритромиелозом (см. Лейкозы), для которого характерны мегалобластоз костного мозга при повышенном содержании витамина B12 в крови (до 1000 нг/мл и выше) и отсутствие терапевтического эффекта от введения витамина B12 (так наз. B12-ахрестическая анемия).
Лечение
При обострении ежедневно вводят витамин B12 (по 100—200 мкг) в течение 1-й недели до ретикулоцитарного криза, который обычно наступает на 5-й день от начала введения витамина B12 и характеризуется увеличенным содержанием ретикулоцитов. В дальнейшем те же дозы вводят через день в течение 4—5 недель до наступления гематол, ремиссии, которая определяется нормализацией периферической крови и костномозгового кроветворения и восстановлением нормального содержания витамина B12 в крови, причем нормализация крови начинается вслед за ретикулоцитарным кризом и завершается через 4—6 недель; нормализация костномозгового кроветворения (трансформация мегалобластиче-ского эритроцитопоэза в нормобласти-ческий) начинается немедленно после введения витамина B12 и завершается через 48—72 часа; содержание витамина B12 в крови восстанавливается постепенно. В период ремиссии исчезают клин, симптомы, включая неврологические. При фуникулярном миелозе вводят массивные дозы витамина B12 (500—1000 мкг) ежедневно в течение 7—10 дней, в дальнейшем два раза в неделю до исчезновения неврологических симптомов.
При психозах в зависимости от клин, картины применяют психотропные средства. При быстро прогрессирующей тяжелой пернициозной анемии (угрожающая Пернициозная кома) показано переливание эритроцитной массы (см. Переливание крови).
Прогноз и Профилактика
Прогноз при своевременно начатом лечении благоприятный.
Профилактика. Для предупреждения обострений П. а. производят инъекции витамина B12 по 50—100 мкг еженедельно в течение 1 года и в дальнейшем 1 раз в 2 недели в течение всей жизни.
Боткин С. П. О пернициозной анемии, Еженед. клин, газ., Мб, с. 81, 1884; он же, Курс клиники внутренних болезней и клинические лекции, т. 2, с. 80, М., 1950; Гольдберг А. И. Агастрические B12-дефицитные анемии, Томск, 1962, библиогр.; Давыдовокий И. В. Патологическая анатомия и патогенез болезней человека, т. 2, М., 1958; Кассирский И. А. и Алексеев Г. А. Клиническая гематология, с. 174, М., 1970; Люмот Г. Н. К вопросу психозов при пернициозной анемии, в кн.: Вопр, клиники, патогенеза и тер. психич. заболев., под ред. В. М. Банщикова и И. А. Шишкина, с. 437, М., 1972; Невский М. П. К вопросу о психозах при пернициозной анемии, Труды психиат, клиники им. G. С. Корсакова, в. 8, с.391, М., 1945; Салу пере В. Проблема хронического гастрита, Таллин, 1978; Димитров Д. Я. Анемии на бременните, София, 1974; Addison Th. Anaemia, disease of the supra-renal capsules, Lond. med. Gaz., v. 43, p. 517, 1849; Besangon F. L’an6mie pernicieuse, P., 1955; Biermer A. Form von prog-ressiver pernicioser AnSmie, KorrespBl. schweiz. Arz., Bd 2, S. 15, 1872; Gastle W. B. a. Townsend W. G. Observations on the etiologic relationship of ac-hylia gastrica to pernicious anemia, Amer. J. med. Sci., v. 178, p. 764, 1929; Gombe J. S. History of a case of anaemia, Trans, med.-chir. Soc. Edinb., v. 1, p. 194, 1824; Foroozan P. a. Trier J. S. Mucosa of the small intestine in pernicious anemia, New Engl. J. Med., v. 277, p. 553, 1967; Kass L. Pernicious anemia, Philadelphia a. o., 1976, bibliogr.; Minot G. R. a. Murphy W. P. Treatment of pernicious anemia by a special diet, J. Amer, med. Ass., v. 87, p. 470, 1926; Porot A. Manuel alphab6tique de psychiatrie, p. 275, P., 1969; Riсkes E. L. a. o. Crystalline vitamin Bt2, Science, v. 107, p. 396, 1948; Schneider С. Uber Geistesstorungen bei pernizioser Anamie, Nervenarzt, S. 286, 1929; Shulman R. Psychiatric aspects of pernicious anaemia, Brit. med. J., v. 3, p. 266, 1967; Smith E. L.Purification of anti-pernicious anaemia factors from liver, Nature (Lond.), v. 161, p. 638, 1948; Taylor K. B. Inhibition of intrinsic factor by pernicious anaemia sera, Lancet, v. 2, p.gl06, 1959; Taylor R. T., Hanna M. L. a. Hullo n J. J. 5-methyltetrahydrofolate homocysteine cobalamin methyltransferase in human bone marrow and its relationship to pernicious anemia, Arch. Biochem., v. 165, p. 787, 1974; Williams W. J. Hematology, p. 266. N. Y., 1977.
Г. А. Алексеев; М. П. Хохлова (пат. ан.), H. Г. Шуме кий (псих.).
Источник