Связь между витаминами ферментами
Витамины — группы разнородных по химической природе веществ, не синтезируемых или синтезируемых в недостаточных количествах в организме, но необходимых для нормального осуществления обмена веществ, роста, развития организма и поддержания здоровья. Эти вещества не являются непосредственными источниками энергии и не выполняют пластических функций. Они являются составными компонентами ферментных систем и играют роль катализаторов в обменных процессах.
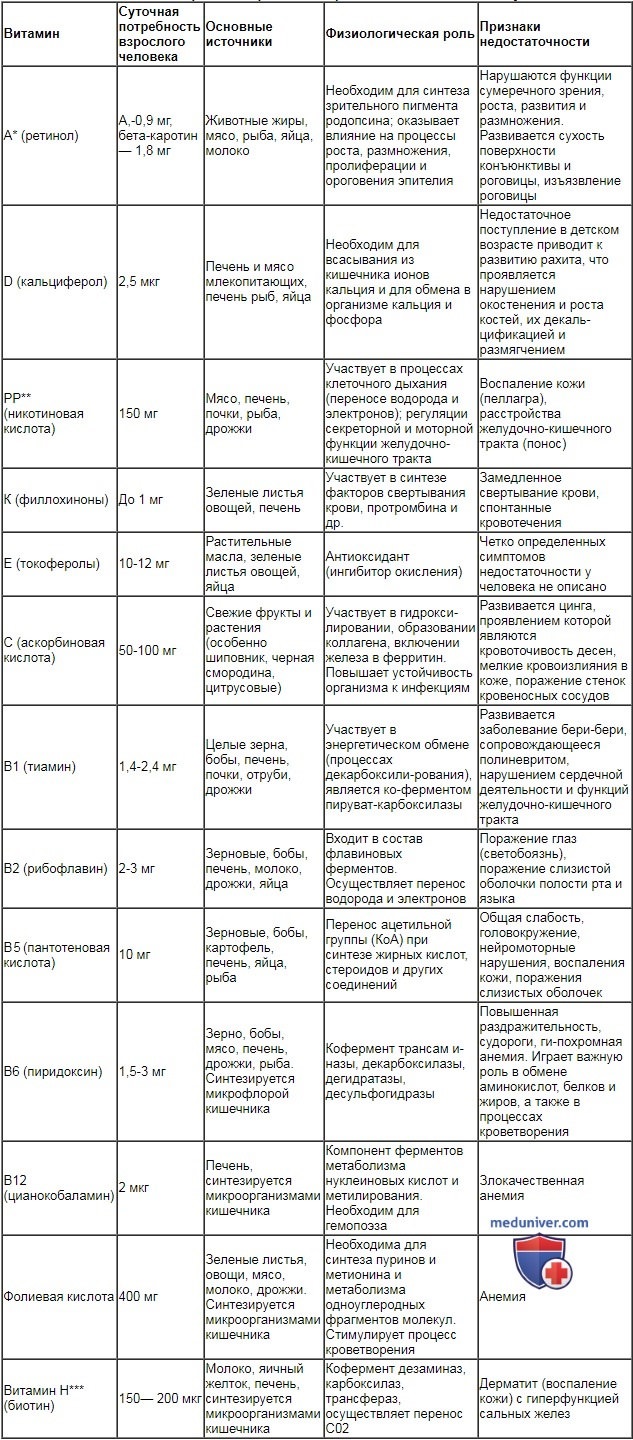
Сведения об источниках витаминов, их суточной потребности для взрослого человека и значении в осуществлении физиологических функций приведены в табл. 12.2.
Таблица 12.2. Физиологическая роль, потребность организма и источник поступления витаминов
| Витамин | Суточная потребность взрослого человека | Основные источники | Физиологическая роль | Признаки недостаточности |
| А* (ретинол) | А,-0,9 мг, бета-каротин — 1,8 мг | Животные жиры, мясо, рыба, яйца, молоко | Необходим для синтеза зрительного пигмента родопсина; оказывает влияние на процессы роста, размножения, пролиферации и ороговения эпителия | Нарушаются функции сумеречного зрения, роста, развития и размножения. Развивается сухость поверхности конъюнктивы и роговицы, изъязвление роговицы |
| D (кальциферол) | 2,5 мкг | Печень и мясо млекопитающих, печень рыб, яйца | Необходим для всасывания из кишечника ионов кальция и для обмена в организме кальция и фосфора | Недостаточное поступление в детском возрасте приводит к развитию рахита, что проявляется нарушением окостенения и роста костей, их декаль-цификацией и размягчением |
| РР** (никотиновая кислота) | 150 мг | Мясо, печень, почки, рыба, дрожжи | Участвует в процессах клеточного дыхания (переносе водорода и электронов); регуляции секреторной и моторной функции желудочно-кишечного тракта | Воспаление кожи (пеллагра), расстройства желудочно-кишечного тракта (понос) |
| К (филлохиноны) | До 1 мг | Зеленые листья овощей, печень | Участвует в синтезе факторов свертывания крови, протромбина и др. | Замедленное свертывание крови, спонтанные кровотечения |
| Е (токоферолы) | 10-12 мг | Растительные масла, зеленые листья овощей, яйца | Антиоксидант (ингибитор окисления) | Четко определенных симптомов недостаточности у человека не описано |
| С (аскорбиновая кислота) | 50-100 мг | Свежие фрукты и растения (особенно шиповник, черная смородина, цитрусовые) | Участвует в гидрокси-лировании, образовании коллагена, включении железа в ферритин. Повышает устойчивость организма к инфекциям | Развивается цинга, проявлением которой являются кровоточивость десен, мелкие кровоизлияния в коже, поражение стенок кровеносных сосудов |
| В1 (тиамин) | 1,4-2,4 мг | Целые зерна, бобы, печень, почки, отруби, дрожжи | Участвует в энергетическом обмене (процессах декарбоксили-рования), является ко-ферментом пируват-карбоксилазы | Развивается заболевание бери-бери, сопровождающееся полиневритом, нарушением сердечной деятельности и функций желудочно-кишечного тракта |
| В2 (рибофлавин) | 2-3 мг | Зерновые, бобы, печень, молоко, дрожжи, яйца | Входит в состав флавиновых ферментов. Осуществляет перенос водорода и электронов | Поражение глаз (светобоязнь), поражение слизистой оболочки полости рта и языка |
| В3 (пантотеновая кислота) | 10 мг | Зерновые, бобы, картофель, печень, яйца, рыба | Перенос ацетильной группы (КоА) при синтезе жирных кислот, стероидов и других соединений | Общая слабость, головокружение, нейромоторные нарушения, воспаления кожи, поражения слизистых оболочек |
| В6 (пиридоксин) | 1,5-3 мг | Зерно, бобы, мясо, печень, дрожжи, рыба. Синтезируется микрофлорой кишечника | Кофермент трансам и-назы, декарбоксилазы, дегидратазы, десульфогидразы | Повышенная раздражительность, судороги, ги-похромная анемия. Играет важную роль в обмене аминокислот, белков и жиров, а также в процессах кроветворения |
| В12 (цианокобаламин) | 2 мкг | Печень, синтезируется микроорганизмами кишечника | Компонент ферментов метаболизма нуклеиновых кислот и метилирования. Необходим для гемопоэза | Злокачественная анемия |
| Фолиевая кислота | 400 мг | Зеленые листья, овощи, мясо, молоко, дрожжи. Синтезируется микроорганизмами кишечника | Необходима для синтеза пуринов и метионина и метаболизма одноуглеродных фрагментов молекул. Стимулирует процесс кроветворения | Анемия |
| Витамин H***(биотин) | 150— 200 мкг | Молоко, яичный желток, печень, синтезируется микроорганизмами кишечника | Кофермент дезаминаз, карбоксилаз, трансфераз, осуществляет перенос С02 | Дерматит (воспаление кожи) с гиперфункцией сальных желез |
*Проявления передозировок витамина: головные боли, эйфория, анемия, изменения со стороны кожи, слизистых оболочек, костной ткани.
** Проявление передозировки витамина: нарушение функций ЦНС и почек; вымывание Са 2+ из костей и повышение его уровня в крови.
***Гиповитаминоз может развиваться при потреблении больших количеств сырого яичного белка, связывающего биотин.
Основными источниками водорастворимых витаминов (группы В, витамин С) являются, как правило, пищевые продукты растительного происхождения и в меньшей мере животного происхождения. Эти витамины легко всасываются из желудочно-кишечного тракта в кровь и лимфу.
Основными источниками жирорастворимых витаминов (витамины A, D, Е, К) являются продукты животного происхождения. Для удовлетворения потребностей организма в витаминах имеет значение не только достаточное содержание в пищевом рационе богатых витаминами продуктов растительного и животного происхождения, но и нормальное осуществление процессов пищеварения и всасывания веществ в желудочно-кишечном тракте. Так, при нарушениях пищеварения в тонком кишечнике, связанных с недостаточным поступлением в двенадцатиперстную кишку желчи или панкреатической липазы, может наблюдаться недостаточное всасывание из желудочно-кишечного тракта витаминов при их нормальном содержании в пище.
Дополнительным источником витаминов К, В6, и В12 является микрофлора толстой кишки. Микроорганизмы синтезируют эти витамины (наряду с другими веществами), которые частично усваиваются организмом.
Длительное голодание, питание пищевыми продуктами, не содержащими или содержащими малое количество витаминов, употребление в пищу продуктов после их длительного хранения или неправильной переработки, нарушение пищеварительных функций могут приводить к недостаточному поступлению витаминов в организм (гиповитаминозу).
Гиповитаминоз или полное прекращение поступления витамина в организм (авитаминоз) приводят как к неспецифическим изменениям функций (снижению умственной и физической работоспособности), так и к специфическим нарушениям в организме, характерным для гипо- и авитаминоза (см. табл. 12.2). Избыточный прием витаминов может приводить к гипервитаминозу. При поступлении водорастворимых витаминов в дозах, превышающих суточную потребность, эти вещества могут быстро выводиться из организма с мочой. При этом обычно признаков гипервитаминоза не отмечается. Однако, например, потребление больших количеств витамина В6 может сопровождаться нарушением функции периферических нервов. Изменения в организме, возникающие при гипервитаминозах A, D, РР, приведены в табл. 12.2.
Источник
О роли витаминов
Витамины – жизненно важные вещества, необходимые нашему организму для поддержания многих его функций. Поэтому достаточное и постоянное поступление витаминов в организм с пищей крайне важно.
Биологическое действие витаминов в организме человека заключается в активном участии этих веществ в обменных процессах. В обмене белков, жиров и углеводов витамины принимают участие либо непосредственно, либо входя в состав сложных ферментных систем. Витамины участвуют в окислительных процессах, в результате которых из углеводов и жиров образуются многочисленные вещества, используемые организмом, как энергетический и пластический материал. Витамины способствуют нормальному росту клеток и развитию всего организма. Важную роль играют витамины в поддержании иммунных реакций организма, обеспечивающих его устойчивость к неблагоприятным факторам окружающей среды. Это имеет существенное значение в профилактике инфекционных заболеваний.
Витамины смягчают или устраняют неблагоприятное действие на организм человека многих лекарственных препаратов. Недостаток витаминов сказывается на состоянии отдельных органов и тканей, а также на важнейших функциях: рост, продолжение рода, интеллектуальные и физические возможности, защитные функции организма. Длительный недостаток витаминов ведет сначала к снижению трудоспособности, затем к ухудшению здоровья, а в самых крайних, тяжелых случаях это может закончиться смертью.
Только в некоторых случаях наш организм может синтезировать в небольших количествах отдельные витамины. Так, например, аминокислота триптофан может преобразовываться в организме в никотиновую кислоту. Витамины необходимы для синтеза гормонов – особых биологически активных веществ, которые регулируют самые разные функции организма.
Значит, получается, что витамины – это вещества, относящиеся к незаменимым факторам питания человека, и имеют огромное значение для жизнедеятельности организма. Они необходимы для гормональной системы и ферментной системы нашего организма. Также регулируют наш обмен веществ, делая организм человека здоровым, бодрым и красивым.
Основное их количество поступает в организм с пищей, и только некоторые синтезируются в кишечнике обитающими в нём полезными микроорганизмами, однако в этом случае их бывает не всегда достаточно. Многие витамины быстро разрушаются и не накапливаются в организме в нужных количествах, поэтому человек нуждается в постоянном поступлении их с пищей.
Первоисточником витаминов являются растения, в которых витамины накапливаются. В организм витамины поступают в основном с пищей. Некоторые из них синтезируются в кишечнике под влиянием жизнедеятельности микроорганизмов, но образующиеся количества витаминов не всегда полностью удовлетворяют потребности организма. Витамины участвуют в регуляции обмена веществ; они являются биологическими катализаторами или реагентами фотохимических процессов, протекающих в организме, также они активно участвуют в образовании ферментов.
Витамины влияют на усвоение питательных веществ, способствуют нормальному росту клеток и развитию всего организма. Являясь составной частью ферментов, витамины определяют их нормальную функцию и активность. Недостаток, а тем более отсутствие в организме какого-либо витамина ведет к нарушению обмена веществ. При недостатке их в пище снижается работоспособность человека, сопротивляемость организма к заболеваниям, к действию неблагоприятных факторов окружающей среды. В результате дефицита или отсутствия витаминов, развивается витаминная недостаточность.
Важность отдельных витаминов для человека
Витамин А содержится в животных продуктах. Богаты этим витамином печень, сливочное масло, яйца и особенно рыбий жир. Растительные продукты содержат каротин — особое вещество, которое в организме человека превращается в витамин А. Много каротина в моркови. При отсутствии в пище витамина А замедляется рост и развивается заболевание глаз (куриная слепота). Витамин А повышает устойчивость организма к инфекционным заболеваниям. Этот витамин хорошо растворяется в жирах. При действии кислорода воздуха витамин А разрушается. Витамин А особенно важен в питании детей первого года жизни.
Витамин B1 содержится в оболочках зерновых хлебов, овощах, плодах, молоке, дрожжах, почках и печени животных. Особенно богаты витамином B1 рисовые отруби и пшеница. Недостаток этого витамина в пище вызывает расстройство нервной системы, падение аппетита, быструю утомляемость. Витамин B1 устойчив к воздействию высокой температуры.
В1 находится и дрожжах, молоке, печени и почках животных, мясе и др. Этот витамин повышает усвояемость пиши, способствует лучшему обмену и т. и. При недостатке его нарушается нормальная функция органов зрения. Витамин С легко разрушается при нагревании, воздействии кислорода воздуха и солнечного света, длительном хранении. Ускоряет потери витамина С хранение овощей, фруктов и ягод в тепле и на свету. Лучше сохраняется он в цитрусовых плодах. Регулирует окисление продуктов обмена углеводов, участвует в обмене аминокислот и жирных кислот, разносторонне влияет на функции сердечнососудистой, пищеварительной, эндокринной, центральной и периферической нервной систем. Недостаток витамина часто приводит к нервным расстройствам.
Витамин С содержится главным образом в овощах и плодах. Особенно богаты этим витамином хвоя, сосна, плоды шиповника, зеленые грецкие орехи, черная смородина и др. Отсутствие витамина С в пище вызывает заболевания, называемые цингой. Этот витамин укрепляет организм против инфекционных заболевании. Витамин С растворим в воде, он легко разрушается при действии кислорода воздуха и кипячении. Недостаток витамина С приводит к снижению сопротивляемости различным инфекциям, а его отсутствие — к развитию цинги. Мнение о том, что большие дозы витамина С лечат простудные заболевания, не нашло подтверждения — лишь в самом начале прием таких доз может способствовать снятию симптомов простуды.
Витамин D находится главным образом в продуктах животного происхождения: в рыбьем жире, сливочном масле, яичном желтке, икре, молоке и т. п. Этот витамин предохраняет детский организм от заболевания рахитом. При отсутствии витамина D кости становятся хрупкими, зубы плохо развиваются. Этот витамин растворяется в жирах. Регулирует обмен кальция и фосфора, способствуя их всасыванию из кишечника и отложению в костях. Витамин D образуется из провитамина в коже под действием солнечных лучей и поступает с животными продуктами: печень рыб, жирные сорта рыб (сельдь, кета, скумбрия и другие), икра, яйца, молочные жиры. Он хорошо сохраняется в консервах и продуктах кулинарной обработки, так как стоек к нагреванию. Готовые препараты витамина D следует употреблять по указанию врача.
Источник
77.Коферменты и их связь с витаминами
Коферменты, или коэнзимы — малые молекулы небелковой природы, специфически соединяющиеся с соответствующими белками, называемыми апоферментами, и играющие рольактивного центра или простетической группы молекулы фермента.
Комплекс кофермента и апофермента образует целостную, биологически активную молекулу фермента.
Роль коферментов нередко играют витамины или их метаболиты (чаще всего — фосфорилированные формы витаминов группы B). Например, коферментом фермента карбоксилазы являетсятиаминпирофосфат, коферментом многих аминотрансфераз — пиридоксаль-6-фосфат.
В роли кофактора могут выступать витамины. Например, кофактором АлАТ и АсАТ является витамин В6. витамин В1 –входит в состав мультиферментного комплекса, таким образом участвует в реакции окислительного декарбоксилирования ПВК и альфакетоглутарата. Витамин РР входит в состав НАД – никотинамидалениндинуклеотида, а витамин В2 в состав ФМН – флавин6мононуклеотида.
78. Регуляция действия ферментов: 1) частичный протеолиз – пепсиноген в пепсин под действием HCl, трипсиноген в трипсин под действием энтерокиназы, химотрипсиноген в химотрипсин под действием трипсина 2) ковалентная модификация – фосфорилирование (присоединение остатка фосфорной кислоты) и дефосфорилирование – пример – 2 фосфорилаза Б не активная + 4 АТФ 1 фосфорилаза А – Рн + 4 АДФ. И может быть все наоборот. Гликогенсинтетаза активная + АТФ гликогенсинтетаза – Рн не активная + АДФ. Адреналин повышает уровень глюкозы в крови и активируется фосфорилаза и расщепляется гликоген.
79.Активаторы ферментов: ионы Ме с 19 по 30 в системе Менделеева, восстановленные формы соединений НАДН2 ФАДН2, аллостерические активаторы, гормоны – адреналин, инсулин.
Ингибирование ферментов: 1) обратимое: а) конкурентное – когда ингибитор похож на субстрат (аллопуринол) б) не конкурентное – аллостерическое (ретроингибирование) и уменьшение доли субстрата
2) необратимое: а) специфическая – СО на цитохромы б) не специфическая – денатурация при t 0 С.
80. Классификация ферментов 1961 год – 5 международный конгресс в Москве: 1) оксидоредуктазы (имеют 5 подклассов) в основе ОВР; 2) трансферазы –перенос амино и метильной групп; 3) гидролазы – все ферменты пищеварительного тракта; расщепление с участием воды; 4) лиазы – расщепление связей без участия воды; 5) изомеразы – превращение глюкозо6фосфат в фруктозо6фосфат — реакции изомеризации; 6) лигазы (синтетазы) – синтез органических веществ с затратой энергии распада АТФ.
КФ 1: Оксидоредуктазы, катализирующие окисление или восстановление. Пример: каталаза, алкогольдегидрогеназа
КФ 2: Трансферазы, катализирующие перенос химических групп с одной молекулы субстрата на другую. Среди трансфераз особо выделяют киназы, переносящие фосфатную группу, как правило, с молекулы АТФ.
КФ 3: Гидролазы, катализирующие гидролиз химических связей. Пример: эстеразы, пепсин, трипсин, амилаза, липопротеинлипаза
КФ 4: Лиазы, катализирующие разрыв химических связей без гидролиза с образованием двойной связи в одном из продуктов.
КФ 5: Изомеразы, катализирующие структурные или геометрические изменения в молекуле субстрата.
КФ 6: Лигазы, катализирующие образование химических связей между субстратами за счет гидролиза АТФ. Пример: ДНК-полимераза
81. Энергетический обмен, катаболизм, источники восстановленных эквивалентов. Совокупность окислительных реакций, происходящих в живых организмах и обеспечивающих их энергией и метаболитами, необходимыми для осуществления процессов жизнедеятельности, называется биологическим окислением. Функции биологического окисления: 1) энергетический обмен, поддержание t тела, мышечная активность, осмотическая работа, транспорт, биосинтез 2) окисление ксенобиотиков 3) окисление токсических продуктов обмена 4) синтез ключевых метаболитов. Основными источниками энергии для организма являются белки, липиды и углеводы, поступающие с пищей. Три стадии катаболизма: 1) специфическое превращение в мономеры – аминокислоты, моносахариды, глицерин, жирные кислоты. 2) образование унифицированных продуктов – ПВК и АцКоА (моносахариды через ПВК). 3) АцКоА в ЦТК образуется СО2, вода; 3НАДН, которые в дых цепи дают воду и 3 АТФ; ФАД Н2, который в дых цепи дает воду и 2 АТФ. Источники восстановленных эквивалентов это ЦТК, все окислительно-восстановительные реакции, бета-окисление жирных кислот. В дых цепь поступает 3НАДН и ФАДН2, они образуются в следующих реакциях: НАДФН+НАДНАДФ+НАДН (трансдегидрогеназа).
82.Митохондриальная цепь окисления водорода. трансмембранный электрохимический потенциал. Перенос 2х протонов из матрикса в межмембранное пространство сопряжен с образованием градиента концентраций протонов водорода (дельта МюН). Именно в этом месте возникает пункт сопряжения, окисления и фосфорилирования. Трансмембранный электрохимический потенциал – это разница протонов между матриксом и наружной частью. Образуется АТФ (АДФ+Фн) путем фосфорилирования с использованием энергии окисления водорода.
83. НАД-зависимые дегидрогеназы – это сложные ферменты, относящиеся к классу оксидоредуктаз и состоящие из белковой и небелковой части. Небелковая часть представлена коферментами НАД или НАДФ. НАД – никотинамидадениндинуклеотид, в его структуре два мононуклеотида, соединенные фосфоэфирной связью. В состав одного мононуклеотида входит амид никотиновой кислоты (витамин ниацин), рибоза и остаток фосфорной кислоты. Второй мононуклеотид представлен аденином, Д-рибозой и также остатком фосфорной кислоты. НАД-зависимые дегидрогеназы акцептируют от субстрата два атома водорода, первый присоединяется к НАД с образованием НАДН, второй выделяется в виде протона. Изоцитрат под действием изоцитратдегидрогеназы образуется альфа-кетоглуторат СО2 НАДН+Н + . Источники НАДН: изоцитратдегидрогеназа, малатдегидрогеназа, мультиферментный комплекс окислительного декарбоксилирования альфа-кетоглутората, бета-окисление жирных кислот.
84. Флавиновые ферменты – это сложные ферменты, состоящие из белковой и небелковой части, небелковой частью представлена простерическая группа ФМН – флавинмононуклеотид или ФАД – флавинадениндинуклеотид. ФМН состоит из витамина В2, пятиатомного спирта ретибола, остатка фосфорной кислоты; в структуре ФАД два мононуклеотида, соединенных фосфоэфирной связью. В состав одного мононуклеотида входит витамин В2, пятиатомный спирт ретибол, остаток фосфорной кислоты. Второй мононуклеотид представлен АМФ – Аденин, рибоза, остаток фосфорной кислоты.
85. Дыхательная цепь, железо-серопротеины, цитохромы. Железо-серопротеины относят к негемовым железопротеинам. Известно три вида FeS-белков: 1) один атом железа тетраэдрически связан с сульфгидрильными группами четырех остатков цистеина; 2) (Fe2S2) содержит 2 атома железа и 2 неорганических сульфида, присоединенных к четырем остаткам цистеина; 3) (Fе4S4) содержит четыре атома железа, четыре сульфгидридные группы и четыре остатка цистеина. Атом железа в этих комплексах может находиться в восстановленном (Fe ++ ) и окисленном (Fe +++ ) состояниях. НАДН-дегидрогеназа содержит второй и третий типы железо-серопротеинов. Цитохромы – это ферментные гемопротеины, транспортирующие только электроны. В качестве простетической группы они содержат гем. В дых цепи располагаются 5 цитохромов, отличающихся по строению простетических групп и имеющих разные спектры поглощения. В цитохроме b гем нековалентно связан с белковой частью, в то время как в цитохромах с и с1 – связь с белковой частью ковалентная. Цитохромы а и а3 имеют иную простетическую группу, называемую гемом-а. Она отличается от простетической группы цитохромов с и с1 наличием формильной группы вместо одной из метильных групп и углеводородной цепью вместо одного из остатков винила. В составе цитохромов а и а3 находятся два атома меди. Простетической группой цитохромов в, с1 и с служит протопорферин 1Х. Цитохром с имеет ковалентно связанный гем и выполняет челночные функции – передает электроны цитохрома с1 к цитохромоксидазе.
86. образование макроэргических связей в дыхательной цепи. Коэффициент Р/О. Разобщение дыхания и фосфорилирования в дыхательной цепи. Коэффициент Р/О – это количество АТФ, которое образовалось в дых цепи. Р/О может быть равно 3 или 2 АТФ. Три АТФ образуется при участии НАДН, две АТФ при участии ФАДН2. В окислительном фосфорилировании не образуется дельта МюН, т.к. есть вещества, которые принимают протоны на себя. В окислительном фосфорилировании не происходит образования АТФ и энергия выделяется в виде тепла.
87. Окислительное субстратное фосфорилирование в процессе биологического окисления. Образование АТФ в процессе метаболизма идет двумя путями – окислительного и субстратного фосфорилирования. Основными источниками поставляющими энергию являются: 1) дых цепь 2) ЦТК 3) гликолиз. Возникновение макроэргической связи в момент окисления субстрата с дальнейшей активацией неорганического фосфата и его переносом на АДФ с образованием АТФ называют субстратным фосфорилированием. В данном случае окисление субстрата связано с фосфорилированием АДФ. Примерами реакций субстратного фосфорилирования являются две реакции гликолиза – окисление 3-фосфоглицеринового альдегида в 1,3-дифосфоглицериновую кислоту, и окисление 2-фосфоглицериновой кислоты в 2-фосфоэнолпировиноградную кислоту; а также одна реакция ЦТК — окисление сукцинил-КоА в янтарную кислоту.Основная масса АТФ образуется путем окислительного фосфорилирования. В процессе окислительного фосфорилирования окисляемый субстрат участия не принимает, а активирование неорганического фосфата сопряжено с переносом электронов и протонов водорода с коферментов дегидрогеназ (принимающих участие в окислении субстрата) к молекулярному кислороду. Сопряжение окисления с фосфорилированием АДФ и последующим образованием АТФ называют окислительным фосфорилированием. Процессы сопряжения окисления и фосфорилирования идут в дых цепи.
88. Образование СО2 в процессе биологического окисления. СО2 в организме образуется двумя путями – путем прямого и окислительного декарбоксилирования. Основная масса СО2 образуется в ЦТК. Первая молекула СО2 образуется путем прямого декарбоксилирования изоцитрата, при этом изоцитратдегидрогеназа обладает декарбоксилирующим эффектом. Вторая молекула СО2 путем окислительного декарбоксилирования альфа-кетоглутората. Одна молекула СО2 образуется в результате окислительного декарбоксилирования ПВК. Человек за сутки выделяет около 500 мл СО2.
89. Виды декарбоксилирования в ЦТК. В ЦТК есть только два типа декарбоксилирования – прямое и окислительное. 1) Прямое декарбоксилирование изоцитрата под действием изоцитратдегидрогеназы, которая обладает декарбоксилирующим эффектом, превращается в альфа-кетоглуторат и НАДН, который является источником водорода для дыхательной цепи, окисление которого приводит к образованию 3х АТФ и воды. Кроме того в этой реакции образуется СО2. 2) Окислительное декарбоксилирование альфа-кетоглутората происходит под действием альфа-кетоглуторатдегидрогеназного комплекса, который включает три фермента и пять кофакторов – ТДФНSКоА, НАД, ФАД, липоевая кислота. Продуктом реакции является образование макроэргического соединения – сукцинил-КоА. В результате этой реакции образуется еще одна молекула восстановительного эквивалента НАДН и СО2.
90. Микросомальное окисление также как митохондриальное, происходит в митохондриях. Но в микросомальном окислении кислород используется с пластической целью, он включается в субстрат. Примерами микросомального окисления являются – окисления ксенобиотиков, синтез стероидных гормонов, активных форм витаминов, жирных кислот, холестерина. Источником водорода в микросомальном окислении служит НАДФН. При микросомальном окислении энергии не образуется.
91. Пути использования, токсичность кислорода, механизмы защиты. 1) митохондриальные окисления – образование воды – оксидазный способ. 2) в микросомальным окислением с пластической целью – оксигеназный способ. 3) для образования Н2О2 – пероксидазный способ. Токсичность кислорода связано с тем, что в ходе окислительных реакций кислород может принимать дополнительный электрон и превращаться в супероксидный радикал (анион). Присоединение двух дополнительных электронов к супероксидному аниону (О2 — ) ведет к образованию пероксидных анионов (О2 -2 ). О2 — +е+2Н + Н2О2; О2 — е+О2. В результате реакции дисмутации, катализируемой супероксиддисмутазой (СОД), образуется перикись водорода: О2 — +О2 — +2Н + Н2О2+О2. Такие формы кислорода имеют высокую химическую активность, реагируют со многими веществами в организме, в том числе с нуклеиновыми кислотами, белками, липидами, оказывая повреждающее действие. Активные формы кислорода запускают цепные реакции перекисного окисления липидов. В процессе ПОЛ образуются органические перекиси. ПОЛ приводит к повреждающему воздействию мембран клеток. Активные формы кислорода образуются в организме и в реакциях неферментативного окисления ряда веществ. В связи с тем, что образование активных форм кислорода ведет к повреждающему эффекту, можно говорить о токсичности кислорода и механизмах защиты. Имеется два способа защиты: 1) ферментативные пути – активируют пероксидаза и каталаза. Пероксиды выступают в роли акцепторов водорода, донорами которых являются органические субстраты. 2Н2О22Н2О+О2 (катализирует каталаза). 2) неферментативные пути – используются препараты-ловушки активных форм О2 – витамин Е, К, различные хиноны.
Источник