Состав кофермента над входит витамин
Полагают, что эти ионы заставляют молекулы фермента или субстрата принять форму, способствующую образованию фермент-субстратного комплекса. Тем самым увеличиваются шансы на то, что фермент и субстрат действительно прореагируют друг с другом, а следовательно, возрастает и скорость реакции, катализируемой данным ферментом. Так, например, активность амилазы слюны повышается в присутствии хлорид-ионов.
Простетические группы
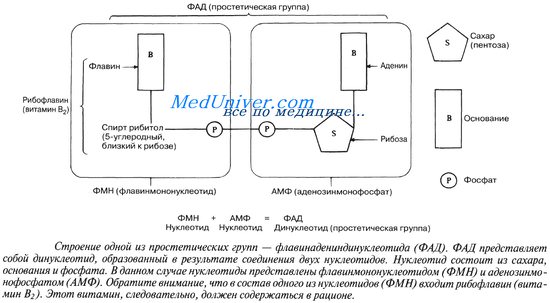
Если кофактор прочно связан с ферментом и остается в этом связанном состоянии постоянно, то его называют простетической группой (от греч. prosthekf — добавление). Роль простети-ческих групп играют органические молекулы. Они помогают ферменту осуществлять его каталитическую функцию, как это видно на примере флавинадениндинуклеотида (ФАД). ФАД содержит рибофлавин (витамин В2), который является водород-акцепторной частью его молекулы.
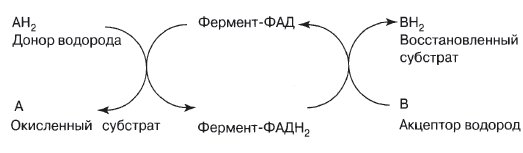
Функция ФАД связана с окислительными путями клетки, в частности с процессом дыхания, в котором ФАД играет роль одного из переносчиков в дыхательной цепи.
Конечный результат: 2Н переносятся от А к В. В качестве связующего звена между А и В действует один фермент. АНг и В вступают в соединение с активным центром фермента, и ФАД передает Нг от одного субстрата к другому.
Гем — это железосодержащая простетическая группа. Его молекула имеет форму плоского кольца (порфириновое кольцо, такое же, как у хлорофилла), в центре которого находится атом железа. Гем выполняет в организме ряд биологически важных функций.
Перенос электронов. В качестве простетиче-ской группы цитохромов) гем выступает как переносчик электронов. Присоединяя электроны, железо восстанавливается до Fe(II), а отдавая их, окисляется до Fe(III). Гем, следовательно, принимает участие в окислительно-восстановительных реакциях за счет обратимых изменений валентности железа.
Перенос кислорода. Гемоглобин и миоглобин — два гемсодержащих белка, осуществляющих перенос кислорода. Железо находится в них в восстановленной, Fe(II), форме.
Каталитическая функция. Гем входит в состав каталаз и пероксидаз, катализирующих расщепление пероксида водорода до кислорода и воды. Содержится он также и в некоторых других ферментах.
Коферменты (например, НАД, НАДФ, ацетилкофермент А, АТФ)
Коферменты, как и простетические группы, — это органические молекулы, выполняющие функцию кофакторов, но в отличие от простетических групп они сохраняют связь с ферментом только в ходе реакции. Все коферменты представляют собой производные витаминов.
Никотинамидадениндинуклеотид (НАД)
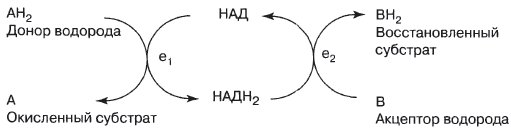
НАД — производное витамина ниацина («никотиновой кислоты») — может существовать как в окисленной, так и в восстановленной форме. В окисленной форме НАД при катализе играет роль акцептора водорода: где ei и е2 — две разные дегидрогеназы.
Конечный результат: 2Н переносятся от А к В. Здесь в качестве связующего звена между двумя различными ферментными системами ei и е2 действует кофермент.
Источник
Коферменты: что это такое, польза, применение в спорте
Коферменты представляют собой органические соединения небелковой природы, которые необходимы для функционирования многих ферментов. Большинство из них являются производными витаминов.
Причиной нарушения метаболизма и снижения синтеза полезных веществ в организме часто является снижение активности некоторых видов ферментов. Поэтому то коэнзимы столь нам необходимы.
В узком смысле, кофермент – это коэнзим Q10, производная фолиевой кислоты и некоторых других витаминов. Важное значение для организма человека имеют те коферменты, которые продуцируются витаминами группы B.
Кофермент нужен для того, чтобы повысить производительность клеточной энергии, которая нужна для поддержания жизнедеятельности. Любой процесс, который протекает в организме человека, требует колоссального энергетического ресурса, будь то умственная деятельность, работа сердечно-сосудистой или пищеварительной системы, физическая активность при нагрузке на опорно-двигательный аппарат. Благодаря реакции, в которую коферменты вступают с ферментами, продуцируется необходимая энергия.
Функции коферментов
Коферменты представляют собой небелковые соединения, которые способствуют активации потенциала ферментов. Они выполняют 2 основные функции:
- Участвуют в каталитических процессах. Кофермент сам по себе не вызывает в организме необходимых молекулярных превращений, в состав ферментов он входит вместе с апоферментом, и только при их взаимодействии происходят каталитические процессы связывания субстрата.
- Транспортировочная функция. Кофермент соединяется с субстратом, в результате чего образуется прочный транспортировочный канал, по которому свободно перемещаются молекулы до центра другого фермента.
Все коферменты объединяет одно важное свойство – они являются термически устойчивыми соединениями, но свойственные им химические реакции довольно сильно разнятся.
Классификация коферментов
По способам взаимодействия с апоферментом коферменты делятся на:
- Растворимые – во время реакции соединяется с молекулой фермента, после чего изменяется по химическому составу и высвобождается заново.
- Простетические – прочно связаны с апоферментом, в процессе реакции находится в активном центре фермента. Их регенерация происходит при взаимодействии с другим коферментом или субстратом.
По химической структуре коферменты делятся на три группы:
- алифатические (глутатион, липоевая кислота и др.)
- гетероциклические (пиридоксальфосфат, тетрагидрофолиевая кислота, нуклеозидфосфаты и их производные (КоА, ФМН, ФАД, НАД и др.), металлопорфириновые гемы и др.
- ароматические (убихиноны).
По функциональному признаку выделяют две группы коферментов:
- окислительно-восстановительные,
- коферменты переноса групп.
Коферменты в спортивной фармакологии
При интенсивных физических нагрузках расходуется большое количество энергии, ее запас в организме истощается, а многие витамины и питательные вещества потребляются гораздо быстрее, чем вырабатываются. Спортсмены испытывают физическую слабость, нервное истощение, нехватку сил. Для того чтобы помочь избежать многих симптомов были разработаны специальные препараты с коферментами в составе. Их спектр действия очень широк, назначаются они не только спортсменам, но и людям с достаточно серьезными заболеваниями.
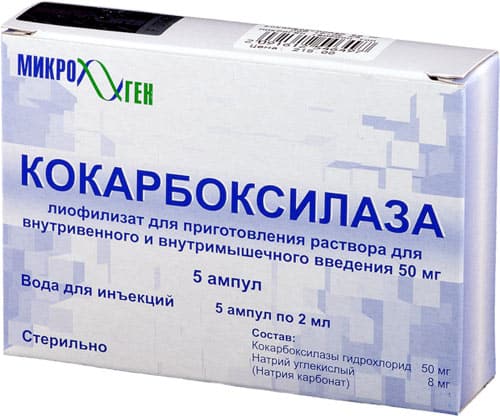
Кокарбоксилаза
Кофермент, который образуется только из поступающего в организм тиамина. У спортсменов он служит средством профилактики перенапряжения миокарда, расстройств нервной системы. Препарат назначается при радикулитах, невритах, а также острой печеночной недостаточности. Вводится внутривенно, разовая доза не должна быть менее 100 мг.
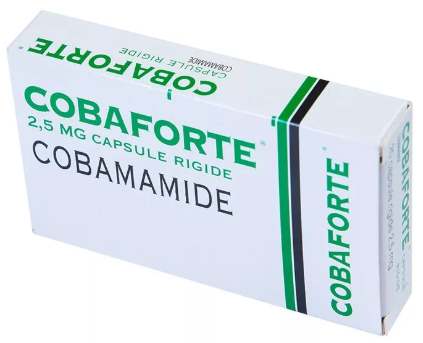
Кобамамид
Заменяет по действию функционал витамина B12, является анаболиком. Помогает спортсменам нарастить мышечную массу, увеличивает выносливость, способствует быстрому восстановлению после занятий. Выпускается в форме таблеток и растворов для внутривенного введения, суточная норма составляет 3 таблетки или 1000 мкг. Длительность курса – не более 20 дней.
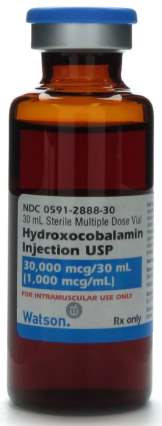
Оксикобаламин
По своему действию схож с витамином B12, но намного дольше держится в крови и гораздо оперативнее преобразуется в коферментную формулу благодаря прочному соединению с плазменными белками.
Пиридоксальфосфат
Для препарата характерны все свойства витамина B6. От него он отличается быстрым терапевтическим эффектом, назначается к приему даже при нарушении фосфорилирования пиридоксина. Принимается три раза в день, суточная доза составляет не более 0,06 гр, а курс – не дольше месяца.
Пиридитол
Активизирует метаболические процессы центральной нервной системы, повышает проходимость глюкозы, препятствует избыточному образованию молочной кислоты, повышает защитные свойства тканей, в том числе устойчивость к гипоксии, которая возникает во время интенсивных спортивных тренировок. Принимают препарат три раза в день по 0,1 гр. после завтрака в течение месяца
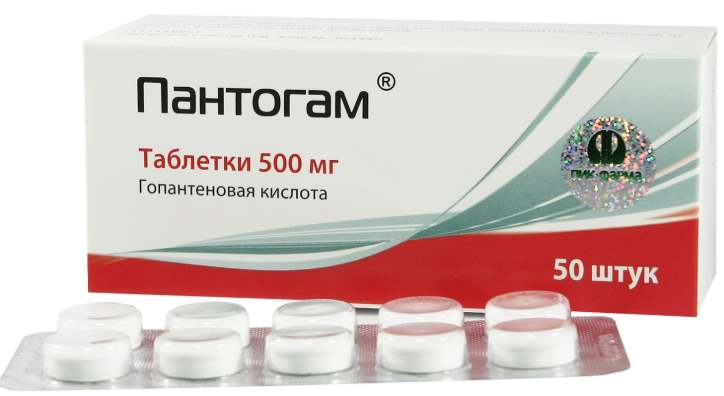
Пантогам
Является гомологом пантотеновой кислоты, ускоряет обменные процессы, снижает проявление болевых реакций, повышает устойчивость клеток к гипоксии. Действие препарата направлено на активацию работы головного мозга, повышение выносливости, показан к применению при черепно-мозговых травмах различного типа. Таблетки принимаются в течение месяца по 0,5 гр не чаще трех раз в день.
Карнитин
Выпускается в форме препарата для инъекций, действие которых направлено на активацию жирового обмена, ускорение регенерации клеток. Оказывает анаболическое, антигипоксическое и антитиреоидное действие. Является синтетическим заменителем витамина B6. Эффективен в виде внутривенной капельницы.
Флавинат
Образуется в организме из рибофлавина, активно участвует в углеводном, липидном и аминокислотном обмене. Выпускается в виде раствора для внутримышечных инъекций, так как его усвоение в желудке неэффективно при нарушении всасывания рибофлавина.
Липоевая кислота
Нормализует углеводный обмен. Повышает скорость окисления углеводов и жирных кислот, что способствует повышению энергетического запаса.
Подписывайтесь на наш канал в Яндекс.Дзен!
Источник
КОФЕРМЕНТЫ
КОФЕРМЕНТЫ (син. коэнзимы) — низкомолекулярные органические соединения биологического происхождения, необходимые в качестве дополнительных специфических компонентов (кофакторов) для осуществления каталитического действия ряда ферментов. Многие К. представляют собой производные витаминов. Биол, эффект значительной группы витаминов (группы В) определяется их превращением в К. и ферменты в клетках организма. Были сделаны попытки (и небезуспешные) прямого использования некоторых К. с леч. целями. Трудности, которые при этом возникают, состоят в том, что не всегда производятся количественные определения содержания К. в крови и органах и еще реже определяется активность ферментов, синтезирующих или разрушающих исследуемые К., в норме и патологии. Обнаруженный при каком-либо заболевании недостаток того или иного К. обычно пытаются устранить, вводя в организм соответствующий витамин. Но если нарушены системы синтеза недостающего К., что нередко имеет место, то введение такого витамина теряет смысл: терапевтический эффект можно получить только введением недостающего кофермента. С леч. целями применяют кокарбоксилазу (см. Тиамин), ФАД, коферментные формы витамина В12 (см. Цианокобаламин) и некоторые другие К. В леч. целях К. вводят парентерально, но и при этом условии не всегда имеется уверенность, что они могут без расщепления проникнуть к месту своего действия (во внутриклеточную среду).
Обладая небольшим мол. весом, К., в отличие от биокатализаторов белковой природы (ферментов), характеризуются термостабильностью и доступностью диализу. Дыхательные хромогены растений (полифенолы), глутаминовую к-ту, орнитин, бисфосфаты (дифосфаты) глюкозы и глицериновой к-ты и другие метаболиты, действующие при определенных обстоятельствах как кофакторы ферментативных процессов переноса, нередко обозначают как К. соответствующих процессов. Правильнее применять термин «кофермент» только к соединениям, биол, функция которых сводится целиком или преимущественно к их специфическому участию в действии ферментов (см.).
Термин «кофермент» был предложен Г. Бертраном в 1897 г. для обозначения функции солей марганца, которые он считал специфическим кофактором фенол азы (лакказы); однако теперь неорганические компоненты ферментных систем не принято относить к числу К. Существование истинного (органического) К. впервые установили англ. биохимики Харден (A. Harden) и Янг (W. Young) в 1904 г., показавшие, что из ферментных экстрактов дрожжевых клеток при диализе удаляется термостабильное органическое вещество, необходимое для действия ферментного комплекса, катализирующего спиртовое брожение (см.). Этот вспомогательный катализатор брожения Харден и Янг назвали козимазой; его строение было установлено в 1936 г. в лабораториях X. Эйлер- Xeльпина и О. Варбурга почти одновременно.
Механизм действия К. неодинаков. Во многих случаях они действуют в качестве промежуточных акцепторов (переносчиков) определенных хим. группировок (фосфатных, ацильных, аминных и др.), атомов водорода или электронов. В других случаях К. участвуют в активировании молекул субстратов ферментативных реакций, образуя с этими молекулами реакционно-способные промежуточные соединения. В виде таких соединений субстраты подвергаются определенным ферментативным превращениям; таковы функции глутатиона (см.) как кофермента глиоксалазы и дегидрогеназы формальдегида, КоА — при ряде превращении жирных кислот (см.) и других органических к-т и т. д.
Типичные К. образуют непрочные сильно диссоциированные соединения со специфическими белками (апоферментами) растворимых ферментов, от которых они легко могут быть отделены путем диализа (см.) или гель-фильтрация (см.). При многих реакциях переноса групп, протекающих при сопряженном действии двух ферментных белков, происходит поочередное обратимое присоединение к молекулам этих белков частиц К. в двух формах — акцепторной и донорной (напр., окисленной и восстановленной, фосфорилированной и нефосфорилированной). В приведенной ниже схеме показан (в несколько упрощенной форме) механизм обратимого переноса водорода между молекулой донора водорода (АН2) и молекулой акцептора (Б) при действии двух дегидрогеназ (Фа и Фб) и кофермента (Ко):
В полном цикле окислительно-восстановительного процесса (реакции 1—6) кофермент кодегидрогеназа не изменяется и не входит в баланс продуктов реакции, т. е. служит катализатором. Если же рассматриваются последовательные фазы цикла, протекающие каждая с участием одного фермента (реакции 1—3 и 4—6), то Ко и КоН2 выступают наравне с молекулами АН2, А, Б, БН2 в качестве второго субстрата. В этом же смысле относительным является различие между субстратами и диссоциирующими К., участвующими в сопряженных реакциях переноса фосфатных, ацильных, гликозильных и других групп.
У многих двухкомпонентных ферментов, построенных по типу протеидов, апофермент образует с небелковым термостабильным компонентом прочное, труднодиссоциирующее соединение. Небелковые компоненты ферментов-протеидов, обычно называемые простетическими группами (напр., флавиновые нуклеотиды, пиридоксальфосфат, металлопорфирины), взаимодействуют с субстратом, оставаясь на всем протяжении ферментативной реакции в составе нерасщепленной молекулы одного протеида. Термин «кофермент» обычно распространяют и на химически взаимодействующие с молекулами субстратов, прочно связанные органические простетические группы ферментов, которые трудно отграничить от легко диссоциирующих К., т. к. между обоими типами кофакторов существуют постепенные переходы.
Точно также нельзя провести резкой грани между К. и нек-рыми промежуточными продуктами обмена веществ (метаболитами), которые в ферментативных процессах выступают то как обычные субстраты, подвергающиеся в данном процессе в основном необратимому изменению, то как необходимые вспомогательные катализаторы при сопряженных ферментативных превращениях, из которых эти метаболиты выходят неизмененными. Метаболиты такого рода могут служить промежуточными акцепторами тех или иных групп в процессах ферментативного переноса, протекающих аналогично процессу, схематично изображенному выше (напр., роль полифенолов как переносчиков водорода в дыхании растительных клеток, роль глутаминовой к-ты в переносе аминных групп путем реакций трансаминирования и т. п.), или в более сложных циклических превращениях с участием нескольких ферментов (примером может служить функция орнитина в цикле образования мочевины). Несколько иной характер носит коферментоподобное действие 1,6-бисфосфоглюкозы, к-рая служит необходимым кофактором и в то же время промежуточной ступенью в процессе межмолекулярного переноса фосфатных остатков при взаимопревращении 1-фосфоглюкозы и 6-фосфоглюкозы под действием фосфоглюкомутазы, когда молекула кофактора переходит в молекулу конечного продукта, отдавая один фосфатный остаток исходному продукту, из к-рого при этом образуется новая молекула кофактора. Точно такую же функцию выполняет 2,3-бисфосфоглицериновая к-та при катализируемом другой фосфомутазой взаимопревращении 2-фосфоглицериновой и 3-фосфоглицериновой к-т.
К. весьма разнообразны по хим. строению. Однако чаще всего среди них встречаются соединения двух типов: а) нуклеотиды и некоторые другие органические производные фосфорной к-ты; б) пептиды и их производные (напр., фолиевая к-та, КоА, глутатион). У животных и у многих микроорганизмов для построения молекул ряда К. необходимы соединения, которые этими организмами не синтезируются и должны доставляться с пищей, т. е. витамины (см.). Водорастворимые витамины группы В в большинстве своем входят в состав К., строение и функции которых известны (это относится к тиамину, рибофлавину, пиридоксалю, никотинамиду, пантотеновой к-те), или же могут сами действовать как активные молекулы К. (витамин В12, фолиевая к-та). То же, вероятно, относится и к другим водо- и жирорастворимым витаминам, роль которых в процессах биол, катализа еще полностью не выяснена.
Ниже перечислены важнейшие К. с указанием типа их строения и основных видов ферментативных превращений, в которых они участвуют. В статьях об отдельных К. приведены более детальные сведения об их структуре и механизме действия.
Коферменты нуклеотидной природы. Адениловые рибонуклеотиды (аденозин-5′-моно-, ди- и трифосфорные к-ты) участвуют в многочисленных реакциях активирования и переноса орто- и пирофосфатных остатков, остатков аминокислот (аминоацилов), угольной и серной к-т, а также в ряде других ферментативных превращений. Аналогичные функции в определенных случаях выполняют производные инозин-5′-фосфорной и гуанозин-5′-фосфорной к-т.
Гуаниловые рибоиуклеотиды (гуанозин-5′-моно-, ди- и трифосфорные к-ты) играют роль К. при реакциях переноса остатка янтарной к-ты (сукцинила), биосинтезе рибонуклеопротеидов в микросомах, биосинтезе адениловой к-ты из инозиновой и, возможно, при переносе остатков маннозы.
Цитидиловые рибонуклеотиды (цитидин-5′-фосфорные к-ты) при биосинтезе фосфатидов играют роль К. переноса остатков О-фосфоэтанол холина, О-фосфоэтаноламина и т. д.
Уридиловые рибонуклеотиды (уридин-5′-фосфорные к-ты) выполняют функции К. в процессах трансгликозилирования, т. е. переноса остатков моноз (глюкозы, галактозы и др.) и их производных (остатков гексозаминов, глюкуроновой к-ты и т. п.) при биосинтезе ди- и полисахаридов, глюкуронозидов, гексозаминидов (мукополисахаридов), а также при активировании остатков сахаров и их производных в некоторых других ферментативных процессах (напр., взаимопревращении глюкозы и галактозы и др.).
Никотинамидадениндинуклеотид (НАД) участвует в важнейших для клеточного обмена реакциях переноса водорода в качестве специфического К. многочисленных дегидрогеназ (см.).
Никотинамидадениндинуклеотидфосфат (НАДФ) участвует в важнейших для клеточного обмена реакциях переноса водорода в качестве специфического К. некоторых дегидрогеназ.
Флавинмононуклеотид (ФМН) участвует в биол, переносе водорода как К. (простетическая группа) некоторых флавиновых («желтых») окислительных ферментов.
Флавинадениндинуклеотид (ФАД) участвует в биол, переносе водорода как К. (простетическая группа) большинства флавиновых («желтых») окислительных ферментов.
Кофермент А (КоА, восстановленная форма — KoA-SH, кофермент ацилирования; соединение аденозин-З’ ,5′-бисфосфорной к-ты с пантотенил-аминоэтантиолом или пантетеином) образует с остатками уксусной и других органических к-т тиоэфиры типа R-СО—S-КоА, где R — остаток органической к-ты, и играет роль К. в переносе и активировании кислотных остатков как при реакциях ацилирования (синтез ацетилхолина, гиппуровой к-ты, парных желчных к-т и т. п.), так и при многих других ферментативных превращениях кислотных остатков (реакции конденсации, оксидоредукции или обратимой гидратации ненасыщенных к-т). При участии КоА протекает ряд промежуточных реакций клеточного дыхания, биосинтеза и окисления жирных к-т, синтеза стероидов, терпенов, каучука и т. п.
Кофермент B12 [KoB12; син. кобаламин, ДБК-кофермент, альфа-(5,6-диметилбензимидазолил)-кобамидцианид]. Возможно, что разнообразные биол, функции витамина В12, хим. механизм которых еще не ясен, напр, в процессе кроветворения, при биосинтезе метильных групп, превращениях сульфгидрильных групп (SH-групп) и т. д., обусловлены его ролью как К. в процессе биосинтеза белков-ферментов.
Другие коферменты, содержащие фосфатные остатки. Дифосфотиамин служит К. при декарбоксилировании (простом и окислительном) пировиноградной, альфа-кетоглутаровой и других альфа-кетокислот, а также при реакциях расщепления углеродной цепи фосфорилированных кетосахаров под действием особой группы ферментов (кетолазы, транскетолазы, фосфокетолазы).
Пиридоксальфосфат конденсируется с аминокислотами (и аминами) в активные промежуточные соединения типа оснований Шиффа (см. Шиффа основания); является К. (простетической группой) ферментов, катализирующих реакции трансаминирования и декарбоксилирования, а также многих других ферментов, которые осуществляют разнообразные превращения аминокислот (реакции расщепления, замещения, конденсации), играющие важную роль в клеточном обмене.
Коферменты пептидной природы. Кофермент формилирования. Восстановленная фолиевая к-та и ее производные, содержащие три или семь остатков глутаминовой к-ты, соединенных гамма-пептидными связями, играют роль К. в промежуточном обмене так наз. одноуглеродных, или «C1», остатков (формила, оксиметила и метила), участвуя как в реакциях переноса этих остатков, так и в их окислительно-восстановительных взаимопревращениях. Формильные и оксиметильные производные Н4-фолиевой к-ты являются «активными формами» муравьиной к-ты и формальдегида в процессах биосинтеза и окисления метильных групп, в обмене серина, глицина, гистидина, метионина, пуриновых оснований и т. д.
Глутатион. Восстановленный глутатион (Г-SH) действует по типу К. при превращении метилглиоксаля в молочную к-ту под влиянием глиоксалазы, при ферментативной дегидрогенизации формальдегида, в определенных стадиях биол, окисления тирозина и т. д. Кроме того, глутатион (см.) играет большую роль в защите различных тиоловых (сульфгидрильных) ферментов от инактивирования в результате окисления SH-групп или связывания их тяжелыми металлами и другими SH-ядами.
Прочие коферменты. Липоевая кислота является вторым К. дегидрогеназ пировиноградной и альфа-кетоглутаровой к-т (наряду с дифосфотиамином); при действии этих ферментов остаток липоевой к-ты, связанный амидной связью (СО — NH) со специфическими ферментными белками, выполняет функции промежуточного акцептора (переносчика) водорода и ацильных остатков (ацетила, сукцинила). Другие предполагаемые функции этого К. недостаточно изучены.
Витамин E (токоферол), витамин К (филлохинон) и продукты их окислительно-восстановительиых превращений или близкородственные производные n-бензохинона (убихинон, кофермент Q) рассматриваются как К. (переносчики водорода), участвующие в определенных промежуточных реакциях дыхательной окислительной цепи и в сопряженном с ними дыхательном фосфорилировании (см.). Установлено, что филлохинон (витамин К) играет роль К. в биосинтезе остатков альфа-карбоксиглутаминовой к-ты, входящих в состав молекул белковых компонентов системы свертывания крови.
Биотин — водорастворимый витамин, выполняющий роль К. или простетической группы в составе ряда ферментов, катализирующих реакции карбоксилирования — декарбоксилирования некоторых органических к-т (пировиноградной, пропионовой и др.). Эти ферменты имеют строение биотинил-протеидов, в которых соответствующий биотину ацильный остаток (биотинил) присоединен амидной связью к N6-аминогруппе одного из остатков лизина молекулы белка.
Аскорбиновая кислота служит активатором ферментной системы окисления тирозина в животных тканях и некоторых других ферментных систем (гидроксилаз), при действии которых в ядро ароматических и гетероциклических соединений, в т. ч. пептидно-связанных остатков пролина при биосинтезе коллагена (см.) и родственных белков, вводятся гидроксильные группы. В этих системах аскорбиновая к-та играет роль второго субстрата — донора водорода, окисляемого молекулярным кислородом параллельно с циклическим субстратом, а не роль истинного К. (специфического биокатализатора).
Библиография: Болдуин Э. Основы динамической биохимии, пер. с англ., с. 55 и др., М., 1949; Витамины, под ред. М. И. Смирнова, М., 1974; Диксон М. и Уэбб Э. Ферменты, пер. с англ., М., 1966; Коферменты, под ред. В. А. Яковлева, М., 1973; Кочетов Г. А. Тиаминовые ферменты, М., 1978, библиогр.; Ферменты, под ред. А. Е. Браунштейна, с. 147, М., 1964, библиогр.
Источник