Сохранение репродуктивного здоровья женщины
Что включает в себя понятие «женское», или репродуктивное здоровье? Это “состояние полного физического, умственного и социального благополучия во всех вопросах, касающихся репродуктивной системы, её функций и процессов, включая воспроизводство и гармонию в психосоциальных и эмоциональных отношениях в семье”, согласно трактовке ВОЗ.
Факторы репродуктивного здоровья:
- Безопасная половая жизнь, возможность применения эффективных методов контрацепции;
- Возможность вынашивания и рождения здорового ребёнка и другие факторы, отражающие социальную жизнь людей;
- Профилактика и своевременное лечение злокачественных новообразований и других заболеваний репродуктивной системы;
- Сохранения здоровья женщины в течение перименопаузального (климактерического) периода.
К сожалению, современной женщине не всегда удается сохранить репродуктивное здоровье. Неблагоприятная экология, частые стрессы, несбалансированное, нерегулярное питание, неконтролируемый прием антибиотиков, а также перенесенные заболевания, передающиеся половым путем, снижают шансы стать счастливыми родителями. В наше время можно констатировать рост числа бесплодных пар, которым приходится прибегать к методу экстракорпорального оплодотворения.
Увеличился возраст рождения первого ребенка. Современная женщина сначала делает карьеру, дающую материальную стабильность, и лишь потом задумывается о детях.
Общие рекомендации по сохранению репродуктивного здоровья женщины:
- Оптимальный возраст для рождения ребенка или нескольких – это 20-35 лет. Медицинские специалисты свидетельствуют о большем количестве осложнений здоровья мамы и малыша, когда женщина беременеет раньше или позднее. Учитывайте этот факт;
- Интервалы между родами должны составлять не менее 2-2,5 лет. Это возможность для роженицы восстановить силы и ресурсы организма;
- Желая отодвинуть сроки рождения ребенка, используйте современные методы контрацепции. А если непреднамеренная беременность стала свершившимся фактом, обращайтесь к врачу как можно раньше для снижения риска осложнений после аборта;
- Есть вероятность забеременеть после родов или аборта до того, как придет первая менструация. Подберите надежный метод контрацепции вместе с врачом до возобновления половой жизни;
- Обязательное своевременное лечение инфекций ЗППП, если это случилось.
Когда идти к врачу девочке? И как понять, что развитие ребенка идет с отклонениями?
Первый осмотр девочек проводится еще в родильном доме врачом-неонатологом. Затем желательно показать ребенка детскому гинекологу, когда исполнится год. Обязателен осмотр врача во время оформления в детский сад, а затем перед поступлением в школу.
Детский гинеколог специализируется на заболеваниях женской половой сферы у девочек до 18 лет. Он не только выявляет и лечит заболевания, но и всегда может проконсультировать, в том числе, и по поводу контрацепции и предотвращения нежелательной беременности.
Многие мамы недоумевают: зачем в обязательном порядке вести трехлетних и шестилетних девочек к детскому гинекологу? Какие гинекологические проблемы могут выявить у таких малышек? Однако, как утверждают специалисты, девочки страдают практически всеми теми гинекологическими недугами, что и взрослые женщины. Мало того, многие “взрослые” болезни в последние годы встречаются у девочек намного чаще, чем раньше. В шесть-семь лет в детском организме начинает запускаться процесс полового созревания, поэтому врач обязательно должен осмотреть ребенка. Если вторичные половые признаки появились у девочки до 7 лет, то это отклонение от нормы.
С началом менструального цикла поход к детскому гинекологу тоже обязателен, поскольку это один из самых важных моментов в развитии девочки. Нормальным считается начало менструации в 12,5 лет, хотя может быть и раньше, и позже. Однако если до 14 лет у девочки нет вторичных половых признаков и до 16 лет менструации, это должно насторожить родителей и заставить их обратиться к врачу- гинекологу.
Как подготовить подростка к предстоящему в будущем вступлению во взрослую жизнь?
В лучшем случае, сами родители должны рассказать подростку о здоровых половых отношениях, иначе он будет искать информацию среди друзей, в соцсетях. Девочками до 12 лет можно говорить об их женском здоровье и будущем материнстве достаточно открыто. Они вполне благожелательно относятся к своей будущей роли в семье.
Минимальный ликбез полового воспитания включает следующие темы для обсуждения с родителями, врачом:
- Методы контрацепции;
- Риски ЗППП (заболевваний, передающихся половым путем) и меры их профилактики;
- Планирование желаемой беременности;
- Соблюдение правил личной гигиены;
- Здоровый образ жизни и укрепление иммунитета (Девочке нельзя даже пробовать курить, потому что эта яйцеклетка «пробует курить» вместе с нею, и это наносит непоправимый вред. Тем более, нельзя пробовать алкоголь, наркотики , потому что яйцеклетка «пробует» все вместе с нею и вместе с нею болеет, неправильно ложится спать и так далее); ;
- Правильное питание.
Впоследствии вступая в брак, молодые люди должны быть готовы и морально и материально стать родителями. Если пара задумается о продолжении рода “здесь и сейчас”, то надо проконсультироваться не только у врача гинеколога, но и у других специалистов. Здоровье родителей – главный ресурс, который нужен будущему ребенку.
Источник
Реабилитация после медицинского аборта – путь к сохранению репродуктивного здоровья женщин
*Импакт фактор за 2018 г. по данным РИНЦ
Читайте в новом номере
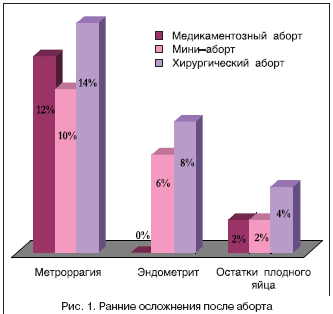
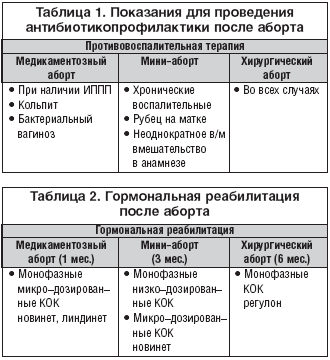
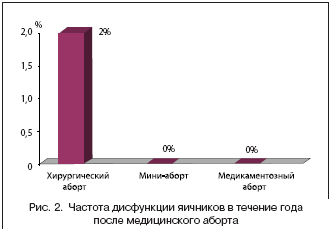
Профилактика абортов – важнейшая составляющая комплекса задач по охране репродуктивного здоровья женщин. Из 210 млн. беременностей, наступающих в мире ежегодно, 46 млн. (22%) заканчиваются медицинским абортом. В нашей стране проблема абортов особенно актуальна, поскольку Россия занимает первое место в мире (в том числе и в странах СНГ) по их числу [9]. На фоне низкой рождаемости из 10 беременностей 7 завершается абортами и только 3 – родами, каждый 10 аборт – у лиц в возрасте до 19 лет [7].Искусственное прерывание нежелательной беременности часто приводит к серьезным, иногда необратимым последствиям, таким как бесплодие, невынашивание, нарушения менструального цикла, рецидивирующие воспалительные заболевания женских половых органов [3,4,7]. Доказано, что дети от матерей с искусственным абортом в анамнезе чаще рождаются в состоянии асфиксии, с нарушениями мозгового кровообращения и другими заболеваниями, что приводит к увеличению детской заболеваемости и смертности [10]. Особенно велика частота осложнений (59,4%) после прерывания первой беременности у молодых женщин [5].Осложнения медицинского аборта составляют около 15–30% в структуре материнской смертности [1]. Экономический ущерб от абортов и связанной с ними гинекологической заболеваемости, а также лечением последующего бесплодия составляет ежегодно более 6млрд. рублей и не имеет тенденции к снижению [3].Снижения неблагоприятного влияния аборта на здоровье и репродуктивную функцию женщины возможно добиться двумя путями: разработкой и внедрением наиболее безопасных методов прерывания беременности, а также адекватной реабилитации женщин после аборта (табл. 2).Современная медицина, помимо традиционного способа прерывания беременности (хирургический аборт или инструментальное выскабливание стенок полости матки), располагает альтернативными методами. Один из них – способ вакуум–аспирации в ранние сроки беременности (мини–аборт), который менее травматичен по сравнению с инструментальным выскабливанием стенок полости матки, но все же является хирургическим вмешательством со всеми возможными при этом осложнениями.Одним из современных наиболее щадящих методов является медикаментозное прерывание беременности ранних сроков путем применения биологически активных веществ. В настоящее время с этой целью применяется мифепристон – таблетированный синтетический стероидный препарат, конкурентный ингибитор прогестерона. Связываясь с прогестероновыми рецепторами, мифепристон блокирует действие прогестерона. При этом восстанавливается чувствительность миометрия к окситоцину, потенциируется действие простагландинов, что усиливает сократительную активность миометрия [2,11].Каким бы щадящим не был способ прерывания беременности, он все равно является серьезной психологической и физической травмой, гормональным стрессом и всегда представляет собой риск серьезных осложнений. Поэтому реабилитация женщин, особенно первобеременных, перенесших искусственный аборт, является очень важной медицинской задачей.Для разработки системы реабилитации женщин после аборта с учетом степени травматичности различных способов медицинского аборта проведено комплексное обследование 150 пациенток, обратившихся для прерывания беременности в первом триместре. В зависимости от метода аборта они составили 3 группы: I группа – 50 женщин, которым с целью прерывания беременности использовался препарат мифепристон; IIгруппа – 50 пациенток, которым прерывание беременности производилось методом вакуум–аспирации (мини–аборт); III группа – 50 пациенток, которым произведен медицинский аборт путем инструментального выскабливания стенок полости матки.Всем женщинам проводилось комплексное обследование до и после аборта с помощью общеклинических, бактериологических, иммуноферментного и морфологического методов исследования. Группы пациенток были идентичны по возрасту, особенностям менструальной функции, наличию экстрагенитальных и гинекологических заболеваний, паритету.Прерывание беременности путем применения мифепристона и вакуум–аспирации осуществлялось до 6 недель, хирургический аборт у большинства (86%) женщин проводился в 6–9 недель, у 14 % – в сроке 10 недель. Беременные основной группы принимали мифепристон в дозе 600 мг за один прием в присутствии врача и препарат поддержки мизопростол 400 мг (2 таблетки) через 36–48 часов после приема мифепристона.Прерывание беременности у 48 (96%) пациенток произошло в среднем через 22–25 ч (25,5±1,9ч), что подтверждено результатами ультразвукового исследования (УЗИ) и определения ХГ в сыворотке крови. Клинически это проявлялось кровянистыми выделениями, более интенсивными в первые 3 дня, чем при обычной менструации. Продолжительность их составляла 5–10 дней (в среднем 7,5±1,6 дня) и не отличалась от таковой во II и III группах. Лишь 5 (10%) женщин отмечали схваткообразные боли внизу живота, требующие приема анальгетических и спазмолитических средств.Наиболее частое количество ранних осложнений после прерывания беременности наблюдалось в случае медицинского аборта путем инструментального выскабливания стенок полости матки. При хирургическом аборте метроррагии возникли в 14% случаев, эндометрит – в 8% случаев, а остатки плодного яйца – в 4% случаев. После мини–аборта метроррагия развилась в 10% случаев, эндометрит – в 6% случаев, а остатки плодного яйца сохранялись в 2% случаев. После проведения медикаментозного аборта метроррагии развились в 12% случаев и остатки плодного яйца наблюдались в 2% (рис. 1).Анализ послеабортных осложнений позволил выделить следующие факторы риска их развития: хронические воспалительные заболевания гениталий, рубец на матке, миома матки, дисфункция яичников, наличие в анамнезе неоднократных внутриматочных вмешательств, юный возраст при первой беременности.Восстановление менструальной функции после медикаментозного прерывания беременности происходило через 28–30 (29,1±1,2) дней, после мини–аборта – через 40–43 (40,2±3,4) дня, после хирургического – через 48–51 (48,2±4,21) день. Фактически после мини – аборта и хирургического аборта наблюдалось отставание начала первой менструации в среднем на 12–14 и 18–21 день соответственно.Изменения гормонального статуса пациенток после прерывания беременности характеризовались в основном увеличением уровня пролактина, снижением уровней эстрадиола и прогестерона. Причем после хирургического аборта изменения гормональной функции гипофизарно–яичниковой системы наблюдались у большего количества женщин (26%), чем в I и II группах (4 и 12% соответственно).Эти данные подтверждены результатами морфологического исследования биоптатов эндометрия, полученных с помощью аспирационной кюретки–пайпель на 7–8–й и 21–23–й дни после прерывания беременности.Гистологическая картина эндометрия на 7–8–й дни после медикаментозного аборта соответствовала пролиферативной фазе цикла. После «мини»–аборта наблюдалось лишь частичное восстановление маточного эпителия с задержкой его пролиферативных изменений в среднем на 14 дней. После инструментального выскабливания стенок полости матки в микропрепаратах определялись только некротизированные фрагменты поверхностного и глубокого эндометрия с первыми признаками частичного восстановления маточного эпителия, а также фрагменты базального слоя эндометрия с воспалительным валиком и единичными железами.Морфологическая картина биоптатов, взятых на 21–йдень после приема мифепристона, характеризовалась полным восстановлением структуры эндометрия, свидетельствовала о прошедшей овуляции (7–й день после овуляции) и иллюстрировала адекватную секреторную фазу цикла. В этот же срок после мини–аборта в пайпель–биоптатах выявлялось значительное отставание перестройки эндометрия, морфологическая картина которого соответствовала лишь пролиферативной фазе (примерно 8–10–й дни нормального менструального цикла). Пайпель–биоптаты после хирургического аборта характеризовались неполной эпителизацией внутренней поверхности матки и воспалительными изменениями в ней, что свидетельствовало о резком замедлении восстановительных процессов эндометрия (на 18–21–й день) по сравнению с таковыми после медикаментозного аборта.Темпы восстановления эндометрия вполне соответствуют минимальной его травме после медикаментозного аборта и максимальной – после инструментального выскабливания стенок полости матки.Сравнительный анализ частоты послеабортных осложнений и особенностей восстановления функции яичников у обследованных пациенток явились основанием для разработки реабилитационных мероприятий, предполагающих профилактику воспалительных осложнений и нарушений менструального цикла. Показания для проведения антибиотикопрофилактики после различных способов прерывания беременности представлены в таблице 1.Профилактика воспалительных осложнений предполагает:•?после медикаментозного аборта – однократное внутримышечное введение цефуроксима в дозе 150 мг в момент появления кровянистых выделений;•?во время мини–аборта однократное внутримышечное введение цефуроксима в дозе 150 мг;•?после хирургического аборта – применение антибиотиков широкого спектра действия в течение 5–10 дней.Клинические наблюдения и экспериментальные данные позволили предложить методику профилактики нарушения репродуктивной системы после аборта. Так как после аборта возникает стрессовое состояние с возбуждением гипоталамо–гипофизарной системы и повышенной выработкой стероидных гормонов – глюкортикоидов и эстрогенов, появляется необходимость снизить возбудимость гипоталамуса и, соответственно, предупредить развития изменений в яичниках и эндометрии. В данном случае рекомендовано использование эстроген–гестагенных оральных контрацептивов, которые способствуют адекватной реабилитации функции гипоталамо–гипофизарной системы и восстановлению репродуктивной функции женщин после аборта. Это особенно важно для подростков и молодых женщин, поскольку прерывание первой беременности, наступившей при недостаточно сформированной репродуктивной системе, очень часто приводит к бесплодию. Особое место в действии КОК определяет гестагенный компонент. Для постабортной реабилитации наиболее приемлем дезогестрел, который является прогестагеном третьего поколения. Дезогестрел обладает высокой прогестагенной активностью при пероральном введении и высокой селективностью. Также следует учесть, что после проведения хирургического аборта доза этинилэстрадиола должна быть не менее 30 мкг для достижения наилучшего терапевтического эффекта.Всем данным требованиям соответствует препарат Регулон (Gedeon Richter), содержащий 30 мкг этинилэстрадиола и 150 мкг дезогестрела. Регулон является монофазным препаратом, обладающим свойством регуляции гипоталамо–гипофизарной системы, т.к. снижает гонадотропную активность. Прием КОК после аборта обеспечивает и 100% контрацепцию, поскольку способность к зачатию может восстановиться уже через 11–14 дней после аборта. Немаловажной особенностью Регулона является противовоспалительное действие и способность содействовать регенерации эндометрия.Регулон назначается в течение 6 месяцев с первого дня после аборта, что необходимо для полноценного восстановления эндометрия и менструального цикла.После проведения мини–аборта и медикаментозного аборта достаточно 20 мкг этинилэстрадиола в сочетании с 150 мкг дезогестрела.Таким образом, использование гормональных контрацептивов после аборта преследует три цели: предупреждение развития постабортных осложнений, возникновения повторной нежелательной беременности на фоне послеабортного стресса и регуляцию менструальной функции.Низкодозированные комбинированные контрацептивы (КОК), содержащие прогестагены третьего поколения, оказывают лечебное и профилактическое действие при различных гинекологических заболеваниях.Кроме того, использование Регулона оказывает положительный эффект при дисменорее и предменструальном синдроме. Применение Регулона способствует увеличению продукции белков, связывающих половые стероиды, в частности, тестостерона, в результате чего наблюдается выраженный антиандрогенный эффект. Поэтому он особенно рекомендуется женщинам с андрогензависимыми изменениями кожи (акне, себорея, гипертрихоз). Регулон хорошо переносится, не вызывает побочных реакций, эффективно регулирует менструальную функцию, надежно предупреждает наступление нежелательной беременности.Одним из этапов реабилитации после прерываний беременности является диспансеризация женщин. Учитывая минимальное влияние на организм пациенток медикаментозного аборта, динамическое наблюдение осуществляется в течение месяца. Женщины, перенесшие мини–аборт без осложнений, должны находиться под диспансерным наблюдением в течение 2–3 месяцев после прерывания беременности. После хирургического аборта динамическое наблюдение пациенток должно проводиться не менее 6 месяцев.Наблюдение пациенток в течение года после медикаментозного аборта не выявило каких–либо нарушений их здоровья, непосредственно связанных с перенесенным вмешательством. Особый интерес представляет факт отсутствия нарушений менструального цикла после медикаментозного и мини–аборта и минимальная их частота после хирургического прерывания беременности (рис. 2).Таким образом, прерывание беременности должно осуществляться в ранние сроки наименее травматичным методом. Правильная организация проведения медицинского аборта и последующая реабилитация женщин даст возможность врачам акушерам–гинекологам сделать аборт максимально безопасным и сохранить репродуктивную функцию женщин.
Литература
1. Гридчик А.Л., Тамазян Г.В. Социальные и медицинские проблемы аборта // Материалы пленума Российской ассоциации акушеров и гинекологов. М. 2000.–С. 66–68.
2. Карева Е.Н., Соловьева Е.В., Кирпичников Н.В., Туманов А.В. К вопросу о механизме абортивного действия простагландинов // Ж. Экспер. и клинич. Фарм.1999.– № 4. – С. 72–76.
3. Краснопольский В.И., Ткачева И.И., Дуб Н.В., Щепатов В.В,, Манухин И.Б. Инфицированный аборт. МОНИИАиГ. Информационно–методическое письмо. 1997.–с.1–4.
4. Краснопольский В.И., Савельева И.С., Белохвостова Ю.Б., Соколова И.И., Ерофеева Л.В. Планирование семьи и репродуктивное здоровье девочек–подростков и молодых женщин //Вестник Росс. Ассоциации акуш. – гинек. 1998г. №1, с. 87–89.
5. Кулаков В.И., Серов В.Н., Барашнев Ю.И., Фролова О.Г. и соавт. Проблема аборта // Руководство по безопасному материнству. М. 2000 .–С. 449–468.
6. Маринкин И.О., Ершов В.Н., Краснопольский В.И., Радзинский В.Е. и соавт. Новые методы профилактики и лечения острых неспецифических послеабортных и послеродовых метроэндометритов. Н. 1995.– С. 3–9.
7. Руководство по охране репродуктивного здоровья. – М., «Триада–Х», 2001. –568 с.
8. Серов В.Н., Стрижаков А.Н., Маркин С.А. Практическое акушерство. М.: Медицина. 1989.–С. 22–24.
9. Хабаров С.В. К эпидемиологии медицинского аборта на селе // Материалы Пленума Российской ассоциации акушеров и гинекологов. М. 2000.– с. 296–298.
10. Чередниченко Т.С. Беременность и роды у женщин после искусственного прерывания первой беременности и здоровье их младенцев. М. 2001. Автореф. диссерт. К.м.н.
11. Cameron IT, Michie AF, Baird DT Therapeutic abortion in early pregnancy with antiprogestogen RU 486 alone or in combination with prostoglondin analogue (gemeprost) Contraception 1986,34 459–468.
Источник