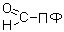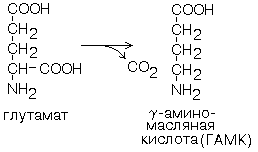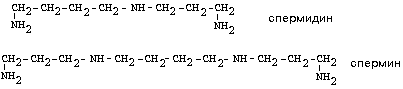33. Переаминирование аминокислот, его механизм, биологическое значение. Процессы дезаминирования и декарбоксилирования аминокислот.
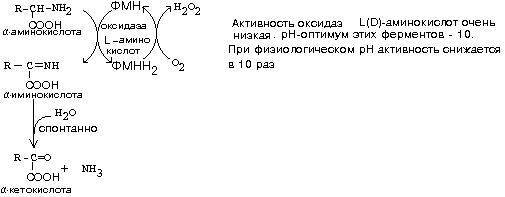
ДЕЗАМИНИРОВАНИЕ АМИНОКИСЛОТУ человека происходит в основном путем окислительного дезаминирования. Эти реакции протекают с помощью двух ферментов:- оксидаза Д-аминокислот- оксидаза L-аминокислот
Эти ферменты обладают групповой стереоспецифичностью. Оксидазы отнимают протоны и электроны от аминокислот с помощью такого же механизма, как и оксидазы, обеспечивающие дезаминирование биогенных аминов. Эти ферменты являются флавопротеинами и содержат в качестве простетической группы ФАД или ФМН:На первой стадии образуется иминокислота, а затем, после спонтанного гидролиза образуется альфа-кетокислота.Кроме оксидаз имеется еще один фермент, катализирующий окислительное дезаминирование глутаминовой кислоты — глутамат-дегидрогеназа (глутаматДГ).Этот фермент является НАД-зависимым и обладает высокой активностью (как и другие НАД-зависимые дегидрогеназы). В этом его отличие от оксидаз аминокислот, которые медленно превращают аминокислоты в физиологических условиях (поэтому в клетке сохраняется большинство аминокислот). Так как глутамат-ДГ является никотинамидной, то отнимаемые протоны и электроны не передаются сразу на кислород, а транспортируются по полной цепи МтО с образованием воды и параллельным образованием трех молекул АТФ.
Глутамат-ДГ обладает высокой активностью и этим отличается от МАО и ДАО. Глутамат-ДГ является регуляторным ферментом — он ингибируется избытком АТФ, и активируется избытком АДФ.
БИОЛОГИЧЕСКОЕ ЗНАЧЕНИЕ РЕАКЦИЙ ДЕЗАМИНИРОВАНИЯ1. Реакции дезаминирования необратимы, как и реакции декарбоксилирования — дезаминирование тоже может играть роль первого этапа на путях распада аминокислот. 2. Один из непосредственных продуктов дезаминирования -конечный продукт метаболизма аммиак. Это токсическое вещество. Поэтому клетки должны затрачивать энергию, чтобы обезвредить аммиак до безвредных продуктов, которые выводятся из организма.3. Другой продукт реакции дезаминирования — альфа-кетокислота.
Все образующиеся альфа-кетокислоты легко расщепляются дальше до СО2 и Н2О (например, аланин превращается в ПВК (путем дезаминирования; аспартат — в ЩУК; глутаминовая кислота — в альфа-кетоглутаровую). Большинство альфа-кетокислот тем или иным путем превращаются в кислоты, которые являются промежуточными метаболитами ЦТК:- в альфа-кетоглутаровую; — в янтарную;- фумаровую; — щавелево-уксусную. Все эти метаболиты могут в организме трансформироваться в углеводы, перед этим превращаясь в ПВК. Поэтому большинство аминокислот относится к группе, которая называется ГЛЮКОГЕННЫМИ АМИНОКИСЛОТАМИ (их 17). Только 3 аминокислоты не могут превращаться в ПВК, но превращаются в Ац-КоА — КЕТОГЕННЫЕ АМИНОКИСЛОТЫ: лейцин, лизин, триптофан). Они могут прямо трансформироваться в жирные кислоты или в кетоновые тела.
Метаболические пути, в которые вступают аминокслоты после дезаминирования, уже не являются собственно путями метаболизма аминокислот, а являются универсальными и для аминокислот, и для углеводов, и для жиров.
Д 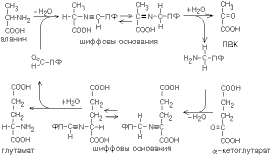
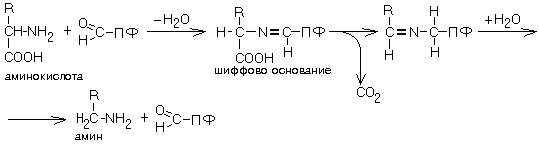
Аминокислота соединяется с активным центром фермента, в состав которого входит альдегидная группа ПФ. Образуются Шиффовы основания (альдимины и кетимины). В результате СООН-группа становится лабильной и отщепляется в виде СО2. Далее происходит гидролиз до соответствующего амина. Эта реакция необратима. Отнятие СО2 происходит без окисления. Субстратная специфичность декарбоксилаз очень разная.
1. ГЛУТАМАТДЕКАРБОКСИЛАЗА — высокоспецифичный фермент. Работает в клетках серого вещества головного мозга. Катализирует реакцию превращения глутаминовой кислоты в гамма-аминомасляную кислоту (ГАМК).ГАМК является медиатором тормозных импульсов в нервной системе. ГАМК и ее аналоги применяются в медицине как нейротропные средства для лечения эпилепсии и других заболеваний.
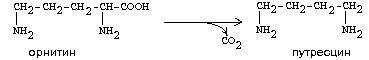
2. ОРНИТИН-ДЕКАРБОКСИЛАЗА — высокоспецифичный фермент. Катализирует превращение орнитина в путресцин:
Образующийся ПУТРЕСЦИН (диаминобутан) является трупным ядом. В результате присоединения остатков пропиламина из путресцина могут образоваться СПЕРМИН и СПЕРМИДИН, содержащие 3 (у спермина) или 4 (у спермидина) имино- или аминогруппы.
Спермин и спермидин относятся к группе биогенных полиаминов. Введение полиаминов в организм снижает температуру тела и кровяное давление. Полиамины принимают участие в процессах пролиферации клеток и роста тканей, а также в регуляции биосинтеза белка. Они являются ингибиторами некоторых ферментов, в том числе протеинкиназ.
Орнитиндекарбоксилаза — это первый фермент на пути образования путресцина и остальных полиаминов, это регуляторный фермент процесса.
ПЕРЕАМИНИРОВАНИЕ (трансаминирование), обратимый перенос аминогруппы из молекулы одного орг. соед. в молекулу другого. Наиб. роль переаминирование играет в биохимии в процессах метаболизма азотистых оснований в тканях животных и растений.Переаминирование аминокислот может происходить и вне клетки в присут. пиридоксаль-5′-фосфата, однако скорость р-ции в 106 раз меньше. Специфичность действия определяется пространств, структурой субстрата, положением ионогенных групп белка, осуществляющих кислотно-основной катализ, и геометрией связывания субстрата.Нарушение нормального течения переаминирования в организме наблюдается при патологич. состояниях, напр. при инфаркте миокарда, заболеваниях печени. Контроль концентрации аминотрансфераз используется в этих случаях как ср-во диагностики. Переаминирование в организме подавляется противотуберкулезными лек. ср-вами (изониазидом, циклосерином и др.), а также при В6-авитаминозе.
ДЕЗАМИНИРОВАНИЕ (деаминирование), удаление группы NH2 из молекул орг. соединений. Сопровождается замещением аминогруппы на др. группу или образованием кратной связи. Осуществляется под действием HNO2, нитрозилсерной к-ты, N2O3, N2O4, H2O, H2, а также ферментов. Наиб. универсальный метод дезаминирования аминов — взаимод. их с HNO2. Сущность метода состоит в обработке кислых водных р-ров аминов нитритом К или Na, в результате чего образуются соли диазония (см. Диазотирование, Диазосоединения). В случае алифатич. аминов эти соли неустойчивы и разлагаются с выделением N2 и образованием карбкатиона, к-рый взаимод. с нуклеоф. агентами среды (вода, анионы и др.) или стабилизируется с образованием олефина.
ДЕКАРБОКСИЛИРОВАНИЕ, элиминирование СО2 из карбоксильной группы карбоновых к-т или карбоксилатной группы их солей. Осуществляют обычно нагреванием в присут. к-т или оснований. Декарбоксилирование монокарбоновых насыщенных к-т протекает, как правило, в жестких условиях. Так, прокаливание ацетата Na с избытком натронной извести приводит к отщеплению СО2 и образованию метана: CH3COONa + NaOH 001= CH4 + Na2CO3.
Источник
Параграф 64. переаминирование
Автор текста – Анисимова Елена Сергеевна.
Авторские права защищены. Продавать текст нельзя.
Курсив не зубрить.
Замечания можно присылать по почте: exam_bch@mail.ru
https://vk.com/bch_5
ПАРАГРАФ 6 4:
«Переаминирование».
Г р у п п ы а т о м о в.
Вы можете встретить разные сочетания атомов.
-NH2 называется аминогруппой.
ОН – гидроксильная группа (от: Н – гидрогениум, а О – оксигениум) или спиртовая.
Атом О, соединенный с атомом углерода двойной (=) связью, называется кето/группой (если С не является первым: =О при первом С является альдегидной группой).
Если с одним атомом С соединены =О и группа ОН, то НО, С и О являются карбоксильной группой, структурная формула которой: О=С–ОН;
не путайте её с группой С-О-О-Н органических перекисей.
Если с одним и тем же атомом С соединены NH2 и =О, то они являются амидной группой.
К л а с с ы веществ.
Вещества с разными функциональными группами относятся к разным классам.
Если в веществе есть СООН группа (карбоксильная), то оно относится к классу карбоновых кислот.
Если в формуле кислоты есть кетогруппа, то кислота является кетокислотой
(вспоминайте примеры кетокислот: кетоглутарат, пируват, оксалоацетат).
Если в формуле кислоты присутствует аминогруппа, то кислота является аминокислотой (глутамат – это «глутарат с аминогруппой», аспартат – это сукцинат с аминогруппой т.д).
Здесь должна быть таблица
«Функциональные г р у п п ы и к л а с с ы» .
Но пока она в отдельном файле.
Если в формуле аминокислоты аспартата зачеркнуть NH2 (аминогруппу) и написать =О (кетогруппу), то получится формула кетокислоты оксалоацетат (ОА).
Формула аланина при аналогичной замене превращается в формулу пирувата,
а формула глутамата – в формулу ;-кетоглутаРата (КГ):
Здесь должна быть таблица, показывающая формулы реакции.
Но пока она в отдельном файле.
В организме существуют соответствующие реакции:
аминокислоты могут превращаться в кетокислоты и наоборот.
64. 1. Переаминирование.
Один из способов превратить аминокислоту в кетокислоту называется пере/аминированием (ПА);
другой способ см. в п. 65 – дез/аминирование глутамата.
При ПА аминокислота должна вступить в реакцию с кетокислотой.
При этом аминокислота и кетокислота как бы обмениваются группами (амино- и кето-): аминокислота отдает свою аминогруппу (кетокислоте),
получает кетогруппу (от кетокислоты) вместо аминогруппы
и превращается в кетокислоту.
Кетокислота отдает кетогруппу (аминокислоте),
получает аминогруппу (от аминокислоты) вместо кетогруппы
и превращается в аминокислоту.
Определение:
Переаминирование – это реакция между аминокислотой и кетокислотой,
в результате которой аминокислота превращается в кетокислоту,
а кетокислота – в аминокислоту.
Аминокислота аспартат при ПА превращается в кетокислоту оксалоацетат,
аминокислота аланин при ПА превращается в кетокислоту пируват,
а аминокислота глутамат – в кетоглутарат.
Реакции ПА обратимы, и это очень важно почему – говорится далее.
Чаще всего Асп или Ала вступают в реакцию с ;-кетоглутаратом
или, наоборот, глутамат вступает в реакцию с оксалоацетатом или пируватом:
Асп + КГ ; ОА + Глу,
Ала + КГ ; Пир + Глу.
64. 2. Ферменты переминирования.
Ф е р м е н т ы , которые катализируют ПА, относятся к классу трансфераз («переносчиков»),
к подклассу амино/трансфераз (АТ).
АТ, катализирующая ПА аспартата (Асп + КГ ; ОА + Глу),
называется аспартат/амино/трансферазой (сокращенно – АсАТ);
обратную реакцию (ОА + Глу ; Асп + КГ) тоже катализирует АсАТ.
АТ, катализирующая ПА аланина (Ала + КГ ; Пир + Глу) ,
называется аланин/амино/трансферазой (АлАТ);
обратную реакцию Пир + Глу ; Ала + КГ тоже катализирует АлАТ.
Аминотрансферазы работают с участием кофермента пиридоксаль/фосфата (ПФ),
в состав которого входит витамин В6.
Без В6 и ПФ АТ не работают и реакции ПА не протекают (с нужной скоростью),
из-за чего многие процессы нарушаются и что приводит к появлению последствий дефицита В6 и признаков гиповитаминоза В6.
ПА – первый этап в непрямом дез/аминировании аминокислот (см. п. 65),
образующихся в основном при распаде белков (протеолизе).
он происходит перед прямым дез/аминированием глутамата;
относится к катаболическим процессам.
ПА – второй этап в непрямом восстановительном аминировании,
приводящем к синтезу аминокислот для синтеза белков,
происходит после прямого аминирования кетоглутарата,
относится к анаболическим процессам.
Здесь есть таблица
«64. 3. Переаминирование с а с п а р т а т о м»,
показывающая формулы реакции, но пока она в отдельном файле.
Здесь есть таблица
«64. 4. Переаминирование с а л а н и н о м»,
показывающая формулы реакции, но пока в отдельном файле.
64. 5.
Реакции ПА обратимы. Разберем оба направления.
Направление процесса «аминокислота в кетокислоту»:
аминокислота + кетоглутарат ; кетокислота + глутамат.
(Глутамат конечно тоже аминокислота, но тут он вспомогательную роль играет).
64. 5. 1. И с т о ч н и к и с у б с т р а т о в для ПА.
1. Источником аминокислот для ПА является распад белков.
Если человек ест белковую пищу и получает белки пищи,
то АК образуются при распаде белков пищи,
а если не ест, то распадаются белки самого организма
(белки крови, печени, мышц и т.д.),
что приводит к их дефициту:
дефицит белков плазмы приводит к отекам,
дефицит белков мышц приводит к мышечной слабости и т.д.;
при длительном голодании разрушаются белки сердца и ряд других – это приводит к смерти.
2. Источником кетоглутарата для ПА является ЦТК:
кетоглутарат образуется в одной из реакций ЦТК,
после чего подвергается действию не фермента ЦТК,
а действию ферментов пере/аминирования (амино/трансфераз) –
таким образом, КГ как бы извлекается из ЦТК для другого процесса.
64.5. 2. Ч т о происходит с п р о д у к т а м и ПА?
Первый продукт ПА – кетокислоты.
Оксалоацетат, пируват и другие кетокислоты, образованные при ПА (из Асп, Ала и т.д.),
могут использоваться для синтеза глюкозы в печени
(другими словами, являются субстратами для глюко/нео/генеза: ГНГ в п.33).
Синтез глюкозы за счет ПА и ГНГ необходим организму при отсутствии других источников глюкозы,
то есть при отсутствии углеводной пищи в течение 12 часов (в среднем) и далее
(примерно на 12 часов хватает резерва глюкозы – гликогена печени;
любителям алкоголя, лекарств – гликогена не хватит на 12ч).
Если через 12 часов отсутствия углеводной пищи
(злаки, картофель, овощи, фрукты, кондитерские изделия)
ПА и ГНГ не заработают, то человек может умереть.
Потому что [глюкозы] в крови снизится (возникнет гипогликемия),
что приведет к появлению слабости, предобморочному состоянию,
затем (если не принять мер для увеличения гликемии, то есть не съесть углеводы или не сделать инъекцию раствора глюкозы)
к обмороку, гипогликемической коме и смерти.
Это связано с тем, что без глюкозы погибают нейроны и эритроциты
(т.к. они нуждаются в глюкозе для выработки АТФ,
и без глюкозы не могут получить достаточное количество АТФ).
ГНГ – это важный, но не единственный путь для кетокислот, полученных при ПА из АК.
Второй путь использования кетокислот – это их поступление в ЦТК.
Есть два варианта превращений кетокислот в ЦТК.
Первый вариант
– превращение аминокислот в ОКСАЛОАЦЕТАТ
и многократное использование в ЦТК
(в первой реакции ЦТК ОА вступает в реакцию с ацетилКоА,
превращаясь в цитрат,
а в последней реакции оксалоацетат образуется снова
и может вступать в реакцию с новой молекулой ацетилКоА).
Этот путь относится к анаплеротическим реакциям,
то есть к таким, которые позволяют восполнить или увеличить количество метаболитов ЦТК
(это способствует синтезу АТФ в клетке,
синтезу АК из метаболитов ЦТК и далее — белков).
Второй вариант
превращений углеводородных скелетов аминокислот (не только кетокислот) в ЦТК –
разрушение до СО2, то есть катаболизм АК.
Этот вариант позволяет клетке получить больше АТФ,
поэтому протекает при потребности клетки в АТФ
(когда для выработки АТФ не хватает углеводов или липидов) –
спасает клетку от смерти.
Избыточные АК тоже подвергаются катаболизму в ЦТК.
Как АК разрушаются до СО2?
Некоторые АК превращаются в ацетилКоА, не превращаясь в оксалоацетат (см. далее о кетогенных в п. 67),
далее ацетилКоА поступает в ЦТК, где превращается в 2СО2 (а водород переносится на коферменты для переноса в ДЦ и выработки АТФ).
Большинство АК могут превращаться в оксалоацетат (см. в № 67 о гликогенных АК). Катаболизм ОА происходит так:
1) ОА превращается в ФЕП (эту реакцию встречали в ГНГ п.33),
2) ФЕП превращается в пируват (эту реакцию встречали в гликолизе п.32),
3) пируват превращается в ацетилКоА под действием ПДГ-комплекса с участием 5 витаминов,
4) ацетилКоА поступает в ЦТК и превращается в 2СО2, отдавая водород коферментам для ДЦ и АТФ.
Второй продукт ПА – глутамат.
Глутамат, образованный при ПА (из КГ) и не только, вступает в реакции, которые называются прямым окислительным дез/аминированием (ПОД) – см. № 65.
В результате ПОД глутамат превращается в кетоглутарат и аммиак.
КГ может вступать в ПА с новой АК или «вернуться» в ЦТК – то есть особого расхода КГ и истощения ЦТК для ПА не происходит (но если в ПА вступает большее количество АК, то потребуются новые «порции» КГ).
Аммиак очень токсичен (повышение его концентрации может привести к смерти), поэтому аммиак нужно обезвреживать; для спасения от аммиака нужна здоровая печень и отсутствие любви к алкоголю – см. п 66.
Итог – ПА дает:
1) полезный продукт кетокислоту, которая спасает от гипогликемии (и от дефицита АТФ), и
2) ядовитый продукт аммиак, который приходится обезвреживать, чтобы не умереть.
В этом направлении реакции ПА идут или тогда,
1) когда нужна глюкоза (при голоде, повышенных нагрузках, дефиците углеводов в пище, некоторых заболеваниях), или тогда,
2) когда есть избыток аминокислот (при повышенном распаде белков организма при переедании белков или при заболеваниях, сопровождающихся разрушением клеток и повышенным распадом белков организма).
Это направление ПА приводит к разрушению АК, то есть является этапом в катаболизме АК (см. п. 65) и белков.
Первый этап непрямого окислительного дез/аминирования. Для успешного выполнения функций ПА нужен В6.
Тут надо добавить таблицу
«АК превращаются в кетокислоты (или другие метаболиты ЦТК, не только путем ПА), когда:»
Но пока она в отдельном файле.
64.6.
Направление процесса: кетокислота + глутамат ; аминокислота + кетоглутарат.
64. 6. 1. И с т о ч н и к и с у б с т р а т о в.
Источником кетокислот (пирувата, оксалоацетата) является глюкоза: пируват образуется при гликолизе, а ОА образуется из пирувата (реакцию встречали в ГНГ, нужен витамин биотин).
Источником глутамата может быть распад белков и другие процессы (см. п 65 и/или 67).
64. 6. 2. Что происходит с продуктами этого направления ПА?
Аминокислота может использоваться для синтеза белков или других веществ.
Кетоглутарат может поступить в ЦТК или снова превратиться в глутамат в результате прямого восстановительного аминирования (см № 65).
При превращении КГ в Глу используется аммиак, что является одним из путей снижения [аммиака] и спасения от его токсичности – п.66.
Это направление ПА приводит к образованию АК, то есть является синтезом некоторых АК (Асп, Ала), анаболическим процессом. См. в п. 65 о непрямом восстановительном аминировании: ПА является вторым этапом этого процесса.
Значение ПА (выше). Определяется тем, что позволяет избавиться от субстратов и получить продукты.
Аминотрансферазы в к л и н и к е.
Определение активности АсАТ и АлАТ в сыворотке применяется для (энзимо)диагностики повреждений СЕРДЦА И ПЕЧЕНИ.
Если АлАТ больше, чем АсАТ, то это указывает на патологию печени (гепатит или др.).
Если АсАТ больше, чем АлАТ, то это указывает на патологию сердца (в том числе на вероятность инфаркта);
при некоторых патологиях печени АсАТ тоже бывает больше, чем АлАТ.
Определение активности только АлАТ или только АсАТ не позволяет ставить диагноз, нужно определять активность обоих ферментов и их соотношение.
Источник