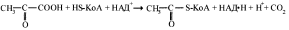Окислительное декарбоксилирование а-кетокислот. Механизм и регуляция окислительного декарбоксилирования пировиноградной кислоты. Роль витаминов.
Реакция окислительного декарбоксилирования карбоновых кислот заключается в отщеплении от молекулы карбоновой кислоты карбоксильной группы при нагревании до 260—300 o С, в присутствии окислителя и хлорид-анионов, протекающем согласно следующей общей схеме: R-C(O)OH —> R-H + CO2
А-кетокислота – это аминокаслота, в которой амино-группа замещена на кето-группу в а-положении. В результате окислительного декарбоксилирования пирувата образуются ацетил- КоА, восстановленный НАД и диоксид углерода:
Эта схема представляет собой суммарный результат многостадийного процесса, который катализируется сложной ферментной системой — пируватдегидро- геназным комплексом. Комплекс содержит три фермента: пируватдекарбоксила- зу, ацетилтрансферазу и дегидрогеназу дигидролипоевой кислоты. Кроме того, в реакциях участвуют пять коферментов: НАД, ФАД, тиаминдифосфат, липоевая кислота и кофермент А (КоА).
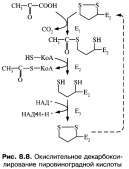
Декарбоксилирование пирувата происходит при прямом участии тиаминди- фосфата (производное витамина В2 ): в ходе реакции к атому углерода тиазолового кольца.
Второй фермент комплекса — дигидролипоат-ацетилтрансфераза — катализирует перенос ацетильного остатка, соединенного с его (фермента 2) собственной простетической группой, на КоА; при этом получаются дигидролипоевая кислота (в составе ацетилтрансферазы) и ацетил-КоА.
Третий фермент — дегидрогеназа дигидролипоевой кислоты (ЕЗ). Акцептором водорода в реакции служит НАД. В результате дегидрирования дигидролипоевая кислота превращается в начальную форму — дегидролипоевую кислоту, и пируватдегидрогеназный комплекс может реагировать с очередной молекулой пирувата. Дигидролипоилдегидрогеназа содержит в качестве кофермента ФАД, который служит промежуточным акцептором водорода.
Таким образом, в окислительном декарбоксилировании пирувата участвует пять коферментов. Три из них — тиаминпирофосфат, липоевая кислота и ФАД — прочно связаны с ферментами комплекса, а два других — КоА и НАД — находятся в свободно растворенном состоянии и служат акцепторами главных конечных продуктов — ацетильного остатка и атомов водорода. Ацетильный остаток затем окисляется в цитратном цикле, а водород с НАДН поступает в цепь переноса электронов и протонов.
Дата добавления: 2016-12-08 ; просмотров: 3522 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Источник
42.Окислительное декарбоксилирование а-кетокислот. Механизм и регуляция окислительного декарбоксилирование пировиноградной кислоты.
Окислительное декарбоксилирование а-кетокислот в карбо-новые кислоты с уменьшенной на один атом цепью углеродных атомов осуществляется при участии системы ферментов. Через ряд каталитических превращений пировиноградная кислота, являющаяся одним из продуктов углеводного обмена ( в частности гликолиза), в виде продукта ее декарбоксилирова-ния и дегидрирования — высоко макроэргического ацетил — КоА — вводится в цикл трикарбоновых кислот в звене превращений ща-велевоуксусной кислоты в лимонную кислоту и в конечном счете окисляется в двуокись углерода и воду. Первичное расщепление пировиноградной кислоты с отделением двуокиси углерода осуществляет ТДФ. В последующих превращениях образовавшегося ацильного остатка окислительным агентом служит а-липоевая кислота, которая сама при этом подвергается восстановительному ацилированию при каталитическом действии пируватдегидрогеназы в 6-ацетилдигидролипоевую кислоту. Аминокислоты декарбоксилируют только а-кетокислоты. Триметилпировиноградная кислота не декарбоксилируется. Установлено, что а-кетокислоты, воз-никшие в процессе дезаминирования а-аминокислот, могут подвергаться в животных тканях д е к а р-боксилированию и одновременному окислению в жирную кислоту. Так же как а-кетокислоты, а, р-ненасыщенные кетоны не взаимодействуют с надкислотами, поскольку С С-связь в этом случае носит электрофильный, а не нуклеофильный характер. Тидрокси — и а-кетокислоты не расщепляются под действием Н1О4, но эта реакция идет с тетраацетатом свинца, На02 в щелочной среде и другими реагентами. Такие реакции представляют собой окислительное декарбоксилирование. Окисление пирувата до ацетил-КоА происходит при участии ряда ферментов и коферментов, объединенных структурно в мультиферментную систему, получившую название «пируватдегидрогеназный ком-плекс». На I стадии этого процесса пируват теряет свою карбоксильную группу в результате взаимодействия с тиа-минпирофосфатом (ТПФ) в составе активного центра фермента пируватдегидрогеназы (E1). На II стадии оксиэтильная группа комплекса E1–ТПФ–СНОН–СН3 окисляется с образованием ацетильной группы, которая одновременно переносится на амид липоевой кислоты (кофермент), связанной с ферментом дигидро-ли-поилацетилтрансферазой (Е2). Этот фермент катализирует III стадию – перенос ацетильной группы на коэнзим КоА (HS-KoA) с образованием конечного продукта ацетил-КоА, который является высокоэнергетическим (макроэргическим) соединением. На IV стадии регенерируется окисленная форма липоамида из восста-новленного комплекса дигидролипоамид–Е2. При участии фер-мента дигидролипоилдегидрогеназы (Е3) осуществляется перенос атомов водорода от восстановленных сульфгидрильных групп дигидролипоамида на ФАД, который выполняет роль простетиче-ской группы данного фермента и прочно с ним связан. На V стадии восстановленный ФАДН2 дигидро-липоилдегидрогеназы передает водород на кофермент НАД с образованием НАДН + Н+. Процесс окислительного декарбоксилирования пирувата происходит в матриксе митохондрий. В нем принимают участие (в составе сложного мультиферментного комплекса) 3 фермента (пируватдегидрогеназа, ди-гидролипоилацетилтрансфераза, дигидролипоилдегидрогеназа) и 5 кофер-ментов (ТПФ, амид липоевой кислоты, коэнзим А, ФАД и НАД), из которых три относительно прочно связаны с ферментами (ТПФ-E1, ли-по-амид-Е2 и ФАД-Е3), а два – легко диссоциируют (HS-KoA и НАД).
ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПВК
Окислительное декарбоксилирование пировиноградной кислоты — многостадийный процесс, который катализирует пируватдегидрогеназный комплекс — митохондриальный мультиферментный комплекс, соединенный с внутренней мембраной со стороны матрикса. ПВК поступает к комплексу из матрикса, и туда же освобождаются продукты реакции.
Пируватдегидрогеназный комплекс включает три фермента (пируватдегидрогеназа (Е1), ацетилтрансфераза (Е2), дегидрогеназа дигидролипоевой кислоты (Е3)) и пять коферментов (НАД+, ФАД, тиаминпирофосфат, липоевая кислота, кофермент А (рис. 36)).
Тиаминпирофосфат связан с пируватдегидрогеназой (Е1), липоевая кислота — с ацетилтрансферазой (Е2), ФАД — с дегидрогеназой дигидролипоевой кислоты (Е3). Кофермент А и НАД+ находятся в свободно растворенном состоянии.
В состав пируватдегидрогеназного комплекса входит примерно по три десятка молекул Е1 и Е2 и 10 молекул Е3. Комплекс работает как конвейер: промежуточные продукты не освобождаются в раствор, а передаются от фермента к ферменту.
Первую реакцию (рис. 37) катализирует Е1, субстратами являются ПВК и дегидролипоевая кислота, являющаяся простетической группой Е2. От ПВК отщепляется карбоксильная группа и образуется СО2, а ацетильный остаток соединяется с атомом серы липоевой кислоты в составе ацетилтрансферазы. Образуется ацетиллипоат-Е2.
Во второй реакцииацетилтрансфераза (Е2) катализирует перенос ацетильного остатка, соединенного с его простетической группой, на коэнзим А. Продукты этой реакции — дигидролипоевая кислота в составе Е2 и ацетил-KоА.
В третьей реакциипроисходит дегидрирование дигидролипоевой кислоты в составе ацетилтрансферазы при воздействии фермента Е3 (дегидрогеназа дигидролипоевой кислоты), содержащего ФАД. ФАД передает водород на НАД + . Образуются НАДН+Н + и дегидролипоевая кислота в составе Е2. Последний фермент снова вступает в окислительное декарбоксилирование ПВК.
Ацетил-KоА (продукт второй реакции) затем окисляется в цикле Кребса. Водород с НАДН (продукт третьей реакции) поступает в дыхательную цепь, где образуется АТФ.
Энергетический выход окислительного декарбоксилирования пирувата – 3 АТФ.
Суммарное уравнение процесса:
СH3-CО-COOH + HS-KoA + НАД + ® СH3-CО-S-KoA + НАДН + Н + + СО2.
Схема окислительного декарбоксилирования пирувата
Источник
ДЕКАРБОКСИЛИРОВАНИЕ
ДЕКАРБОКСИЛИРОВАНИЕ — процесс отщепления двуокиси углерода (CO2) от органических кислот или аминокислот. В биол, системах существенное значение — биохимическое и физиологическое — имеет Д. аминокислот и кетокислот. Реакция Д. может составлять часть общего механизма превращения аминокислот, в результате чего образуются биогенные амины, обладающие высокой фармакологической активностью.
Д. аминокислот является одним из основных путей промежуточного обмена аминокислот у всех организмов. В зависимости от хим. природы аминокислоты в результате Д. образуются биогенные амины (см.) или новые бета-, и гамма-монокарбоновые аминокислоты. Реакции Д. катализируются специфическими ферментами — декарбоксилазами (см.) и протекают по следующей схеме:
Ферментативному Д. подвергаются только L-стереоизомеры аминокислот; исключение составляет мезо-альфа, эпсилон-диаминопимелиновая к-та, в к-рой содержится два стереоизомерных атома углерода, один находится в L-, а другой в D-конфигурации. В организме могут происходить сопряженные реакции Д. и переаминирования (см.) или реакции Д. и дезаминирования (см.) лизина, аргинина и их производных. Так, у бактерий Pseudomonas обнаружен фермент, катализирующий окислительное превращение L-лизина до дельта-аминовалериановой к-ты, CO2 и NH3:
Реакция Д. аминокислот в животных тканях не является количественно преобладающей реакцией обмена аминокислот, о чем свидетельствует относительно низкая активность декарбоксилаз в их тканях и сравнительно небольшое количество субстратов для Д. Однако продукты Д. имеют большое физиол, значение, биогенные амины, напр., физиологически активны даже в очень низких концентрациях. Впервые К. М. Розанов в 1936 г. показал образование гистамина в животных тканях путем Д. гистидина. В тканях животных интенсивно протекает Д. диоксифенилаланина (см.) с образованием дофамина (окситирамина), который является, по современным представлениям, предшественником норадреналина и адреналина в организме животных. Гистамин понижает кровяное давление, а тирамин, триптамин и особенно 5-окситриптамин (серотонин) обладают гипертензивным действием. Высокой фармакол. активностью обладают некоторые производные этих аминов (адреналин, норадреналин, эфедрин, холин и др.). Ряд данных свидетельствует о повышении кровяного давления при нарушении кровообращения в почках (ишемия и др.) в связи с накоплением в почечной ткани аминов, для окисления которых необходим кислород. Предполагается, что некоторые расстройства психической деятельности обусловлены интоксикацией организма биогенными аминами, образовавшимися в тканях. Т. о., процессы Д. аминокислот в организме, возможно, участвуют в регуляции некоторых физиол, процессов. Кроме того, продукты Д. аминокислот — таурин, бета-аланин и другие необходимы для биосинтеза ряда сложных соединений, выполняющих специфические биол, функции. Ниже представлены уравнения наиболее распространенных реакций Д. аминокислот и их производных в организме животных и человека.
В животных тканях доказано наличие фермента декарбоксилазы ароматических L-аминокислот (КФ 4.1.1.28), катализирующего Д. почти всех ароматических аминокислот.
Ортотирозин, метатирозин и альфа-метилпроизводные триптофана, тирозина и ДОФА также декарбоксилируются этим ферментом. Ферментные препараты из мозгового слоя надпочечников и почек крыс не катализируют, однако, Д. триптофана и тирозина, но декарбоксилируют ДОФА. В тучных клетках найден особый фермент, катализирующий, по-видимому, Д. гистидина. Имеются данные, что триптофан декарбоксилируется ферментными препаратами из почек лишь после окисления его до 5-окситриптофана и что именно 5-окситриптофан является субстратом для Д., в результате к-рого образуется физиологически активный 5-окситриптамин (серотонин).
Большое физиол. значение для человека и животных имеет Д .L-глутамино-вой к-ты (см. Глутаминовая кислота). Открытие гамма-аминомасляной к-ты (ГАМК) последовало за обнаружением в гомогенатах мозга L-глутаматдекар-боксилазы (КФ 4.1.1.15), катализирующей Д. L-глутамата с образованием гамма-аминомасляной кислоты.
Есть основания считать, что ГАМК относится к числу передатчиков нервных импульсов. Кроме того, ГАМК может переаминироваться с пировиноградной, альфа-кетоглутаровой и, возможно, рядом других кетокислот с образованием соответствующей аминокислоты и полуальдегида янтарной к-ты; окисление последнего до янтарной к-ты обеспечивает функционирование обходного пути окисления L-глутами-новой к-ты, минуя альфа-кетоглутаровую к-ту. На схеме показано сопряжение двух путей окисления L-глутамино-вой к-ты с циклом Трикарбоновых к-т (см. Трикарбоновых кислот цикл).
Для митохондрий мозга именно L-глутаминовая к-та, а не глюкоза является основным субстратом дыхания. В этой связи обходной путь превращения L-глутаминовой к-ты с участием глутаматдекарбоксилазы приобретает большое физиол, значение. По полученным на высших растениях данным В. Л. Кретовича (1972), регулированию системы глутаминовая к-та ГАМК + CO2 принадлежит существенная роль в общем процессе регуляции содержания в клетке глутаминовой к-ты и глутамина, являющегося исходным веществом для биосинтеза многих жизненно важных для растительного организма соединений. Вероятно, что такую же роль Д. L-глутаминовой к-ты играет в организме животных и человека.
Процесс Д. широко распространен у микроорганизмов. При гниении белков образование аминов вызывается Д. различных аминокислот под действием бактериальных декарбоксилаз (см. Гниение).
Значительных достижений в исследовании Д. аминокислот у микроорганизмов добились советские исследователи. С. Р. Мардашев в 1947 г. из клеток бактерии Pseudomycobacterium n. sp. выделил специфическую декарбоксилазу, отщепляющую CO2 от бета-COOH-группы L-аспарагиновой к-ты с образованием a-аланина. В 1950 г. в той же лаборатории был выделен вид Micrococcus п. sp., содержащий декарбоксилазу, специфичную в отношении L-гистидина. Используя эти бактерии, С. Р. Мардашев с сотр. разработал быстрый и точный метод определения аспарагиновой к-ты и гистидина в белках. Д. L-аспарагиновой к-ты является уникальной реакцией, поскольку при этом декарбоксилируется бета-COOH-, а не альфа-COOH-группа, как это обычно происходит при Д. аминокислот.
Ферментные препараты аспартат-бета-декарбоксилазы (аспартат-1-декар-боксилазы; КФ 4.1.1.11) были получены из ряда микроорганизмов, в т. ч. и из Achromobacter; в последнем случае фермент был получен в кристаллическом состоянии. Этот фермент активируется не только пиридоксаль-5′-фосфатом, что характерно для декарбоксилаз аминокислот, но и каталитическими количествами альфа-кетокислот.
Реакции Д. аминокислот широко распространены также у высших зеленых растений. Важно отметить, что реакции Д. у растений имеют прямое отношение к биосинтезу ряда алкалоидов.
С. Р. Мардашевым и его сотр. было установлено, что уроканиновая к-та является ингибитором гистидиндекарбоксилазы (КФ 4.1.1.22). Т. к. содержание уроканиновой к-ты в коже больных при некоторых дерматозах понижено, можно было предвидеть в этом случае более активное Д. гистидина с образованием гистамина, способствующего дерматозу.
Была сделана попытка применения леч. мазей, содержащих уроканиновую к-ту, для терапии дерматозов; предварительные данные свидетельствуют о положительном эффекте.
Гамма-Аминомасляная к-та — продукт Д. L-глутамата — применяется для лечения патол, состояний, связанных с нарушением функций ц. н. с.: при ослаблении памяти, атеросклерозе мозговых сосудов и нарушениях мозгового кровообращения, после перенесенных травм и параличей, при головной боли, бессоннице, головокружениях, связанных с гипертонической болезнью, в педиатрии — при умственной отсталости.
Д. кетокислот было впервые обнаружено К. Нейбергом в 1911 г. В экстрактах из пивных дрожжей им были найдены специфические ферменты, катализирующие Д. пировиноградной, альфа-кетомасляной, альфа-кетовалериановой и других a-кетокислот с образованием соответствующего альдегида и CO2. Реакция Д. кетокислот протекает по схеме:
Позднее было доказано существование Д. альфа-кетоглутаровой к-ты. Из экстрактов высших растений были выделены специфические декарбоксилазы альфа-кетоглутаровой и щавелево-уксусной к-т. Было показано, что Д. щавелево-уксусной к-ты (оксалата) с образованием пировиноградной к-ты (пирувата) осуществляется p-декарбоксилазой, атакующей бета-COOH-группу, что отличает ее от альфа-декарбоксилазы Нейберга.
В тканях животных альфа-кетокислоты подвергаются окислительному Д. с образованием соответствующих укороченных на один атом углерода карбоновых к-т и CO2. В процессе тканевого обмена углеводов, жиров и белков в качестве промежуточных продуктов образуются Пировиноградная, альфа-кетоглутаровая, щавелево-уксусная и другие а-кетокислоты. Накопление их (особенно пировиноградной к-ты, образующейся также в результате других метаболических превращений) может привести к нарушению физиол, функций, и в первую очередь — функций ц. н. с. Поскольку все декарбоксилазы a-кетокислот являются сложными ферментами, коферментом которых является фосфорилированная форма витамина B1—тиаминпирофосфат, то при B1-авитаминозе имеют место нарушения функций нервной системы, напр, при полиневрите.
Выяснению путей окисления пировиноградной к-ты посвящено много работ. В 1943 г. Г. Кребс предложил схему превращения пировиноградной к-ты через цикл ди- и трикарбоновых к-т (см. Трикарбоновых кислот цикл), в к-ром одна молекула пировиноградной к-ты окисляется с образованием трех молекул CO2 и двух молекул H2O (см. Окисление биологическое). Выяснены детали механизма этой реакции и пути ее регуляции. Основным путем превращения пировиноградной к-ты в животных тканях, у растений и у аэробных микроорганизмов является ее окислительное Д. до ацетил-КоА, катализируемое мультиферментным пируватдегидрогеназным комплексом. Д. альфа-кетоглутаровой к-ты также осуществляется при участии аналогичного альфа-кетоглутаратдегидрогеназного комплекса.
Полное окисление альфа-кетокислот, начинающееся с окислительного Д., до CO2 и H2O способствует освобождению энергии, необходимой для протекания процессов жизнедеятельности в любых живых организмах, причем значительная часть этой энергии накапливается в высокоэргических пирофосфатных связях АТФ.
Библиография: Березов Т. Т. и Лерман М. И. диаминопимелиновая кислота — новая природная аминокислота, Усп. совр, биол., т. 51, в. 3, с. 285, 1961, библиогр.; Браунштейн А. Е. Биохимия аминокислотного обмена, М., 1949, библиогр.; он же, Главные пути ассимиляции и диссимиляции азота у животных, М., 1957, библиогр.; Каган 3. С. и Игнатьева Л. И. Аллостерические свойства декарбоксилазы мезо-a, е-диаминопимелиновой кислоты у накапливающего L-лизин штамма Brevibacterium-22, Докл. АН СССР, т. 197, с. 1196, 1971; Каган 3. С., Кретович В. Л. иДроновА. С. Влияние кетокислот на декарбоксилазу глютаминовой кислоты у пшеницы, Биохимия, т. 28, в. 5, с. 824, 1963, библиогр.; Мардашев С. Р. Энзиматическое декарбоксилирование аминокислот, Усп. совр, биол., т. 28, в. 3, с. 365, 1949, библиогр.; Blaschko H. The amino acid decarboxylases of mammalian tissue, Advanc. Enzymol., v. 5, p. 67, 1945, bibliogr.; Boeker E. А. а. Snell E. E. Amino acid decarboxylases, в кн.: Enzymes, ed. by P. D. Boyer, v. 6, p. 217, N. Y.— L., 1972, bibliogr.; Lovenberg W., Weissbасh H. a. Udenfriend S. Aromatic L — amino acid decar-boxvlase, J. Biol. Chem., v. 237, p. 89, 1962; Meister A. Biochemistry of the amino acids, v. 1—2, N. Y.— L., 1965; Moriguсhi M., Jamamoto T. a. Soda K. Studies on L-lysine decarboxylase from Bacterium cadaveris, Bull. Inst. Chem. Res., Kyoto Univ., v. 51, № 6, p. 333, 1973, bibliogr.; Morris D. R. a. Fillingame R. H. Regulation of amino acid decarboxylation, Ann. Rev. Biochem., v. 43, p. 303, 1974, bibliogr.
Источник