О пролапсе митрального клапана
Патология регистрируется у малышей и совершеннолетних пациентов, обнаруживается при прослушивании сердца или во время целенаправленного лабораторно-диагностического обследования. Нарушение эластичности створок в митральном клапане левого предсердия называется пролапсом, отклонение наблюдается при сократительном механизме левого желудочка.
Разновидности заболевания
Специалисты выделяют первичную и вторичную форму пролапса митрального клапана, поражение может затрагивать переднюю, заднюю или обе створки. Наблюдаются три степени патологии:
первая – с провисанием створок от 3 до 6 мм;
вторая – от 6 до 9 мм;
третья – больше 9 мм.
Заболевание разделяется по скорости обратного хода крови:
первая степень – в области створок;
вторая – в середине левого предсердия;
третья – на противоположном конце предсердия.
К начальному поражению относится пролапс митрального клапана 1 степени.
Источники развития
Патологическое состояние чаще регистрируется у женщин, наблюдается практически у 10% больных. Первичная форма заболевания относится к врожденным болезням и сочетается с иными генетическими аномалиями в соединительных тканях:
с дифференцированной формой врожденной соединительнотканной недостаточности – болезнью Марфана;
несовершенным десмогенезом – синдромом Черногубова — Элерса – Данлоса;
поликистозным поражением почек у взрослых.
Вторичная форма формируется в качестве осложнений:
нарушенного кровоснабжения в сосочковых мышцах;
болезни Бенье – Бека – Шаумана;
ГКМП с патологическим утолщение левого желудочка.
У большинства пациентов заболевание выявляется при профилактическом обследовании – оно протекает без выраженной симптоматики.
Клинические симптомы
При пролапсе митрального клапана симптоматика напоминает проявления ВСД, особенно в молодом возрасте. Основные признаки представлены:
ощущением недостаточного поступления воздуха;
ознобом, частыми или редкими мочеиспусканиями, как ответной реакцией на психоэмоциональные нагрузки;
цефалгиями по утрам и вечерам, частыми перепадами настроения;
головокружения, кратковременными обмороками.
Дополнительные симптомы включают чувство сердцебиения, аритмии – выраженность зависит от степени тяжести патологии. Больные могут предъявлять жалобы на дискомфорт с левой стороны груди, которые не связаны с тяжелым трудом, занятиями спортом или психоэмоциональным состоянием.
Диагностическое обследование
При обращении в участковую поликлинику пациент направляется на консультацию к кардиологу. Врач просматривает историю болезни, задает вопросы о симптомах и общем состоянии больного. При осмотре предварительный диагноз выставляется по косвенным признакам во время прослушивания сердца.
При сокращении желудочков может наблюдаться посторонний звук, напоминающий щелчок и легкий шум, возникающий при обратном ходе крови. Легкая степень поражения указанной симптоматики не проявляет.
Лабораторное исследование не позволяет установить диагноз, основным считается инструментальное обследование. При проверке пациент проходит:
ЭКГ – пролапс митрального клапана не показывает специфических изменений. В некоторых случаях может наблюдаться блокада проводящих магистралей, экстрасистолы, признаки мерцательной аритмии.
УЗИ сердечной мышцы – эхокардиография считается точной методикой, позволяющей выявить наличие заболевания, оценить степень поражения и дисфункцию клапанов.
После подтверждения предположительного диагноза кардиолог приступает к расчету схемы терапии.
Особенности лечения
У пролапса митрального клапана нет специфических признаков, позволяющих точно определять патологию. Симптоматика схожа со многими болезнями, что не дает право на самостоятельную терапию по учебнику. Лечением должен заниматься врач, опираясь на данные диагностического обследования.
Терапия не проводится при пролапсе, не имеющем признаков недостаточности в митральном клапане или при нормальном ЭКГ, без видимых нарушений ритмичности сокращений сердца. За пациентом устанавливается наблюдение, с регулярным прохождением УЗИ – через год.
Больному рекомендуется снизить количество или полностью отказаться от употребления алкогольных напитков, чая или кофе. Пациент должен бросить курить. В качестве меры профилактики прописывается прием поливитаминного комплекса с магнием. Научно доказано, что при указанной патологии снижается содержание элемента в крови.
Медикаментозная терапия при пролапсе неактуальна и направлена на подавление присутствующих клинических симптомов. Для лечения болезни при сильном забросе крови в предсердие используется хирургическое вмешательство, с установкой протезаили пластикой пораженного клапана.
Возможные последствия
У большинства пациентов заболевание протекает без вторичных поражений. Последствия присутствуют у больных, имеющих утолщенные или удлиненные митральные створки, увеличенную полость в левом желудочке или правом предсердии, систолические шумы.
Основные осложнения патологии представлены:
отрывом сухожильных нитей;
переходом на следую стадию болезни;
скоплением высокомолекулярного белка на створках;
аритмическими отклонениями в сердцебиении;
инфекционным полипозно-язвенным воспалением эндокарда.
При тяжелой степени недостаточности митрального клапана и отсутствии своевременной терапии проблема заканчивается летальным исходом. Врачи рекомендуют не отказываться от ежегодных профилактических осмотров в поликлинике и прохождения диагностического обследования. Своевременное обнаружение заболевания и вовремя проведенное хирургическое вмешательство поможет сохранить жизнь и вернуть частично потерянную трудоспособность.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Авторизуйтесьчтобы оставлять комментарии
Возрастные ограничения 18+
Лицензия на осуществление фармацевтической деятельности ЛО-77-02-011246 от 17.11.2020 Скачать.
Источник
Терапия препаратами магния при первичном пролапсе митрального клапана
Нормальный уровень магния в организме человека признан основополагающей константой, контролирующей здоровье человека [2, 7, 8]. В настоящее время среди возможных патогенетических механизмов дисплазии соединительной ткани (ДСТ) многие исследователи указыв
Нормальный уровень магния в организме человека признан основополагающей константой, контролирующей здоровье человека [2, 7, 8]. В настоящее время среди возможных патогенетических механизмов дисплазии соединительной ткани (ДСТ) многие исследователи указывают на хронический дефицит ионов магния, что ведет к нарушению формирования соединительнотканных структур, обусловливает хаотичность расположения волокон коллагена — основной морфологический признак ДСТ [5, 7, 9, 10].
Сведения о распространенности дефицита магния (норма магния в сыворотке крови: 1,0–1,15 ммоль/л) варьируются в широких пределах в зависимости от исследованной популяции, критериев диагностики и использованных методов исследования. По данным исследований, проведенных в России с участием пациентов с идиопатическим пролапсом митрального клапана (ПМК), уменьшение содержания магния в волосах выявлено в 72,0% случаев [5]. В схемы комплексного ведения пациентов с первичным ПМК прочно вошли препараты магния [5].
С целью сравнения эффективности применения у пациентов с идиопатическим ПМК препаратов Магнерот и Магне В6 мы провели простое сравнительное открытое проспективное исследование.
Критериями включения служили:
- ранее диагностированный первичный ПМК в возрасте от 16 до 35 лет;
- понимание пациентами сути предстоящего исследования;
- возможность проведения монотерапии препаратом магния и соблюдения двухнедельного периода вымывания перед проведением исследования в случае, если больной получал медикаментозную терапию;
- добровольное информированное согласие на участие в исследовании.
Критериями исключения были:
- наличие врожденного или приобретенного порока сердца, подтвержденного данными ЭхоКГ;
- наличие черепно-мозговой травмы в анамнезе;
- сердечно-сосудистые заболевания;
- острые заболевания в течение одного месяца до исследования;
- противопоказания к применению препаратов магния;
- побочные эффекты терапии, требующие отмены препарата;
- несоблюдение больным графика лечения и обследования;
- нежелание пациента продолжать участие в исследовании.
В соответствии с критериями включения и исключения (табл. 1), в исследование были включены 90 пациентов с идиопатическим ПМК (45 мужчин и 45 женщин) в возрасте 23,3 ± 5,2 года. У 52 пациентов функция митрального клапана была нарушена в виде наличия митральной регургитации различной степени выраженности (39% — регургитация 1-й степени, 39% — 2-й степени, 22% — 3-й степени); у 32 больных функция митрального клапана была сохранена; в 64% случаев выявлялась миксоматозная дегенерация митрального клапана. Кроме того, отмечены: в 14% случаев — расширение аорты, в 20% — пролапс трикуспидального клапана, в 87% — аномально расположенные хорды, в 56% — удлинение хорд митрального клапана. Все пациенты имели те или иные фенотипические признаки ДСТ: у всех выявлен астенический тип конституции, у 78% наблюдались деформации грудной клетки или позвоночника, у 26% — другие локомоторные проявления ДСТ (синдром гипермобильности суставов, плоскостопие, искривление нижних конечностей), у 34% — птозы внутренних органов, у 72% — дефицит массы тела. В качестве группы контроля были обследованы 30 практически здоровых добровольцев (15 мужчин и 15 женщин, средний возраст — 22,3 ± 3,5 года), соответствующих по полу и возрасту.
Всем пациентам было проведено общеклиническое обследование, эхокардиография, суточное мониторирование ЭКГ по Холтеру (Холтер-ЭКГ), велоэргометрия (ВЭМ), а также определение уровня магния в слюне и сыворотке. Исходный вегетативный тонус оценивали на основании клинических тестов (А. М. Вейн, 1998). Для выявления и оценки невротических нарушений использовался опросник, разработанный Д. М. Менделевичем и К. К. Яхиным [3]. Статистическая обработка результатов проводилась с использованием пакета программ SPSS for Windows.
Результаты. Оценка субъективного статуса пациентов, проведенная до начала медикаментозной терапии, продемонстрировала преобладание жалоб со стороны сердечно-сосудистой системы — 89%. Далее по частоте отмечены жалобы астенического характера (слабость, вялость, легкая утомляемость, снижение работоспособности, апатия): они регистрировались у 80% пациентов.
При проведении ЭКГ и Холтер-ЭКГ были выявлены случаи манифестных и латентных нарушений ритма и проводимости сердца. Проведение Холтер-ЭКГ в большинстве случаев было более информативно в диагностике нарушений ритма пациентов с ПМК, что диктует необходимость включения этого метода диагностики в программу обследования пациентов с ДСТ. По данным Холтер-ЭКГ, у пациентов с ПМК фиксировались суточные колебания сердечного ритма от 39-59 до 109-182 уд/мин. У 42% (38 пациентов) выявлен синдром ранней реполяризации желудочков, у 68 человек — нарушения процессов реполяризации различной степени выраженности, у 24 больных — удлинение интервала QT в сравнении с должной величиной.
По данным анкетирования, у 76 (84%) пациентов была выявлена вегетососудистая дистония, при этом у 54 больных (71%) обнаружена симпатикотония, у 22 (24%) — ваготония, у 14 человек — эутония. Анализ вариабельности сердечного ритма у пациентов с ПМК продемонстрировал достоверно более высокие значения среднесуточных показателей — SDNN, SDNNi, RMSSD с преобладанием активности симпатического отдела (SDANN — 149,4 мс, р = 0,004).
Уровни магниемии у пациентов с ПМК достоверно не отличались от контрольной группы и от нормального содержания магния в сыворотке крови, тогда как исследование концентрации магния в ротовой жидкости документировало дефицит данного макроэлемента у пациентов с ПМК, подтверждая имеющиеся литературные данные (табл. 2)
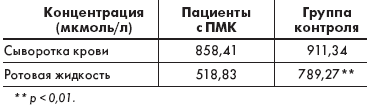 |
| Таблица 2. Содержание магния в сыворотке крови и ротовой жидкости пациентов с ПМК |
При сопоставлении показателей вариабельности сердечного ритма и уровнем магния в ротовой жидкости выявлены прямые корреляционные взаимосвязи: чем ниже содержание магния в биологических средах организма, тем ниже показатели вариабельности сердечного ритма и выше тонус симпатической нервной системы. Возможным объяснением этого явления может быть нарушение активности Na + –K + -АТФ-азы при низкой концентрации ионов магния, что влияет на обратный захват адреналина симпатическими нейронами, и, следовательно, его инактивацию и приводит к гиперсимпатикотонии.
Анализ показателей клинического опросника для выявления и оценки невротических состояний выявил присутствие в психологическом профиле пациентов такого феномена, как невротическая тревога (табл. 3). Кроме того, значения по шкалам астении и вегетативных нарушений превысили уровень показателей нормального диапазона, что отражало формирование психического истощения, обусловленного вегетативной напряженностью, являющейся одним из облигатных признаков ДСТ [4].
После проведенного обследования пациенты с ПМК были распределены методом последовательного включения на две группы, сопоставимые по полу и возрасту. Пациентам группы I (45 человек) назначался Магнерот по схеме: 2 таблетки 3 раза в день первые 7 дней, затем по 1 таблетке 3 раза в день в течение 8 нед. В группе II (45 человек) назначался Магне В6: 2 таблетки 3 раза в день в течение 8 нед.
 |
| Таблица 3. Величины диагностических коэффициентов по шкалам невротических расстройств |
Повторное обследование пациентов проводилось после завершения курса лечения. Уровень магния в ротовой жидкости достоверно повысился в обеих группах (0,903 ммоль/л, р 2 соответственно до и после лечения (p > 0,05)). Изменения массы тела были отмечены у 42% пациентов этой группы (р = 0,091). Наибольшая прибавка составила 3 кг к завершению курса лечения; вместе с тем у большинства пациентов данной группы показатели индекса массы тела оставались ниже возрастной нормы. При этом следует отметить, что все 19 пациентов, отмечавших положительную динамику массы тела, активно интересовались возможностью продлить курс лечения Магнеротом. Вопрос, связан ли описанный эффект с особенностью препарата — наличием в составе оротовой кислоты — требует уточнения.
В обеих группах все пациенты завершили полный курс лечения препаратом. Курсовая доза магния, полученная в первой группе Магнерот, составила 6 888 мг, во второй группе (Магне В6) — 16 128 мг. Препараты магния хорошо переносились больными, лишь у двух человек группы I (4%) были жалобы на головокружение и нарушение стула при приеме 6 таблеток Магнерота в день, которые исчезли через 2 дня после снижении дозы препарата наполовину. Других отступлений от протокола лечения не наблюдалось.
Выводы
- Применение препаратов магния у пациентов с ПМК патогенетически обосновано выявляемым дефицитом тканевого пула данного макроэлемента.
- Курсовое назначение препаратов магния приводит к улучшению субъективного самочувствия. Магнерот устраняет вегетативную дисфункцию также хорошо, как апробированный в практике кардиологов и неврологов Магне В6.
- Положительная динамика электрофизиологических показателей сердечной деятельности, уменьшение частоты эпизодов желудочковых нарушений ритма и наджелудочковой экстрасистолии наблюдается в обеих группах. Однако использование препарата Магнерот более предпочтительно, о чем свидетельствуют данные статистического анализа.
- Лекарственные средства второго поколения магнийорганических препаратов (Магнерот, Магне В6) демонстрируют эффективность в качестве корректоров магниевого дефицита. Следует отметить, что в первой группе курсовая доза магния была на 9 900 мг меньше, а приверженность к терапии и полученные результаты оказались выше.
- С учетом метаболической активности оротовой кислоты [2], входящей в состав препарата Магнерот, и полученной динамики массы тела у 19 пациентов группы I (не достигшей статистически значимого уровня) требуется дальнейшее исследование в плане уточнения возможного влияния препарата на показатели трофологического статуса пациентов.
Литература
- Городецкий В. В. Препараты магния в медицинской практике. Малая энциклопедия магния / В. В. Городецкий, О. Б. Талибов. М.: Медпрактика, 2003. 44 с.
- Громова О. А. Магний и пиридоксин: основы знаний. Новые технологии диагностики и коррекции дефицита магния / О. А. Громова. Обучающие программы ЮНЕСКО. М.: РСЦ Институт микроэлементов, ЮНЕСКО, 2006. 176 с.
- Менделевич В. Д. Клиническая медицинская психология: Практическое руководство / В. Д. Менделевич. М.: Медпресс, 1998. 542 с.
- Нечаева Г. И. Кардио-гемодинамические синдромы при дисплазии соединительной ткани (клиника, диагностика, прогноз): автореф. дис. … д-ра мед. наук / Г. И. Нечаева. Томск, 1994. 37 с.
- Результаты применения магниевой соли оротовой кислоты «Магнерот» при лечении больных с идиопатическим пролапсом митрального клапана / О. Б. Степура, О. О. Мельник, А. Б. Шехтер и др. // Российские медицинские вести. 1999. № 2. С. 64–69.
- Dreosti E. Magnesium status and health / Dreosti E. // Nutr. Rev. 1995; 53: 23–7.
- Durlach J. Primary mitral valve prolapse: a clinical form of primary magnesium deficit / J. Durlach // Magnes. Res. 1994; 7: 339–340.
- Durlach J. Le magnesium en biologie et an medicine / Durlach J., Bara M. // 2nd edition. Cachan (France): Edition Medicales Internationales; 2000.
- Idiopathic magnesium deficiency in mitral valve prolapse / L. Cohen, H. Bittermann, E. Grenadier et al // Amer. J. Сardiol. 1986; 57 (6): 486–487.
- Is magnesium deficit in lymphocytes a part of the mitral valve prolapse syndrome?/ Kitliewski M., Stepniewski M., Nessler J. et al. // Magnes. Res. 2004; 17(1): 39–45.
- Schimatchek H. F. Prevalence of hypomagnesemia in an unselected German population of 16,000 individuals / Schimatchek H. f., Rempis R. // Magnes. Res. 2001; 14: 283–90.
Г. И. Нечаева, доктор медицинских наук, профессор
И. В. Друк, кандидат медицинских наук
О. В. Тихонова, кандидат медицинских наук
С. Л. Морозов
Омская ГМА, Омск
Источник