При недостатке витамина в12 нарушается гликогенолиз
Описание наследственных нарушений каждого этапа метаболизма витамина В12 (кобаламина) в новом свете представило патогенез дефицита кобаламина и фолата (Hall, 1990). Клинические проявления приблизительно одинаковы при всех врожденных нарушениях метаболизма кобаламина, за исключением изолированного дефицита аденозилкобаламина, проявления которого идентичны симптомам метилмалоновой ацидурии (Rosenblatt и Whitehead, 1999; Surtees, 2001; Whitehead, 2006).
а) Биохимические изменения. Понятие «кобаламин» объединяет группу веществ, выполняющих функцию коферментов в двух клеточных реакциях человека: образовании метионина из гомоцистеина с метилкобаламином в качестве кофермента и превращении метилмалонил-кофермента А в сукцинил-кофермент А с аденозилкобаламином в качестве кофермента. Кобаламин, поступающий с пищей, преимущественно с животными белками, абсорбируется с помощью фактора Касла, затем поступает в кровоток в комплексе с транскобаламином-II после захвата клетками с помощью специфического поверхностного рецептора.
Внутри клетки кобаламин подвергается серии модификаций в результате которых образуется метилкобаламин и аденозилкобаламин. Дефицит кобаламина может быть классифицирован на четыре группы: дети, рожденные матерями с дефицитом кобаламина, дефицит системы абсорбции кобаламина, дефект транспорта витамина и нарушения внутриклеточной утилизации. Четвертая группа соответствует ряду дополнительных групп, обозначаемых от CblA до CblH, каждая из которых связана с специфическим ферментным блоком внутриклеточного метаболизма. В зависимости от участка ферментного дефекта, у пациентов отмечается метилмалоновая ацидурия или гомоцистинурия или их сочетание.
Уровень кобаламина в плазме остается нормальным при всех, за исключением одного (CblF), внутриклеточных дефектах метаболизма кобаламина, а также при дефекте транскобаламина II. С другой стороны, при врожденном гиповитаминозе и дефектах абсорбции отмечается низкий уровень кобаламина в плазме.
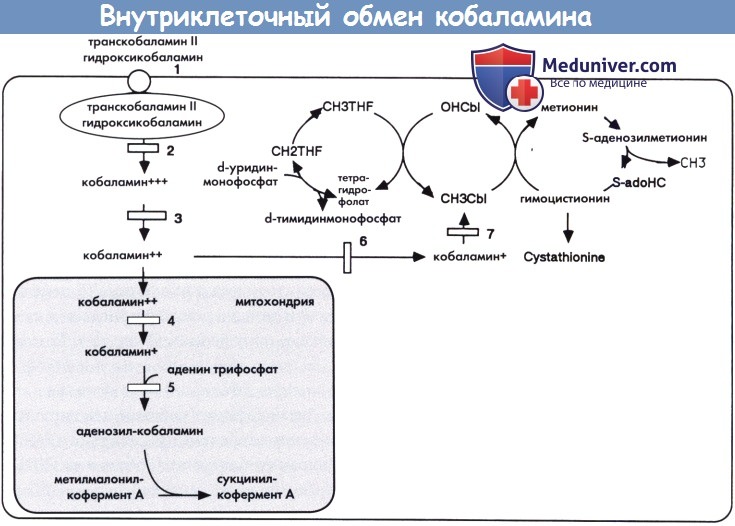
Дефицит транскобаламина II (1), кобаламина F (2) и кобаламина С или кобаламина D (3) приводят к нарушению синтеза кофакторов аденозил- и метил-кобаламина, в результате чего возникает комбинированная метилмалоновая ацидурия и гомоцистинурия в сочетании с гипометионинемией. Дефицит кобаламина А (4) и кобаламина В (5) приводят к нарушению синтеза только аденозил-кобаламина, в результате чего возникает изолированная метилмалоновая ацидурия. Дефицит кобаламина Е (6) и кобаламина G (7) приводит к нарушению синтеза только метил-кобаламина, в результате чего возникает гомоцистинурия и гипометионинемия (дефицит кобаламина А, В, С, D, Е, F и G является различными дополнительными группами метилмалоновой ацидурии: см. текст).
б) Генетические изменения. Все нарушения внутриклеточного метаболизма кобаламина наследуются аутосомно- рецессивным путем. Пренатальная диагностика может проводиться путем исследования амниотической жидкости и органических кислот. Дальнейшее подтверждение диагноза проводится на основании измерения количества определенных ферментов в культуре хорионических ворсин или с помощью молекулярного анализа, когда известно о наличии у пациента обеих мутаций (Morel et al., 2005).
в) Патофизиология. Многие неврологические, гематологические и биохимические проявления типичны для приобретенного дефицита кобаламина и фолата, врожденных дефектов абсорбции или транспорта кобаламина и фолата и внутриклеточных нарушений метаболизма кобаламина и фолата. Все виды нарушений приводят к дефициту метионинсинтетазы, играющей ключевую роль в патогенезе нарушений метаболизма кобаламина и фолата (Hall, 1990; Weir и Scott, 1995). Дефицит метионинсинтетазы обладает несколькими предположительными вторичными эффектами, включающими накопление метилтетрагидрофолата (СН3ТГФ) (теория фолатной ловушки), что препятствует ее участию в синтезе кофермента фолата, который необходим для синтеза ДНК и гемопоэза.
Дефицит метионинсинтетазы также приводит к нарушению синтеза метионина и аденозилметионина, который является основным донором метиловых остатков для метилирования многих субстратов, таких как нейротрансмиттеры, основный белок миелина и фосфолипиды плазматических мембран. Считается, что данное нарушение метилирования является причиной подострой сочетанной дегенерации спинного мозга, описанного как при приобретенном, так и врожденном дефекте. Другие факторы могут нарушать структуру и функцию центральной нервной системы при приобретенном и врожденном нарушении метаболизма кобаламина, например, токсическое действие накопленного гомоцистеина может стать причиной сосудистых повреждений и тромбоэмболии, и накопления метилмалонил-кофермента А и пропионил-кофермента А в связи с нарушением активности мутазы.
г) Клинические проявления:
1. Врожденный дефицит витамина В12. Дефицит кобаламина у детей на грудном вскармливании у матерей с субклинической пернициозной анемией или находящихся на строгой вегетарианской диете без достаточного поступления витамина В12 может привести к неврологическому регрессу, аномальным движениям и коме в сочетании с мегалобластной анемией. Введение витамина В12 приводит к быстрому улучшению неврологического статуса, но сохраняется задержка дальнейшего развития (Gutierrez-Aguilar et al., 2005).
2. Дефицит абсорбции и транспорта кобаламина. Нарушения абсорбции и транспорта кобаламина являются причиной синдрома дефицита кобаламина, характеризующегося прогрессирующим течением с началом в возрасте от 1 месяца до нескольких лет. Обычно первые симптомы связаны с желудочно-кишечным трактом, а также включают плохую прибавку в весе, мышечную слабость, вялость и мегалобластную анемию. Несколько месяцев спустя развиваются периферическая нейропатия, миелопатия и энцефалопатия с заметной отсрочкой развития. Нарушения абсорбции связаны с дефицитом фактора Касла или дефектом кубилинамниотического комплекса, который действует в качестве рецептора комплекса IF-кубилин (синдром Имеслунда-Гресбека) (Fyfe et al., 2004).
Дефект транспорта связан с дефицитом транскобаламина II, дефицит которого даже при лечении, может привести к тяжелым неврологическим нарушениям (Monagle и Tauro, 1995).
3. Нарушение внутриклеточного метаболизма. Внутриклеточный дефицит кобаламина, нарушающий синтез только метилкобаламина (кобаламин E/G/F) или метил- и аденозилкобаламина (кобаламин С/D) отмечается при трех основных типах заболевания. Чаще всего встречается тяжелая форма заболевания с началом в раннем возрасте, описанная у новорожденных и младенцев в возрасте до 3-х месяцев. Симптомы включают прогрессирующую сонливость, гипотонию, аномальные движения и/или припадки в сочетании с панцитопенией и мегалобластной анемией. У некоторых пациентов также отмечается полиорганная недостаточность, включающая почечную недостаточность с гемолитическим уремическим синдромом, кардиомиопатию и интерстициальную пневмонию. Поражение сетчатки с гранулярной депигментацией макулы и дальнейшим периферическим пигментным ретинитом часто является ранним признаком дефицита кобаламина С. Сообщающаяся гидроцефалия может быть дальнейшим осложнением.
У небольшого количества пациентов заболевание проявляется в детском возрасте в виде прогрессирующей неврологической деградации, микроцефалии, эпизодических припадков и мегалобластной анемии, которая обычно является основанием для постановки диагноза. При отсутствии лечения острая неврологическая деградация может сочетаться с признаками и симптомами, напоминающими подострую дегенерацию спинного мозга. В редких случаях развития заболевания у подростков и взрослых, отмечалась сходная подострая дегенерация спинного мозга, которой предшествовала острая деградация интеллектуальных функций и иногда поведенческие нарушения. Среди пациентов старшего возраста мегалобластная анемия может быть едва заметной, а пограничный макроцитоз следует рассматривать особенно тщательно (Ogier de Baulny et al., 1998; Roze et al., 2003). Fla KT и MPT выявляется атрофия мозга и/или демиелинизация (Rossi et al., 2001).
д) Лечение нарушения обмена витамина В12. Следует систематически исследовать чувствительность к поддерживающей терапии витамином В12. В зависимости от имеющегося дефекта выбирается использование парентерального или перорального пути введения, фармакологических или минимальных доз и гидроксикобаламина или естественных субстратов кобаламина (метил-, аденозилкобаламина). При нарушении транспорта и внутриклеточных дефектах может потребоваться пополнение запасов метионина путем перорального введения бетаина или дополнительного применения метионина. На основании метаболического пути бетаина предполагается, что дополнительное применение фолиевой кислоты может быть полезным при длительном лечении бетаином. В связи с тем, что эндогенный синтез карнитина зависит от метионина, при состояниях, сопровождающихся нарушением синтеза метионина, может быть эффективно поддерживающее применение карнитина. Логично соблюдение диеты с нормальным содержанием белка и отказ от повышенного потребления белка (Ogier de Baulny et al., 1998).
Редактор: Искандер Милевски. Дата публикации: 14.12.2018
Источник
Недостаток витамина В12
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Витамин В12 (кобаламин — Cbl) поступает в организм в основном с продуктами животного происхождения (такими как мясо, молоко) и усваивается путём абсорбции. Абсорбция витамина В12 — многоэтапный процесс, включающий:
- протеолитическое высвобождение кобаламина из белков;
- присоединение кобаламина к белку желудочного секрета (внутренний фактор — IF, фактор Кастла);
- узнавание комплекса «IF-кобаламин» рецепторами слизистой оболочки подвздошной кишки;
- транспорт через илиальные энтероциты в присутствии ионов кальция;
- высвобождение в циркуляцию системы воротной вены в комплексе с транкобаламином II (ТС II) — белком сыворотки крови.
Обычно дефицит (недостаток) витамина В12 у детей раннего возраста вызван его недостаточным поступлением с пищей в организм матери.
Наиболее частое нарушение абсорбции витамина В12 — пернициозная анемия. Это хроническое заболевание, развивающееся вследствие нарушения поступления кобаламина вследствие недостаточности IF в желудочном секрете. Недостаточное содержание IF в желудочном секрете может быть вызвано врождённым дефицитом этого фактора или приобретёнными причинами, в том числе иммунными (выработкой аутоантител против IF и париетальных клеток слизистой оболочки желудка).
Для высвобождения кобаламина из белкового комплекса, в форме которого соединение поступает с пищей, необходимы кислая реакция среды и пепсиновая активность желудочного сока. Именно поэтому пернициозная анемия развивается при некоторых заболеваниях желудка (атрофическом гастрите, частичной гастрэктомии).
При отсутствии или повреждении IF поступление кобаламина в энтероциты становится невозможным, что приводит к развитию пернициозной анемии. Недостаточность IF может быть как врождённой, так и приобретённой.
Нарушение метаболизма витамина В12 во многих случаях развивается при недостаточном белковом питании (квашиоркор), заболеваниях печени. Некоторые лекарственные средства влияют на абсорбцию и метаболизм витамина В12.

Код по МКБ-10
Метаболизм витамина В12
Витамин В12 (кобаламин) — входит в состав продуктов только животного происхождения: мясо, печень, молоко, яйца, сыр и другие (витамин в тканях животных является производным бактерий). Под влиянием кулинарной обработки и протеолитических ферментов желудка он высвобождается и быстро связывается с «R-binders» (транс-кобаламины I и III) — белками с быстрой (rapid) электро-форетической подвижностью, по сравнению с внутренним фактором; в меньшей степени витамин В12 соединяется с внутренним фактором (ВФ, фактор Касла) — гликопротеином, вырабатываемым париетальными клетками фундальной части и тела желудка.
Патогенез
В плазме витамин В12 присутствует в виде коферментов — метилкобаламина и 5′-дезоксиаденозилкобаламина. Метилкобаламин необходим для обеспечения нормального кроветворения, а именно для синтеза тимидинмонофосфата, входящего в состав ДНК, и образования тетрагидрофолиевой кислоты. Нарушение образования тимидина при дефиците витамина В12 приводит к нарушению синтеза ДНК, замедлению нормальных процессов созревания гемопоэтических клеток (удлинение фазы S), что выражается в мегалобластическом кроветворении.
Симптомы недостатка витамина В12
Выделяют наследственные и приобретенные формы витамин В12-дефицитной анемии.
Наследственные формы витамин В12 дефицитных анемий встречаются редко. Клинически характеризуются типичной картиной мегалобластной анемии с наличием симптоматики поражения желудочно-кишечного тракта и нервной системы.
Симптомы болезни появляются постепенно. Первоначально отмечают ухудшение аппетита, отвращение к мясу, возможны диспепсические явления. Наиболее выражен анемический синдром — бледность, легкая иктеричность кожи с лимонно-желтым оттенком, субиктеричность склер, слабость, недомогание, быстрая утомляемость, головокружение, тахикардия, одышка даже при небольшой физической нагрузке.
Источник
Дефицит витаминов группы B: симптомы, диагностика и лечение
Нехватка витаминов может возникнуть по самым разным причинам. К основным из них относятся:
- однообразный рацион;
- неправильное приготовление продуктов;
- заболевания желудочно-кишечного тракта;
- беременность и период лактации;
- стрессовые состояния и нервные перегрузки;
Витамин B1
Клеточный энергетик, способствующий росту и развитию. Витамин B1 повышает умственную и физическую работоспособность, улучшает детоксикационную функцию и обмен веществ в нервной системе. Он также повышает настроение, обладает мягким обезболивающим и ранозаживляющим действием.
При дефиците витамина B1 возникают различные нарушения со стороны нервной, сердечно-сосудистой и пищеварительной систем. Чтобы восполнить его недостаток, включите в рацион гречку, кукурузу, кешью, чечевицу.
Основные симптомы дефицита витамина B1
- потеря аппетита;
- нарушение координации движения;
- депрессия, нервозность;
- ослабление когнитивных функций (снижение памяти);
- мышечная слабость.
Крайняя форма нехватки витамина — болезнь Бери-бери, при которой происходит поражение периферических нервов или сердечно-сосудистой системы. В результате этого истощаются мышцы, особенно ног, появляются сильные боли в икрах, развивается слабость и ухудшается походка.
Причины дефицита витамина B1
- постоянное употребление рафинированных продуктов (мука высших сортов и продукты из нее, шлифованный рис);
- повышенная потребность в витамине (беременность, кормление грудью, стресс, физические нагрузки, инфекции);
- хронические заболевания (сахарный диабет, тиреотоксикоз, отравление антибиотиками, алкоголизм);
- курение;
- чрезмерное употребление чая и кофе, так как кофеин разрушает витамин B1.
Если Вы заметили, что ухудшилось настроение, появились судороги в икроножных мышцах, на фоне постоянного стресса пропал аппетит, выполните в СИТИЛАБ исследование 95-10-201 — Витамин B1 (тиамин). Анализ помогает выявить дефицит витамина B1, своевременно назначить прием лекарственных препаратов и скорректировать режим питания.
Витамин B5
Пантотеновая кислота (витамин B5) оказывает стресс-протекторное действие и входит в состав кофермента А, который принимает участие в обменных процессах и белков, и жиров, и углеводов.
Витамин B5 необходим для синтеза жизненно важных веществ, таких как гемоглобин, холестерин, гистамин, ацетилхолин. Кроме этого, он активизирует синтез глюкокортикостероидов (гормоны надпочечников), которые обладают иммунорегулирующим, антиаллергическим, противовоспалительным действием. Важно понимать, что без пантотеновой кислоты плохо или вовсе не усваиваются и другие витамины. В рацион добавить порцию витамина помогут скумбрия, сардина, тунец, сладкий болгарский перец, кедровые орехи.
Основные симптомы дефицита витамина B5
- быстрая утомляемость, слабость, апатия;
- появления чувства жжения в пальцах ног, нередко — их онемении;
- при выраженном недостатке возникает синдром «горящих ступней» — мучительные боли в ногах в ночное время.
При нехватке пантотеновой кислоты снижается выработка желудочного сока, ухудшается работа сердца, развиваются невриты, повышается риск развития заболеваний кожи, язвы двенадцатиперстной кишки.
Причины дефицита витамина B5
- длительное неполноценное питание (бедная белками, жирами, витамином С и витаминами группы В пища);
- подавление кишечной микрофлоры, в том числе длительный прием антибиотиков и сульфаниламидных препаратов;
- заболевания кишечника различной природы.
Чтобы своевременно выявить дефицит пантотеновой кислоты, пройдите в СИТИЛАБ исследование 95-10-202 — Витамин B5 (пантотеновая кислота).
Витамин B6
По сути, витамин B6 (пиридоксин) — «активатор» метаболизма. Он необходим для регуляции усвоения белков, обмена аминокислот, принимающих участие в синтезе основных нейромедиаторов и гемоглобина. При участии пиридоксина происходит доставка глюкозы к клеткам, в том числе к клеткам мозга. Витамин B6 влияет на когнитивные функции: улучшает память, мышление, а также повышает настроение и помогает противостоять стрессу.
Содержится во многих растительных продуктах — бананы, орехи (фисташки, фундуку), авокадо, фасоль, соя, говяжья печень. Важно помнить, что при длительной или неправильной термической обработке продуктов данный витамин разрушается.
Основные симптомы дефицита витамина B6
- утомляемость, депрессия;
- выпадение волос;
- «заеды» в уголках губ.
Явная нехватка витамина B6 снижает синтез дофамина, серотонина, гамма-аминомасляной кислоты, мелатонина. Это может приводить к психологическим и физиологическим нарушениям, бессоннице, снижению интеллектуальных способностей, раздражительности, апатии или наоборот к агрессивному поведению.
Причины дефицита витамина B6
- ослабленное состояние, в том числе после операций, тяжелой болезни;
- атеросклероз;
- сердечно-сосудистые заболевания;
- беременность;
- длительное избыточное потребление белковой пищи;
- повышенные физические нагрузки;
- заболевания печени, гастриты;
- малокровие.
Если Вы заметили, что прическа стала не такой пышной, появилась сильная сухость кожи в области носогубной складки, над бровями, в целом кожа стала более сухой и шершавой, медленно заживают порезы и царапины — не откладываете визит к врачу. Первое, что Вам необходимо сделать, это сдать кровь в СИТИЛАБ для исследования 95-10-203 Витамин B6 (пиридоксин), которое поможет установить, есть ли дефицит витамина B6 в организме или его достаточно.
Витамин B12
Витамины B12 — это целая группа кобальтосодержащих биологически активных веществ. Одним из главных в ней является цианокобаламин. Он участвует в производстве эритроцитов и процессе кроветворения. Содержится преимущественно в продуктах животного происхождения — мясо, молоко, яйца. Поэтому чаще всего дефицит наблюдается у людей, соблюдающих строгую вегетарианскую диету, у беременных, которым требуется повышенное количество B12, а также при атрофическом гастрите, хронических воспалительных заболеваниях тонкой кишки.
Основные симптомы дефицита витамина B12
- онемение конечностей;
- мышечная слабость;
- расстройства зрения (двоение в глазах, размытые контуры предметов);
- бледность кожи;
- снижение памяти.
При нехватке витамина B12 возникает риск развития тромбозов, нарушается работа вегетативной нервной системы.
Причина дефицита витамина B12 — недостаточное всасывание его в кишечнике. Это может быть связано с нарушением внутреннего фактора в желудке, развитием патогенной микрофлоры, которая может препятствовать всасыванию в желудке.
С возрастом, после 40 лет, усвоение витамина B12 происходит хуже, поэтому важно своевременно выявить его дефицит, чтобы предотвратить серьезные болезни. Для этого пройдите в СИТИЛАБ исследование 33-20-045 — витамин B12.
Источник