Статьи
Дефицит витамина В6
Витамин В6 (Пиридоксин) является сводным названием группы водорастворимых взаимозаменяемых соединений пиридоксина, пиридоксаля, и пиридоксамина, и их 5′-фосфат производных. Пиридоксаль-5′-фосфат (ПЛФ) и, в меньшей степени, пиридоксамин фосфат, действуют как коферменты для многих ферментов, участвующих в метаболизме аминокислот, в том числе аминотрансфераз, декарбоксилаз, рацемаз и дегидратаз. В ходе ПЛФ-зависимых реакций синтезируется целый ряд важнейших соединений: нейромедиаторов, таких как серотонин
(из 5-гидрокситриптофана), γ-аминомасляной кислоты (из глутамата), допамин, и гистамин, а также гем и порфирины. Кроме того, витамин В6 участвует в метаболизме гликогена, превращении триптофана в ниацин, синтезе цистеина из метионина, активном транспорте аминокислот через клеточные мембраны, комплексообразовании металлов и синтезе арахидоновой и докозагексаеновой кислоты из линолевой и линоленовой кислот соответственно. Таким образом, витамин В6 необходим для нормальной работы нервной системы, сокращения сердечной мышцы, процессов формирования гемоглобина и красных кровяных телец, метаболизма других витаминов, а также поддержания физиологических концентраций уровней липидов крови.
Потребность в витамине В6 зависит от возраста: 0-6 мес: 0,5 мг/сут, 6 мес-1 год – 0,6 мг/сут., 1-3года – 0,9 мг/сут., 4-6 лет – 1,3 мг/сут., 7-10 лет – 1,6 мг/сут, мальчики 11-14 лет – 1,8 мг/сут, юноши 15-18 лет – 2 мг/сут., девушки 11-18 лет – 1,6 мг/сутки.
Потребность в пиридоксине может повышаться во время стресса и при повышенных нагрузках, приеме антидепрессантов и оральных контрацептивов, химиотерапии и наличии злокачественных заболеваний, у пациентов, страдающих СПИДом, гепатитами, получающих терапию гемодиализа, заболеваниях кишечника, особенно глистных инвазиях, а также у лиц, употребляющих алкоголь и курильщиков. Следует отметить что лицам, употребляющим белковую пищу богатую триптофаном, метионином и цистеином также необходимы более высокие количества витамина В6. Такие препараты как изониазид, пеницилламин, кортикостероиды, а также противосудорожные медикаменты ингибируют активность витамина В6.
Содержание пиридоксина в грудном молоке женщин не страдающих гиповитаминозом В6 и адаптированных смесях для детского питания достаточно для нормального роста и развития ребенка. Кроме того, хорошими источниками данного витамина являются: цельнозерновые, мясо, рыба, птица, печень и некоторые овощи. При высокотемпературной обработке продуктов питания большая часть пиридоксина.
Причина заболеваний и состояний, которые ранее связывались с общим дефицитом пиридоксина в настоящее время пересматривается. Имеется целый ряд состояний которые связаны с нарушением структуры ферментов, участвующих в обмене пиридоксина, пиридоксаля, пиридоксамина или связанных с ними веществ. Эти синдромы включают развитие витамин В6-зависимых судорог, витамин В6-дефицитную анемию, ксантуреновую ацидурию, цистатионурию и гомоцистеинурию, а также некоторые другие заболевания.
Учитывая что в настоящее время достаточное количество продуктов питания обогащено витамином В6, «чистые» дефицитные состояния встречаются достаточно редко. Что касается детей, наиболее часто проявления гиповитаминоза В6 регистрируются у детей получающих специфическую терапию по поводу туберкулеза, лечение гормональными или противосудорожными препаратами. Нередко дефицит витамина В6 отмечается у пациентов получающих высокодозовую химиотерапию (например при злокачественных заболеваниях крови). В некоторых случаях гиповитаминоз выявляется при резистентной к терапии железодефицитной или полидефицитной анемии. Типичными проявлениями недостаточного поступления пиридоксина с пищей являются судороги у новорожденных и детей младшего возраста, периферический неврит, дерматит и анемия. Также характерны неспецифичные проявления со стороны желудочно-кишечного тракта. Поражения кожи чаще протекают по типу себорейного дерматита с образованием участков шелушения и зуда, кроме того, могут поражаться и слизистые рта, языка, в таком случае нередко образование могнущих трещин и язв. Периферические нейропатии также протекают неспецифично и могут быть представлены различными нарушениями чувствительности (покалывание, жжение, чувство холода, болезненные ощущения), в тяжелых случаях возможно развитие мышечной слабости и нарушения со стороны двигательной сферы. У детей с дефицитом витамина В6 отмечаются более частые инфекции, снижается эмоциональная устойчивость, они быстрее устают, им тяжелее дается усвоение новых навыков и знаний. В литературе описаны случаи возникновения лимфопении (снижения количества лимфоцитов), оксалурии (повышенное выделение оксалатов с мочой) и развития мочекаменной болезни у пациентов с нарушенным метаболизмом пиридоксина.
Дети получающие терапию противосудорожными препаратами или изониазидом на длительной основе угрожаемы по развитию витамин В6-дефицитных состояний!
В большинстве случаев диагноз устанавливается клинически, однако возможны специфические тесты по определению ферментативной активности эритроцитов, нагрузочные пробы с триптофаном.
Если на то нет специальных указаний, профилактику гиповитаминоза В6 можно не проводить, достаточно разнообразия и полноценности диеты ребенка.
Лечение проводится таблетированными формами витамина В6 или комплексами витаминов группы В и фолиевой кислоты, а в некоторых случаях – применяются внутримышечные инъекции пиридоксина. Наиболее частым осложнением (побочным эффектом) терапии пиридоксином является аллергия, однако описаны случаи развития судорог, периферических нейропатий, а также лекарственного гепатита у пациентов, получавших высокие дозы витамина В6.
Данный материал предназначен для родителей и рассчитан на лиц старше 18 лет, имеющих образование не ниже чем полное среднее/ среднее специальное и свободно владеющих русским языком. Он не является пособием по диагностике, лечению или тактике ведения того или иного заболевания или состояния, не может являться учебным пособием для студентов или других учащихся и представлен лишь с ознакомительной целью. В целях безопасности Вашего ребенка некоторые специфические аспекты диагностики и терапии заболеваний или состояний были умышленно опущены.
Не пытайтесь самостоятельно устанавливать у ребенка диагноз. Не пытайтесь лечить ребенка самостоятельно или по совету лиц, не имеющих юридического и морального права на лечение детей. Помните, Ваши взгляды, оценка полученной самостоятельно медицинской информации могут быть непрофессиональны и заведомо ошибочны, а действия – нанести вред Вашему ребенку. Если у Вас есть вопросы/сомнения/подозрения/опасения по поводу состояния здоровья Вашего ребенка, пожалуйста, обратитесь к врачу, имеющему действующий профессиональный сертификат и допущенному к работе с детьми. Если состояние Вашего ребенка кажется Вам угрожающим – не сомневайтесь – вызовите Врача или позвоните в Скорую Медицинскую Помощь.
Источник
Источники и пути обезвреживания аммиака в разных тканях
П
д

аминокислот в кишечнике азотистых оснований


С

Восстановительное аминирование Образование аммонийных солей (в почках)
-кетоглутарата (в мозге)
Дезаминирование остальных аминокислот осуществляется путем трансдезаминирования, т. е непрямого дезаминирования. Трансдезаминирование — это сочетание двух процессов:
а) трансаминирование любой аминокислоты с -кетоглутаровой и получение глутаминовой а/к (фермент трансаминаза),
б) последующее прямое окислительное дезаминирование глутамата с образованием аммиака, воды, 3 АТФ, (фермент ГДГ).
Таким образом, прямое окислительное дезаминирование и трансдезаминирование приводят к образованию в тканях свободного аммиака (есть и другие пути, приводящие к освобождению аммиака).
Свободный аммиак даже в небольших количествах токсичен для человека и, особенно для ткани мозга. Могут возникать симптомы аммиачного отравления – головокружение, спутанная речь, тошнота и в тяжелых случаях даже коматозное состояние.
В тканях существуют механизмы его обезвреживания:
в ткани мозга основной путь обезвреживания и удаления аммиака происходит с участием -кетоглутарата:
а) восстановительное аминирование (фермент ГДГ, NН3, кофактор НАДФНН )
с образованием глутаминовой кислоты;
б) амидирование глутаминовой кислоты (а также аспарагиновой) с образованием глутамина (фермент глутаминсинтетаза) с последующим транспортом его в печень и почки, где происходит освобождение амидного азота (аммиака) с помощью гидролитического фермента глутаминазы.
Но главный путь обезвреживания аммиака происходит в печени, где этот токсический продукт азотистого обмена превращается в высокорастворимое нетоксичное соединение –мочевину, которая поступает в кровь и выводится из организма с мочой.
Схема орнитинового цикла


N
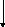


Знание метаболического процесса превращения аммиака в мочевину в печени (орнитиновый цикл Кребса-Хензелайта) имеет важное значение для объяснения и понимания биохимической основы некоторых патологических состояний. При патологии печени (гепатит, цирроз, отравления фосфором, мышьяком) функция печени снижается, в результате аммиак накапливается в крови, развивается гипераммониемия с определенными клиническими симптомами. Наследственные нарушения, вызываемые частичным блокированием одной из реакций цикла мочевинообразования, также приводят к увеличению концентрации аммиака в крови и появлению некоторых промежуточных метаболитов (цитрулинемия, аргининемия).
Малобелковая диета может приводить к снижению содержания аммиака в крови и улучшению клинической картины наследственных нарушений.
Таким образом, при поражениях печени, почек важно определять содержание мочевины в крови и моче, знать эти показатели в норме и правильно оценивать полученные данные.
При циррозе печени часто наблюдаются нарушения функций центральной нервной системы: снижение памяти, нарушение ориентировочных и поведенческих реакций. Накопление какого метаболита в нервной ткани может быть причиной таких расстройств? Ответ накопление аммиака, так как при циррозе печени нарушается детоксикацонная функция печени
При дефиците витамина В6 у детей возникают судороги, которые довольно быстро исчезают при парэнтеральном введении пиридоксина. Имеется ли связь между дефицитом витамина В6, нарушением метаболизма аминокислот и возникающими судорогами? Ответ: витамин В6 в качестве кофактора ПАЛФ катализирует декарбоксилирование глу, при этом образуется ГАМК, — тормозной нейромедиатор, при его недостатке развиваются судороги
В эксперименте на животных обнаружено, что в печени снижена активность фермента аргиназы. К чему это может привести? Ответ: аргиназа – заключительный фермент орнитинового цикла, может привести к повышению содержания аргинина, а в конечном счете, аммиака
У ребенка одного года резко снижен уровень мочевины и повышен уровень аммиака. Как можно назвать такое состояние? Объясните возможный механизм изменений. Ответ: состояние, при котором повышено содержание аммиака в крови –гипераммониемия, (см зад 1)
У больных сахарным диабетом развивается отрицательный азотистый баланс, а с мочой экскретируется повышенное количество мочевины. Почему? Ответ: при сахарном диабете глюкозы в клетке не хватает, на энергетические нужды начинает использоваться липиды и белки, которые катаболизирует на аминокислоты, при этом активно вступают в процессы трансдезаминирования, при этом образуется свободный аммиак, который обезвреживается в орнитиновом цикле с образованием мочевины, которая выводится с мочой.
При питании взрослого человека в основном белками растительного происхождения (вегетарианство) наблюдается отрицательный азотистый баланс. Почему? ответ Механизм отрицательного азотистого баланса очень похож на ответ зад 5, с той разницей, что при вегетарианстве причиной катаболизма собственных внутриклеточных белков является недостаток всех незаменимых аминокислот в растительной пище, а следовательно — и в клетке. Назовите возможные причины гипераммониемий
Объясните механизм действия больших доз аргинина при наследственном дефекте аргининосукцинатлиазы (ответ: в отсутствие аргинина снизились количество орнитина в клетках и скорость цикла синтеза мочевины)
Крысам, голодавшим в течение 12 часов, дали аминокислотную смесь. Содержащую все а/к, за исключением аргинина. Через 2 часа содержание аммиака у животных в крови возросло до 140 (мкг/л и появились клинические симптомы гипераммониемии( кома, судороги). В контрольн. Группе животных, получавших полную смесь а/к, симптомов не наблюдалось
а) почему отсутствие аргинина привело к гипераммониемии?
Б) напишите реакцию. Скорость которой снижается в отсутствие аргинина. Назовите фермент
В) можно ли аргинин заменить орнитином?
Ответ: А) в отсутствие аргинина снизились количество орнитина в клетках и скорость цикла мочевинообразования
Б) аргинин— мочевина+ орнитин (фермент Аргиназа)
Источник