Витамин – д – дефицитный рахит
Витамин – Д – дефицитный рахит (ВДДР) связан с недостатком поступления витамина Д с пищей или нарушения его образования из 7 – дегидрохолестерина в коже под влиянием УФО. Рахит является мультифакторным заболеванием, так как разбалансировка кальций регулирующих механизмов может быть вызвана многими причинами эндогенного и экзогенного характера.
Экзогенные причины развития рахита: недостаточное поступление витамина Д с пищей, низкая инсоляция.
Эндогенные: нарушение всасывания в кишечнике витамина Д, кальция, фосфора, нарушение метаболизма витамина Д в печени и почках, нарушение реабсорбции кальция и фосфора в почках и др.
Со стороны матери к развитию рахита предрасполагают: неудовлетворительные жилищные условия, юный возраст матери и возраст старше 35 лет, частые беременности с коротким интервалом, аборты, гестозы, экстрагенитальная патология: обменные заболевания, патология желудочно – кишечного тракта, почек, вредные привычки, дефекты в питании (дефицит белка, кальция, фосфора, витаминов Д, В1, В2, В6, таких микроэлементов, как магний, цинк, железо, медь, кобальт, участвующих в построении костной ткани), гиподинамия, недостаточное пребывание на солнце и свежем воздухе, особенно во время беременности.
Со стороны ребенка к развитию рахита предрасполагают:
— время рождения (июнь – декабрь),
— масса при рождении (более 4 кг),
— быстрая прибавка в массе в первые 3 месяца жизни,
— недостаточное пребывание на свежем воздухе;
— недостаточный двигательный режим: тугое пеленание, отсутствие ЛФК и массажа;
— перинатальная энцефалопатия с поражением третьего желудочка;
— заболевания кожи, печени, почек, синдром мальабсорбции, частые ОРВИ, кишечные инфекции;
— прием противосудорожных препаратов (фенобарбитал и др.).
Рахит особенно часто встречается у недоношенных детей, чему в значительной степени содействует гипоксически – ишемеческие повреждения головного мозга. Гипоксия отрицательно сказывается на метаболизме клеток, повреждая их мембраны. У таких детей нередко отмечается длительная гипокальциемия, являющаяся фоном, на котором развивается рахит.
У недоношенных детей по сравнению с доношенными, частота заболевания рахитом значительно выше. Это обусловлено уменьшенным запасом витамина Д, кальция и фосфора, недостаточной минерализацией скелета, более выраженной склонностью к ацидозу, гипопротеинемией, низким уровнем лимонной кислоты в сыворотке крови, увеличенной потребностью в кальции и фосфоре вследствие усиленного роста после рождения, нарушением всасывания в кишечнике жиров и витамина Д, незрелостью ферментных систем печени и почек, частыми инфекционными болезнями и желудочно – кишечными расстройствами.
Физиологическая роль витамина Д.
Витамин Д и его активные метаболиты являются структурными единицами гормональной системы, регулирующей фосфорно-кальциевый обмен. Многокомпонентную регуляцию фосфорно-кальциевого гомеостаза в основном осуществляют паратгормон, витамин Д и кальцитонин. Физиологические колебания кальция и фосфора поддерживаются в довольно узких границах: от 2 до 2,8 ммоль/л. Гипокальциемия немедленно активирует синтез паратиреоидного гормона, который усиливает выведение кальция из костной ткани в кровь, а также экскрецию фосфора почками в результате уменьшения его реабсорбции в почечных канальцах и сохраняя таким образом нормальное соотношение кальция и фосфора.
Имеется 7 разновидностей витамина Д1 – 7, которые обнаружены в продуктах растительного и животного происхождения. Наибольшей биологической активностью обладают витамины Д3 (животного происхождения) – холекальциферол и витамин Д2 (растительного происхождения) – эргокальциферол.
Существуют 2 пути поступления витамина Д в организм ребенка: с пищей и путем его образования в коже под влиянием ультрафиолетовых лучей с длиной волны 280 – 310 микрометров. При этом провитамин Д7 – дегидрохолестерин превращается в витамин Д3. Витамины Д2 и Д3, как таковые, не обладают биологической активностью. Для того чтобы оказать физиологическое действие на органы – мишени, они должны подвергнуться 2 ферментативным гидроксилированиям. Одна часть поступающего после кишечного всасывания или кожного синтеза витамина Д фиксируется в жировых тканях и мышцах, представляя собой резервную форму, другая – переносится в печень. Печеночное активирование витамина Д происходит путем гидролиза в позиции 25 посредством печеночного фермента и его трансформации в кальцидиол (25 – ОН – Д3). В почках митохондриальный фермент 1a — гидроксилаза трансформирует 25 – ОН – Д3 в 1.25 (ОН)2 – Д3 (кальцитриол). Этот метаболит затем поступает в слизистую кишечника, где вызывает образование кальций связывающего белка (СаСб). Последний, способствует всасыванию кальция в кишечнике, обеспечивая потребность организма в кальции и фосфоре. Кальцитриол является наиболее активным натуральным метаболитом Д и расценивается как гормон.
Таким образом, витамину Д принадлежит важная роль в поддержании гомеостаза кальция, обеспечении в организме положительного кальциевого баланса, нормальной работе цикла Кребса.
В условиях гипокальциемии витамин Д действует на кость аналогично паратгормону — временно увеличивает резорбцию костной ткани, одновременно усиливая всасывание кальция из кишечника. После восстановления кальция в крови до нормы витамин Д улучшает качество костной ткани: способствует увеличению количества остеобластов, уменьшает кортикальную порозность и резорбцию кости. Рецепторы к 1,25(ОН) 2 Д3 имеют клетки многих органов, обеспечивая универсальную регуляцию ферментных внутриклеточных систем. Механизм регуляции следующий: 1,25(ОН)2 витамин Д3 активирует соответствующий рецептор, далее в передаче сигнала участвуют посредники – аденилатциклаза и цАМФ, мобилизующие кальций и его связь с белком – кальмодулином. Конечный эффект – усиление функции клетки и, следовательно, органа.
Кальцидиол является промежуточным метаболитом, не оказывающим влияние на метаболизм костной ткани. По уровню содержания его в крови (в норме – 20 – 40 нг/ мл) судят о насыщенности организма витамином Д. Образование кальцидиола нарушается при заболеваниях печени.
Паратгормон является вторым надежным регулятором кальций – фосфорного обмена. Сигналом для повышения продукции паратгормона служат: снижение концентрации ионизированного кальция в плазме и внеклеточной жидкости, обусловленные дефицитом витамина Д, недостаточное всасывание кальция в кишечнике, избыточная потеря ионов кальция через почки. Одновременно паратгормон подавляет реабсорбцию неорганических фосфатов в почечных канальцах, благодаря чему достаточно жестко регулируется соотношение Са : Р на ионном уровне. Избыточная продукция паратгормона сопровождается развитием гиперфосфатурии, гипофосфатемии, остеопении и остеомаляции, в тяжелых случаях – остеопороза.
Третий регулятор кальциевого обмена – кальцитонин. Он подавляет резобцию кости, усиливает отложение кальция в кость и его выведение из организма с мочой. В регуляции кальциевого обмена также принимают участие гормоны щитовидной железы (тироксин, трийодтиронин), эстрогены, андрогены, соматотропный гормон, инсулин, и другие, окончательная роль которых уточняется. Рахит сопровождается нарушением не только минерального, но и белкового, липидного, углеводного, витаминного обменов, что ведет к изменению функций центральной нервной системы; при этом страдают сердечно – сосудистая система, органы дыхания, кроветворения. Комплекс патологических сдвигов ослабляет организм, тормозит рост, физическое и умственное развитие ребенка, снижает резистентность детей к инфекции, угнетает иммуннокомпетентную систему. Все это создает благоприятные условия для присоединения различных заболеваний, особенно пневмонии и их не благоприятного течения.
Основными патогенетическими звеньями в развитии рахита являются дефицит витамина Д и его активных метаболитов, недостаточность кальций регулирующей системы, снижение всасывания кальция и фосфора в кишечнике, гиперпаратиреоидизм, усиленная потеря фосфора с мочой, ацидоз. Гипокальциемия немедленно активирует синтез паратиреоидного гормона, который усиливает выведение Са из костной ткани в кровь, а также экскрецию Р почками в результате уменьшения его реабсорбции в почечных канальцах. Все это приводит к нарушению процессов костеобразования, развитию остеопений и остеомаляции. Наиболее сильно поражаются те кости, рост которых наиболее интенсивен в этот период. Одним из ранних признаков нарушений костной системы является краниотабес (размягчение) задних частей теменных костей и чешуи затылочной кости. У больных рахитом отмечается позднее закрытие родничков и швов. Зубы прорезываются с большим опозданием. Во втором полугодии жизни появляются рахитические изменения: позвоночника (кифоз, сколиоз, лордоз); грудной клетки (развернутость нижней апертуры грудной клетки, деформации ее по типу «грудь сапожника», «куриная грудь», на ней определяется «гаррисонова борозда»; костей таза («плоский или клювовидный таз»); нижних конечностей («Х-образные или О-образные ноги»). Другим симптомом поражения костей является симптом остеоидной гиперплазии, проявляющийся «реберными четками», «браслетами», «нитями жемчуга». При этом происходит деминерализация костей в условиях гипокальциемии, гипоксии, гипоцитратемии, метаболического ацидоза. Нарушается синтез коллагена в условиях дефицита метаболитов витамина Д и аминоацидурии – идет избыток разрастания коллагена в кости, накопление остеоида с нарушенной структурой и отсутствием кальция.
Мышечная гипотония и электролитные сдвиги у больных рахитом сопровождаются нарушением моторики желудочно-кишечного тракта и появлениям склонности к запорам. Гипотония мышц передней брюшной стенки приводит к образованию характерного «лягушачьего живота». Увеличивается печень, селезенка.
Фосфор входит в состав ферментов, участвующих в цикле Кребса (перевод перувата в цитраты). При нарушении цикла Кребса накапливаются соли пировиноградной кислоты. Возникает дефицит цитратов, который усугубляет метаболический ацидоз. На это реагирует вегетативная нервная система – появляется вегето — дистонический синдром: повышенная возбудимость, нарушение сна, аппетита, повышенная потливость. В области затылка – облысение, зуд. Дермографизм – стойкий, красный.
В период реконвалесценции значительно улучшается общее самочувствие, исчезают вегетативные и неврологические нарушения, нормализуется содержание Р и Са в крови.
Классификация рахита была принята шестым Всесоюзным съездом детских врачей в 1947 году. Новой классификации пока не принято, но согласно методическим рекомендациям МЗ СССР от 1990 года «Профилактика и лечение рахита у детей раннего возраста» предлагается выделять степени тяжести и характер течения рахита.
Е.М.Лукьянова и соавт., в 1988 г. дополнили и систематизировали классификацию рахита и представили ее следующим образом (табл. 21).
Источник
Современный взгляд на патогенез и профилактику рахита у детей

Опубликовано в журнале:
«Практика педиатра», март 2012, с. 34-40
И.Н. Захарова, Н.А. Коровина, Ю.А. Дмитриева, ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздравсоцразвития РФ
Проблеме рахита сегодня уделяется довольно скромное внимание. Большинство научных исследований, касающихся особенностей метаболизма костной ткани и минерального обмена, посвящено преимущественно проблеме остеопороза. Некоторыми педиатрами рахит продолжает расцениваться как физиологическое состояние, не требующее коррекции.
Однако по ряду причин с таким взглядом нельзя согласиться. Младенческий рахит является не только педиатрической, но и медико-социальной проблемой, так как имеет серьезные последствия, обуславливающие высокую заболеваемость детей в старшем возрасте. Перенесенный в детстве рахит и связанное с ним нарушение накопления пиковой костной массы может предрасполагать к развитию остеопороза в последующие годы жизни. Остеопения и остеомаляция, наблюдаемые при рахите, способствуют формированию нарушений осанки, множественному кариесу зубов. Последствиями нарушения абсорбции кальция, фосфора, магния могут явиться мышечная гипотония, вегетативные дисфункции, нарушения моторики желудочно-кишечного тракта. Выявляемые при рахите дисфункции иммунитета в виде снижения уровня интерлейкинов, интерферона, показателей фагоцитоза предрасполагают к частым инфекционным заболеваниям, нарушая социальную адаптацию ребенка.
По данным статистического анализа Минздравсоцразвития РФ, показатель заболеваемости детей рахитом в России за последние 5 лет превышает 50%. Высокая частота заболевания, несмотря на активную профилактику, требует пересмотра существующих взглядов на этиологию и патогенез рахита, способы его профилактики и терапии.
Этиология
Основным этиологическим фактором развития рахита у детей считается дефицит витамина D в организме. Известно, что витамин D поступает в организм человека двумя путями: с пищей и в результате синтеза в коже под влиянием ультрафиолетовых лучей. Наиболее богатыми источниками витамина D являются печень трески, тунца, рыбий жир, в меньшей степени – сливочное масло, яичный желток, молоко. В продуктах растительного происхождения содержится его аналог – эргокальциферол (витамин D2). Всасывание витамина D происходит в основном в двенадцатиперстной и тощей кишке в присутствии желчных кислот [1].
Фотосинтез витамина D в коже осуществляется путем превращения 7-дегидрохолестерола (провитамина D3) в холекальциферол (витамин D3) под влиянием солнечного излучения и температуры кожи. Скорость фотосинтеза холекальциферола в коже составляет порядка 15–18 МЕ/см2/час, что позволяет большинству людей полностью удовлетворить потребность в нем за счет эндогенного синтеза в коже при адекватной инсоляции [2]. Однако следует учитывать, что на эффективность синтеза витамина D в коже человека существенное влияние оказывают климатические условия, географическая широта местности, уровень загрязненности воздуха, а также степень пигментации кожи. В частности, показано, что в зоне около 55° северной широты, где расположены Москва, Нижний Новгород, Казань и ряд других городов России, солнечное излучение способно обеспечить образование адекватного количества витамина D в коже лишь в течение 4 месяцев в году (с середины апреля до середины августа) [3]. Таким образом, при определенных условиях важную роль в предотвращении гиповитаминоза D играет холекальциферол, получаемый с пищей или в составе витаминных препаратов.
Патогенез
Образовавшийся в коже и поступивший из кишечника холекальциферол связывается со специфическим витамин D-связывающим белком, осуществляющим его транспортировку к местам дальнейшего метаболизма. Часть витамина D транспортируется в жировую и мышечную ткани, где он фиксируется, представляя собой резервную форму. Основное же его количество переносится в печень, где происходит первый этап трансформации – гидроксилирование с образованием кальцидиола – 25(ОН)D3, являющегося основной транспортной формой витамина D и маркером, характеризующим обеспеченность им организма. Синтез 25(ОН)D3 зависит только от количества исходного субстрата, то есть витамина D, поступившего с продуктами питания или образовавшегося в коже. Образованный в печени 25-гидроксихолекальциферол переносится с помощью D-связывающего белка в почки, где в проксимальных извитых канальцах осуществляется второй этап его трансформации, приводящий к образованию гормонально активной формы витамина D – кальцитриола (1,25(ОН)2D3) или альтернативного метаболита 24,25(ОН)2D3. В условиях дефицита кальция и фосфора в организме метаболизм 25(ОН)D3 идет по пути образования 1,25(ОН)2D3, основной эффект которого направлен на повышение сывороточной концентрации кальция путем усиления его абсорбции из кишечника и реабсорбции в почках, а также посредством резорбции кальция из костей. Процесс образования кальцитриола катализируется ферментом альфа-1-гидроксилазой, присутствующей в митохондриях клеток почечных канальцев. При нормальной или повышенной концентрации кальция и фосфора в сыворотке крови нарастает активность фермента 24-гидроксилазы, под действием которой образуется альтернативный метаболит 25(ОН)D3 – 24,25(ОН)2D3, обеспечивающий фиксацию кальция и фосфора в костной ткани.
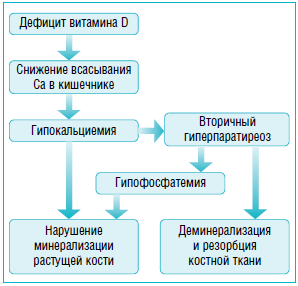
В условиях дефицита витамина D уменьшается синтез кальцитриола, следствием чего является снижение абсорбции кальция в кишечнике. Развивающаяся при этом гипокальциемия активирует синтез паратиреоидного гормона. В условиях вторичного гиперпаратиреоза усиливается резорбция костной ткани с целью поддержания нормокальциемии, а также увеличивается реабсорбция кальция в почках и экскреция фосфатов (рис.). Усиление всасывания кальция в кишечнике носит временный характер, так как этот процесс осуществляется посредством активации паратгормоном синтеза 1,25(ОН)2D3 в почках, однако в условиях дефицита исходного субстрата (25(ОН)D3) процесс образования кальцитриола будет также нарушаться [1, 4].
Рисунок
Патогенез витамин-D-дефицитного рахита
Дефицит кальция, фосфатов и повышенная резорбция костной ткани в условиях вторичного гиперпаратиреоидизма являются ключевыми патогенетическими моментами формирования типичных для рахита костных изменений. В дистальных отделах зон роста при рахите отмечаются значительные изменения, выражающиеся в неспособности новообразованного остеоида адекватно минерализоваться. Пролиферация и гипертрофия хрящевых клеток приводит к разрастанию метафизарных пластинок, что проявляется в виде типичных для рахита деформаций костей черепа, появления «рахитических четок». Таким образом, в условиях гиповитаминоза D в структуре костного метаболизма отмечается преобладание процессов резорбции над новообразованием костной ткани, приводящее к отложению остеоида при отсутствии его адекватной минерализации. При сохраняющемся дефиците витамина D кости скелета теряют свою прочность и подвергаются деформации за счет сокращения мышц и тяжести собственного тела.
Клинические проявления витамин-D-дефицитного рахита обычно сочетаются с характерными биохимическими изменениями в виде гипокальциемии, гипофосфатемии, повышения активности щелочной фосфатазы, а также выраженного снижения уровня 25(ОН)D3 вплоть до его полного отсутствия в крови [1].
Учитывая роль гиповитаминоза D в патогенезе рахита, детям раннего возраста рекомендовано проведение специфической профилактики заболевания препаратами витамина D в дозе 500 МЕ ежедневно на протяжении осеннее-зимне-весеннего периода [5]. При этом, несмотря на практически повсеместно проводимую профилактику, частота рахита в России остается высокой [6]. Наряду с этим, в последнее время появляются данные о том, что симптоматика рахита у детей раннего возраста не всегда коррелирует с содержанием витамина D в организме, а в ряде случаев заболевание развивается и при нормальном уровне 25(ОН)D3 в сыворотке крови [7, 8]. Это требует активного поиска дополнительных факторов, участвующих в развитии рахитического процесса с целью оптимизации профилактики и лечения заболевания у детей.
Высокая напряженность процессов остеогенеза в раннем возрасте ставит костную ткань ребенка в критическое положение по отношению к любым неблагоприятным воздействиям внешней среды и, в первую очередь, к дефициту различных макрои микронутриентов в составе рациона питания. В настоящее время в патогенезе рахита большая роль уделяется дефициту кальция. Результаты современных исследований позволяют предположить, что при дефиците кальция в рационе ребенка потребность в витaмине D существенно возрастает, что предрасполагает к развитию заболевания у детей с нормальным уровнем 25(ОН)D3 [9]. В основе патогенеза рахита при дефиците кальция в рационе питания может лежать ускорение метаболизма 25-гидроксихолекальциферола в целях повышения уровня 1,25(ОН)2D3 [10]. В данной ситуации резко возрастает потребность в витамине D, и, в случае отсутствия дополнительного поступления холекальциферола в организм, содержание 25(ОН)D3 снижается до уровня, соответствующего гиповитаминозу. Таким образом, нарушение минерализации кости в растущем организме может возникнуть как в случае дефицита витамина D при адекватном поступлении кальция, так и при дефиците кальция в условиях достаточной обеспеченности организма холекальциферолом.
Существенная роль в возникновении рахита принадлежит дефициту или несбалансированности белкового компонента питания. Имеются данные, что качественная и количественная белковая недостаточность, дефицит незаменимых аминокислот и гиповитаминоз D приводят к однонаправленным изменениям в метаболизме кальция и фосфора, а также в структуре костной ткани. На фоне данных состояний отмечается уменьшение содержания витамин-D-зависимого кальций-связывающего белка в слизистой тонкой кишки, снижение скорости всасывания макро- и микроэлементов в пищеварительном тракте и минерализации костной ткани [11].
Нарушения фосфорно-кальциевого обмена могут возникать и в условиях изменения липидного состава рациона питания, влияющего на секрецию желчи, играющей важную роль в процессе усвоения кальция, фосфора и витамина D. Более того, некоторые жирные кислоты способны образовывать с кальцием нерастворимые соли и выводить их с калом, что также может приводить к гипокальциемии и нарушению процессов минерализации при избыточном потреблении жиров [11].
Неполноценность углеводного состава пищи также существенно влияет на фосфорно-кальциевый обмен и химическую структуру скелета. В трудах отечественных исследователей ранее указывалось, что рахит легче возникает и тяжелее протекает у детей, получающих избыточное количество однообразных, богатых углеводами продуктов. Это связано с тем, что фитиновая кислота, содержащаяся в злаках, образует с кальцием нерастворимые соли, что нарушает процесс усвоения минерала [12].
Помимо гиповитаминоза D, большую роль в нарушении костного метаболизма играет дефицит ряда витаминов и микроэлементов, в частности аскорбиновой кислоты, ретинола, витаминов группы В, магния, марганца, цинка, кремния. Данные микронутриенты принимают активное участие в механизмах ремоделирования кости, образования костной матрицы, влияют на активность синтеза паратгормона, определяют структуру ядерных рецепторов к кальцитриолу [13].
Факторы риска
Большинство отечественных исследователей свидетельствуют о существовании определенных факторов риска, наличие которых может предрасполагать к развитию рахитического процесса [1, 14, 15]. Значимым компонентом в патогенезе заболевания являются неблагополучные социально-экономические условия проживания матери, недостаточное пребывание беременной женщины и ребенка на свежем воздухе, ухудшение экологических условий в крупных городах. Немаловажную роль в развитии рахита играют перенесенные ребенком частые инфекционные заболевания, способствующие возникновению пищевых дефицитов на фоне снижения аппетита и повышенных эндогенных затрат. Кроме того, возникновение метаболического ацидоза на фоне заболевания повышает растворимость фосфорно-кальциевых солей и препятствует нормальной минерализации костной ткани [15].
Неблагополучное течение беременности у матери, задержка внутриутробного развития плода, недоношенность, морфофункциональная незрелость могут явиться причинами замедления созревания ферментативных систем, что в конечном счете приведет к нарушению фосфорно-кальциевого обмена, метаболизма витамина D и развитию клиники рахита даже в условиях адекватной специфической профилактики. Способствовать развитию рахита может патология со стороны органов, участвующих в обмене холекальциферола в организме младенца (желчевыводящие пути, печень, почки, кишечник, кожа). Известно, что предрасположенность к рахиту выше у младенцев, имеющих высокие темпы роста и прибавки в массе в первые месяцы жизни. В такой ситуации высокая потребность в кальции может быть обеспечена только при адекватном уровне кальцитриола в сыворотке, повышенное образование которого требует ускорения метаболизма исходного субстрата – 25(ОН)D3, что, в свою очередь, приводит к быстрому истощению метаболита в тканевых депо и сыворотке крови [7]. Указанные факторы риска могут способствовать развитию эндогенного гиповитаминоза D даже при достаточном поступлении холекальциферола в организм ребенка.
Следует отметить, что в современных условиях те или иные особенности материнского и младенческого анамнеза можно выявить у большинства детей, однако рахит развивается не во всех случаях. В этой связи определенный интерес представляет выделение наиболее значимых факторов риска развития рахита в настоящее время с целью их своевременного выявления и коррекции при проведении профилактических и терапевтических мероприятий. В ходе анализа анамнестических данных 117 детей с рахитом и 62 здоровых младенцев, нами было установлено, что среди описанных факторов наиболее значимыми на современном этапе являются ускоренные темпы прибавки в массе и росте на первом году жизни, а также сопутствующие заболевания со стороны органов, участвующих в метаболизме витамина D. Указанные факторы были выявлены более чем у 50% детей с рахитом, при этом определялись у них достоверно чаще (p ® Комфорт. Рассматривая достоинства современных молочных смесей, следует все же отметить, что суточный объем питания, обеспечивающий физиологическую потребность ребенка в витамине D, достигается только к 5–6-месячному возрасту, а клиника рахита развивается в начале первого полугодия жизни ребенка. Таким образом, в условиях недостаточной инсоляции, низкого содержания витамина D в грудном молоке и недостаточного его поступления в организм младенца на ранних этапах искусственного вскармливания для профилактики рахита и гиповитаминоза D большое значение имеет дополнительное назначение холекальциферола.
Согласно методическим рекомендациям МЗ 1990 года, оптимальной профилактической дозой витамина D для детей раннего возраста в настоящее время является 500 МЕ, которая назначается начиная с 4–5-недельного возраста в осеннее-зимне-весенний период детям, вскармливаемым грудным молоком, в течение первого и второго года жизни. Детям из группы риска по развитию заболевания (при наличии сопутствующей патологии со стороны почек или желудочно-кишечного тракта или ускоренных темпов роста ребенка), в соответствии с данными рекомендациями, показано назначение холекальциферола в дозе 1000 МЕ в течение месяца с последующим переходом на 500 МЕ в сутки [5].
Список литературы находится в редакции.
Сведения об авторах:
Ирина Николаевна Захарова, заведующая кафедрой педиатрии ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздравсоцразвития РФ, профессор, д-р мед. наук
Нина Алексеевна Коровина, профессор кафедры педиатрии ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздравсоцразвития РФ, д-р мед. наук
Юлия Андреевна Дмитриева, ассистент кафедры педиатрии ГБОУ ДПО «Российская медицинская академия последипломного образования» Минздравсоцразвития РФ
Источник