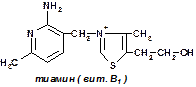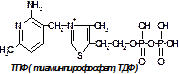Коферменты, характеристика, связь с витаминами.
Коферменты — это органические вещества, как правило, аминокислотной природы, непосредственно участвующие в катализе в составе фермента. Простые, относятся обычно к классу гидролаз, практически все гидролитические ферменты состоят только из
аминокислот, т.е. являются простыми белками. Кроме того, некоторые лиазы, а вот все остальные классы ферментов в основном явл. сложными белками, т.е. для каталитической активности многих ферментов кроме белковой части необходим второй компонент получивший название кофактор. Есть каталитически активный фермент вместе с
кофактором получил название холофермент. Это каталитически активный фермент, состоящий из белковой и небелковой части кофактора. Белковая часть холофермента получила название апофермент.
Характерной особенностью холофермента или сложных ферментов протеидов является, то, что ни белковая часть апофермента, ни кофактор в отдельности не обладают заметной каталитической активностью. Какую же роль выполняют тот и другой?
Оказывается апофермент резко повышает каталитическую активность кофактора, а кофактор в свою очередь стабилизирует белковую часть, делает ее более устойчивой и менее уязвимой к денатурирующим агентам. Поэтому встает вопрос, что и какие вещества явл. кофакторами?
Роль кофакторов, как выяснилось, играют большинство витаминов или соединений построенных с их участием, но не только витамины выступают в роли кофакторов. Кроме того, это некоторые полипептиды, группы нуклеотидов и их производные и, наконец, ионы некоторых металлов. Последние годы в соответствии с химической природой кофакторов появилась классификация:
1. Кофакторы жирного ряда (глютатион, липоевая кислота, долихол фосфат).
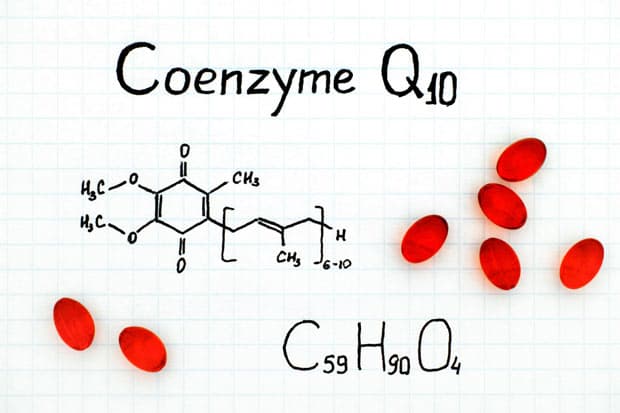
2 Кофакторы алифатического ряда (убихинон или коэнзим Q).
3. Кофакторы гетероциклического ряда а) содержащие витамины (B1) тиоминлирофосфат (В6) перидоксальфосфат (В7) биоцетин (В9) тетрогидрофолат содержащий фоливую кислоту (фолиум — лист) 6) не содержащие витаминов геминовые кофакторы. Основой этих кофакторов является гемовое железо
4. Кофакторы-нуклеотиды а) содержащие витамины содержащие витамин В2 (флавинмононуклеотид ) (фляос — желтый) (флавинадениндинукле отид) НАД, НАДФ (РР или В5) HSKoA (пантотеновая кислота ВЗ) Кобамидные коферменты (В 12) содержат кобальт б) нуклеотиды не витамины АТФ, уридиндифосфорноглюкуроновая кислота (УДФК), фосфоаденозинфосфосульфат (ФАФС) — активная фосфорная кислота, (ЦТФ) цитидинтрифосфорная кислота. Ф-ции: АТФ участвует в переносе адениловой и фосфорной кислоты, участвует в реакциях аденилирования и фосфолирирования ФАФС участвует в переносе сульфогрупп УДФК участвует в переносе глюкуроновой кислоты ЦТФ участвует в активации холина и фосфотидной кислоты. Процессы идущие при биосинтезе фосфолипидов.
5 Кофакторы ионов металлов Fe, Mn, Zn, К, Na, Mg, Ca, Сu.
Не нашли, что искали? Воспользуйтесь поиском:
Источник
Коферменты . Их роль. связь с витаминами
Коферменты в каталитических реакциях осуществляют транспорт различных групп атомов, электронов или протонов. Коферменты связываются с ферментами: ковалентными связями; ионными связями; гидрофобными взаимодействиями и т.д. Один кофермент может быть коферментом для нескольких ферментов. Многие коферменты являются полифункциональными (например, НАД, ПФ). В зависимости от апофермента зависит специфичность холофермента. Все коферменты делят на две большие группы: витаминные и невитаминные.
Коферменты витаминной природы – производные витаминов или химические модификации витаминов.
Сюда относят:флавинмононуклеотид (ФМН); флавинадениндинуклеотид (ФАД).Ребитол и изоалоксазин образуют витамин В2. Витамин В2 и остаток фосфорной к-ты образуют ФМН
ФМН в соединении с АМФ образуют ФАД.
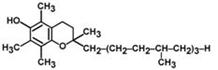
Витамин Е
антистерильный витамин, антиоксидантный энзим.
В химическом плане это альфа-, бета-, гамма- и дельта-токоферолы, но преобладающим является альфа-токоферол.
Витамин Е устойчив к нагреванию.
Роль витамина Е в обмене веществ
1. регулирует интенсивность свободно-радикальных реакций. Препятствует перекисному окислению липидов биомембран;
2. повышает активность витамина А.
Суточная потребность витамина Е 20-25 мг. Источники витамина Е: растительные масла (!), а также печень, желток яиц, проросшие зерна; масло облепихи.
Гемоглобин
Гемоглобин входит в состав группы белков гемопротеины, которые сами являются подвидом хромопротеинов и подразделяются на неферментативные белки (гемоглобин, миоглобин) и ферменты (цитохромы, каталаза, пероксидаза). Небелковой частью их является гем – структура, включающая в себя порфириновое кольцо (состоящее из 4 пиррольных колец) и иона Fe2+. Железо связывается с порфириновым кольцом двумя координационными и двумя ковалентными связями.
№15
АДФ,АТФ
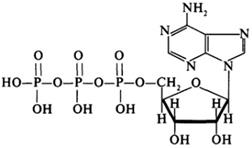
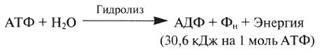
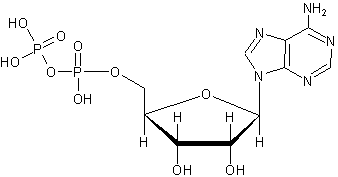
АТФ (Аденозинтрифосфа́т)
Значение АТФ При расщеплении АТФ на АДФ и неорганический фосфат (Фн) высвобождается энергия:
Помимо энергетической АТФ выполняет в организме ещё ряд других не менее важных функций:
-Вместе с другими нуклеозидтрифосфатами АТФ является исходным продуктом при синтезе нуклеиновых кислот.
-Кроме того, АТФ отводится важное место в регуляции множества биохимических процессов. Являясь аллостерическим эффектором ряда ферментов, АТФ, присоединяясь к их регуляторным центрам, усиливает или подавляет их активность.
-АТФ является также непосредственным предшественником синтеза циклического аденозинмонофосфата — вторичного посредника передачи в клетку гормонального сигнала.
-Также известна роль АТФ в качестве медиатора в синапсах и сигнального вещества в других межклеточных взаимодействиях (пуринергическая передача сигнала
Аденозиндифосфат (АДФ) — нуклеотид, состоящий из аденина, рибозы и двух остатков фосфорной кислоты. АДФ образуется в результате переноса концевой фосфатной группы АТФ. АДФ участвует в энергетическом обмене во всех живых организмах.
Дата добавления: 2016-06-18 ; просмотров: 3709 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ
Источник
Коферменты: что это такое, польза, применение в спорте
Коферменты представляют собой органические соединения небелковой природы, которые необходимы для функционирования многих ферментов. Большинство из них являются производными витаминов.
Причиной нарушения метаболизма и снижения синтеза полезных веществ в организме часто является снижение активности некоторых видов ферментов. Поэтому то коэнзимы столь нам необходимы.
В узком смысле, кофермент – это коэнзим Q10, производная фолиевой кислоты и некоторых других витаминов. Важное значение для организма человека имеют те коферменты, которые продуцируются витаминами группы B.
Кофермент нужен для того, чтобы повысить производительность клеточной энергии, которая нужна для поддержания жизнедеятельности. Любой процесс, который протекает в организме человека, требует колоссального энергетического ресурса, будь то умственная деятельность, работа сердечно-сосудистой или пищеварительной системы, физическая активность при нагрузке на опорно-двигательный аппарат. Благодаря реакции, в которую коферменты вступают с ферментами, продуцируется необходимая энергия.
Функции коферментов
Коферменты представляют собой небелковые соединения, которые способствуют активации потенциала ферментов. Они выполняют 2 основные функции:
- Участвуют в каталитических процессах. Кофермент сам по себе не вызывает в организме необходимых молекулярных превращений, в состав ферментов он входит вместе с апоферментом, и только при их взаимодействии происходят каталитические процессы связывания субстрата.
- Транспортировочная функция. Кофермент соединяется с субстратом, в результате чего образуется прочный транспортировочный канал, по которому свободно перемещаются молекулы до центра другого фермента.
Все коферменты объединяет одно важное свойство – они являются термически устойчивыми соединениями, но свойственные им химические реакции довольно сильно разнятся.
Классификация коферментов
По способам взаимодействия с апоферментом коферменты делятся на:
- Растворимые – во время реакции соединяется с молекулой фермента, после чего изменяется по химическому составу и высвобождается заново.
- Простетические – прочно связаны с апоферментом, в процессе реакции находится в активном центре фермента. Их регенерация происходит при взаимодействии с другим коферментом или субстратом.
По химической структуре коферменты делятся на три группы:
- алифатические (глутатион, липоевая кислота и др.)
- гетероциклические (пиридоксальфосфат, тетрагидрофолиевая кислота, нуклеозидфосфаты и их производные (КоА, ФМН, ФАД, НАД и др.), металлопорфириновые гемы и др.
- ароматические (убихиноны).
По функциональному признаку выделяют две группы коферментов:
- окислительно-восстановительные,
- коферменты переноса групп.
Коферменты в спортивной фармакологии
При интенсивных физических нагрузках расходуется большое количество энергии, ее запас в организме истощается, а многие витамины и питательные вещества потребляются гораздо быстрее, чем вырабатываются. Спортсмены испытывают физическую слабость, нервное истощение, нехватку сил. Для того чтобы помочь избежать многих симптомов были разработаны специальные препараты с коферментами в составе. Их спектр действия очень широк, назначаются они не только спортсменам, но и людям с достаточно серьезными заболеваниями.
Кокарбоксилаза
Кофермент, который образуется только из поступающего в организм тиамина. У спортсменов он служит средством профилактики перенапряжения миокарда, расстройств нервной системы. Препарат назначается при радикулитах, невритах, а также острой печеночной недостаточности. Вводится внутривенно, разовая доза не должна быть менее 100 мг.
Кобамамид
Заменяет по действию функционал витамина B12, является анаболиком. Помогает спортсменам нарастить мышечную массу, увеличивает выносливость, способствует быстрому восстановлению после занятий. Выпускается в форме таблеток и растворов для внутривенного введения, суточная норма составляет 3 таблетки или 1000 мкг. Длительность курса – не более 20 дней.
Оксикобаламин
По своему действию схож с витамином B12, но намного дольше держится в крови и гораздо оперативнее преобразуется в коферментную формулу благодаря прочному соединению с плазменными белками.
Пиридоксальфосфат
Для препарата характерны все свойства витамина B6. От него он отличается быстрым терапевтическим эффектом, назначается к приему даже при нарушении фосфорилирования пиридоксина. Принимается три раза в день, суточная доза составляет не более 0,06 гр, а курс – не дольше месяца.
Пиридитол
Активизирует метаболические процессы центральной нервной системы, повышает проходимость глюкозы, препятствует избыточному образованию молочной кислоты, повышает защитные свойства тканей, в том числе устойчивость к гипоксии, которая возникает во время интенсивных спортивных тренировок. Принимают препарат три раза в день по 0,1 гр. после завтрака в течение месяца
Пантогам
Является гомологом пантотеновой кислоты, ускоряет обменные процессы, снижает проявление болевых реакций, повышает устойчивость клеток к гипоксии. Действие препарата направлено на активацию работы головного мозга, повышение выносливости, показан к применению при черепно-мозговых травмах различного типа. Таблетки принимаются в течение месяца по 0,5 гр не чаще трех раз в день.
Карнитин
Выпускается в форме препарата для инъекций, действие которых направлено на активацию жирового обмена, ускорение регенерации клеток. Оказывает анаболическое, антигипоксическое и антитиреоидное действие. Является синтетическим заменителем витамина B6. Эффективен в виде внутривенной капельницы.
Флавинат
Образуется в организме из рибофлавина, активно участвует в углеводном, липидном и аминокислотном обмене. Выпускается в виде раствора для внутримышечных инъекций, так как его усвоение в желудке неэффективно при нарушении всасывания рибофлавина.
Липоевая кислота
Нормализует углеводный обмен. Повышает скорость окисления углеводов и жирных кислот, что способствует повышению энергетического запаса.
Подписывайтесь на наш канал в Яндекс.Дзен!
Источник
77.Коферменты и их связь с витаминами
Коферменты, или коэнзимы — малые молекулы небелковой природы, специфически соединяющиеся с соответствующими белками, называемыми апоферментами, и играющие рольактивного центра или простетической группы молекулы фермента.
Комплекс кофермента и апофермента образует целостную, биологически активную молекулу фермента.
Роль коферментов нередко играют витамины или их метаболиты (чаще всего — фосфорилированные формы витаминов группы B). Например, коферментом фермента карбоксилазы являетсятиаминпирофосфат, коферментом многих аминотрансфераз — пиридоксаль-6-фосфат.
В роли кофактора могут выступать витамины. Например, кофактором АлАТ и АсАТ является витамин В6. витамин В1 –входит в состав мультиферментного комплекса, таким образом участвует в реакции окислительного декарбоксилирования ПВК и альфакетоглутарата. Витамин РР входит в состав НАД – никотинамидалениндинуклеотида, а витамин В2 в состав ФМН – флавин6мононуклеотида.
78. Регуляция действия ферментов: 1) частичный протеолиз – пепсиноген в пепсин под действием HCl, трипсиноген в трипсин под действием энтерокиназы, химотрипсиноген в химотрипсин под действием трипсина 2) ковалентная модификация – фосфорилирование (присоединение остатка фосфорной кислоты) и дефосфорилирование – пример – 2 фосфорилаза Б не активная + 4 АТФ 1 фосфорилаза А – Рн + 4 АДФ. И может быть все наоборот. Гликогенсинтетаза активная + АТФ гликогенсинтетаза – Рн не активная + АДФ. Адреналин повышает уровень глюкозы в крови и активируется фосфорилаза и расщепляется гликоген.
79.Активаторы ферментов: ионы Ме с 19 по 30 в системе Менделеева, восстановленные формы соединений НАДН2 ФАДН2, аллостерические активаторы, гормоны – адреналин, инсулин.
Ингибирование ферментов: 1) обратимое: а) конкурентное – когда ингибитор похож на субстрат (аллопуринол) б) не конкурентное – аллостерическое (ретроингибирование) и уменьшение доли субстрата
2) необратимое: а) специфическая – СО на цитохромы б) не специфическая – денатурация при t 0 С.
80. Классификация ферментов 1961 год – 5 международный конгресс в Москве: 1) оксидоредуктазы (имеют 5 подклассов) в основе ОВР; 2) трансферазы –перенос амино и метильной групп; 3) гидролазы – все ферменты пищеварительного тракта; расщепление с участием воды; 4) лиазы – расщепление связей без участия воды; 5) изомеразы – превращение глюкозо6фосфат в фруктозо6фосфат — реакции изомеризации; 6) лигазы (синтетазы) – синтез органических веществ с затратой энергии распада АТФ.
КФ 1: Оксидоредуктазы, катализирующие окисление или восстановление. Пример: каталаза, алкогольдегидрогеназа
КФ 2: Трансферазы, катализирующие перенос химических групп с одной молекулы субстрата на другую. Среди трансфераз особо выделяют киназы, переносящие фосфатную группу, как правило, с молекулы АТФ.
КФ 3: Гидролазы, катализирующие гидролиз химических связей. Пример: эстеразы, пепсин, трипсин, амилаза, липопротеинлипаза
КФ 4: Лиазы, катализирующие разрыв химических связей без гидролиза с образованием двойной связи в одном из продуктов.
КФ 5: Изомеразы, катализирующие структурные или геометрические изменения в молекуле субстрата.
КФ 6: Лигазы, катализирующие образование химических связей между субстратами за счет гидролиза АТФ. Пример: ДНК-полимераза
81. Энергетический обмен, катаболизм, источники восстановленных эквивалентов. Совокупность окислительных реакций, происходящих в живых организмах и обеспечивающих их энергией и метаболитами, необходимыми для осуществления процессов жизнедеятельности, называется биологическим окислением. Функции биологического окисления: 1) энергетический обмен, поддержание t тела, мышечная активность, осмотическая работа, транспорт, биосинтез 2) окисление ксенобиотиков 3) окисление токсических продуктов обмена 4) синтез ключевых метаболитов. Основными источниками энергии для организма являются белки, липиды и углеводы, поступающие с пищей. Три стадии катаболизма: 1) специфическое превращение в мономеры – аминокислоты, моносахариды, глицерин, жирные кислоты. 2) образование унифицированных продуктов – ПВК и АцКоА (моносахариды через ПВК). 3) АцКоА в ЦТК образуется СО2, вода; 3НАДН, которые в дых цепи дают воду и 3 АТФ; ФАД Н2, который в дых цепи дает воду и 2 АТФ. Источники восстановленных эквивалентов это ЦТК, все окислительно-восстановительные реакции, бета-окисление жирных кислот. В дых цепь поступает 3НАДН и ФАДН2, они образуются в следующих реакциях: НАДФН+НАДНАДФ+НАДН (трансдегидрогеназа).
82.Митохондриальная цепь окисления водорода. трансмембранный электрохимический потенциал. Перенос 2х протонов из матрикса в межмембранное пространство сопряжен с образованием градиента концентраций протонов водорода (дельта МюН). Именно в этом месте возникает пункт сопряжения, окисления и фосфорилирования. Трансмембранный электрохимический потенциал – это разница протонов между матриксом и наружной частью. Образуется АТФ (АДФ+Фн) путем фосфорилирования с использованием энергии окисления водорода.
83. НАД-зависимые дегидрогеназы – это сложные ферменты, относящиеся к классу оксидоредуктаз и состоящие из белковой и небелковой части. Небелковая часть представлена коферментами НАД или НАДФ. НАД – никотинамидадениндинуклеотид, в его структуре два мононуклеотида, соединенные фосфоэфирной связью. В состав одного мононуклеотида входит амид никотиновой кислоты (витамин ниацин), рибоза и остаток фосфорной кислоты. Второй мононуклеотид представлен аденином, Д-рибозой и также остатком фосфорной кислоты. НАД-зависимые дегидрогеназы акцептируют от субстрата два атома водорода, первый присоединяется к НАД с образованием НАДН, второй выделяется в виде протона. Изоцитрат под действием изоцитратдегидрогеназы образуется альфа-кетоглуторат СО2 НАДН+Н + . Источники НАДН: изоцитратдегидрогеназа, малатдегидрогеназа, мультиферментный комплекс окислительного декарбоксилирования альфа-кетоглутората, бета-окисление жирных кислот.
84. Флавиновые ферменты – это сложные ферменты, состоящие из белковой и небелковой части, небелковой частью представлена простерическая группа ФМН – флавинмононуклеотид или ФАД – флавинадениндинуклеотид. ФМН состоит из витамина В2, пятиатомного спирта ретибола, остатка фосфорной кислоты; в структуре ФАД два мононуклеотида, соединенных фосфоэфирной связью. В состав одного мононуклеотида входит витамин В2, пятиатомный спирт ретибол, остаток фосфорной кислоты. Второй мононуклеотид представлен АМФ – Аденин, рибоза, остаток фосфорной кислоты.
85. Дыхательная цепь, железо-серопротеины, цитохромы. Железо-серопротеины относят к негемовым железопротеинам. Известно три вида FeS-белков: 1) один атом железа тетраэдрически связан с сульфгидрильными группами четырех остатков цистеина; 2) (Fe2S2) содержит 2 атома железа и 2 неорганических сульфида, присоединенных к четырем остаткам цистеина; 3) (Fе4S4) содержит четыре атома железа, четыре сульфгидридные группы и четыре остатка цистеина. Атом железа в этих комплексах может находиться в восстановленном (Fe ++ ) и окисленном (Fe +++ ) состояниях. НАДН-дегидрогеназа содержит второй и третий типы железо-серопротеинов. Цитохромы – это ферментные гемопротеины, транспортирующие только электроны. В качестве простетической группы они содержат гем. В дых цепи располагаются 5 цитохромов, отличающихся по строению простетических групп и имеющих разные спектры поглощения. В цитохроме b гем нековалентно связан с белковой частью, в то время как в цитохромах с и с1 – связь с белковой частью ковалентная. Цитохромы а и а3 имеют иную простетическую группу, называемую гемом-а. Она отличается от простетической группы цитохромов с и с1 наличием формильной группы вместо одной из метильных групп и углеводородной цепью вместо одного из остатков винила. В составе цитохромов а и а3 находятся два атома меди. Простетической группой цитохромов в, с1 и с служит протопорферин 1Х. Цитохром с имеет ковалентно связанный гем и выполняет челночные функции – передает электроны цитохрома с1 к цитохромоксидазе.
86. образование макроэргических связей в дыхательной цепи. Коэффициент Р/О. Разобщение дыхания и фосфорилирования в дыхательной цепи. Коэффициент Р/О – это количество АТФ, которое образовалось в дых цепи. Р/О может быть равно 3 или 2 АТФ. Три АТФ образуется при участии НАДН, две АТФ при участии ФАДН2. В окислительном фосфорилировании не образуется дельта МюН, т.к. есть вещества, которые принимают протоны на себя. В окислительном фосфорилировании не происходит образования АТФ и энергия выделяется в виде тепла.
87. Окислительное субстратное фосфорилирование в процессе биологического окисления. Образование АТФ в процессе метаболизма идет двумя путями – окислительного и субстратного фосфорилирования. Основными источниками поставляющими энергию являются: 1) дых цепь 2) ЦТК 3) гликолиз. Возникновение макроэргической связи в момент окисления субстрата с дальнейшей активацией неорганического фосфата и его переносом на АДФ с образованием АТФ называют субстратным фосфорилированием. В данном случае окисление субстрата связано с фосфорилированием АДФ. Примерами реакций субстратного фосфорилирования являются две реакции гликолиза – окисление 3-фосфоглицеринового альдегида в 1,3-дифосфоглицериновую кислоту, и окисление 2-фосфоглицериновой кислоты в 2-фосфоэнолпировиноградную кислоту; а также одна реакция ЦТК — окисление сукцинил-КоА в янтарную кислоту.Основная масса АТФ образуется путем окислительного фосфорилирования. В процессе окислительного фосфорилирования окисляемый субстрат участия не принимает, а активирование неорганического фосфата сопряжено с переносом электронов и протонов водорода с коферментов дегидрогеназ (принимающих участие в окислении субстрата) к молекулярному кислороду. Сопряжение окисления с фосфорилированием АДФ и последующим образованием АТФ называют окислительным фосфорилированием. Процессы сопряжения окисления и фосфорилирования идут в дых цепи.
88. Образование СО2 в процессе биологического окисления. СО2 в организме образуется двумя путями – путем прямого и окислительного декарбоксилирования. Основная масса СО2 образуется в ЦТК. Первая молекула СО2 образуется путем прямого декарбоксилирования изоцитрата, при этом изоцитратдегидрогеназа обладает декарбоксилирующим эффектом. Вторая молекула СО2 путем окислительного декарбоксилирования альфа-кетоглутората. Одна молекула СО2 образуется в результате окислительного декарбоксилирования ПВК. Человек за сутки выделяет около 500 мл СО2.
89. Виды декарбоксилирования в ЦТК. В ЦТК есть только два типа декарбоксилирования – прямое и окислительное. 1) Прямое декарбоксилирование изоцитрата под действием изоцитратдегидрогеназы, которая обладает декарбоксилирующим эффектом, превращается в альфа-кетоглуторат и НАДН, который является источником водорода для дыхательной цепи, окисление которого приводит к образованию 3х АТФ и воды. Кроме того в этой реакции образуется СО2. 2) Окислительное декарбоксилирование альфа-кетоглутората происходит под действием альфа-кетоглуторатдегидрогеназного комплекса, который включает три фермента и пять кофакторов – ТДФНSКоА, НАД, ФАД, липоевая кислота. Продуктом реакции является образование макроэргического соединения – сукцинил-КоА. В результате этой реакции образуется еще одна молекула восстановительного эквивалента НАДН и СО2.
90. Микросомальное окисление также как митохондриальное, происходит в митохондриях. Но в микросомальном окислении кислород используется с пластической целью, он включается в субстрат. Примерами микросомального окисления являются – окисления ксенобиотиков, синтез стероидных гормонов, активных форм витаминов, жирных кислот, холестерина. Источником водорода в микросомальном окислении служит НАДФН. При микросомальном окислении энергии не образуется.
91. Пути использования, токсичность кислорода, механизмы защиты. 1) митохондриальные окисления – образование воды – оксидазный способ. 2) в микросомальным окислением с пластической целью – оксигеназный способ. 3) для образования Н2О2 – пероксидазный способ. Токсичность кислорода связано с тем, что в ходе окислительных реакций кислород может принимать дополнительный электрон и превращаться в супероксидный радикал (анион). Присоединение двух дополнительных электронов к супероксидному аниону (О2 — ) ведет к образованию пероксидных анионов (О2 -2 ). О2 — +е+2Н + Н2О2; О2 — е+О2. В результате реакции дисмутации, катализируемой супероксиддисмутазой (СОД), образуется перикись водорода: О2 — +О2 — +2Н + Н2О2+О2. Такие формы кислорода имеют высокую химическую активность, реагируют со многими веществами в организме, в том числе с нуклеиновыми кислотами, белками, липидами, оказывая повреждающее действие. Активные формы кислорода запускают цепные реакции перекисного окисления липидов. В процессе ПОЛ образуются органические перекиси. ПОЛ приводит к повреждающему воздействию мембран клеток. Активные формы кислорода образуются в организме и в реакциях неферментативного окисления ряда веществ. В связи с тем, что образование активных форм кислорода ведет к повреждающему эффекту, можно говорить о токсичности кислорода и механизмах защиты. Имеется два способа защиты: 1) ферментативные пути – активируют пероксидаза и каталаза. Пероксиды выступают в роли акцепторов водорода, донорами которых являются органические субстраты. 2Н2О22Н2О+О2 (катализирует каталаза). 2) неферментативные пути – используются препараты-ловушки активных форм О2 – витамин Е, К, различные хиноны.
Источник