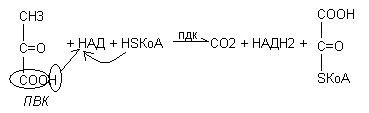Окислительное декарбоксилирование пирувата
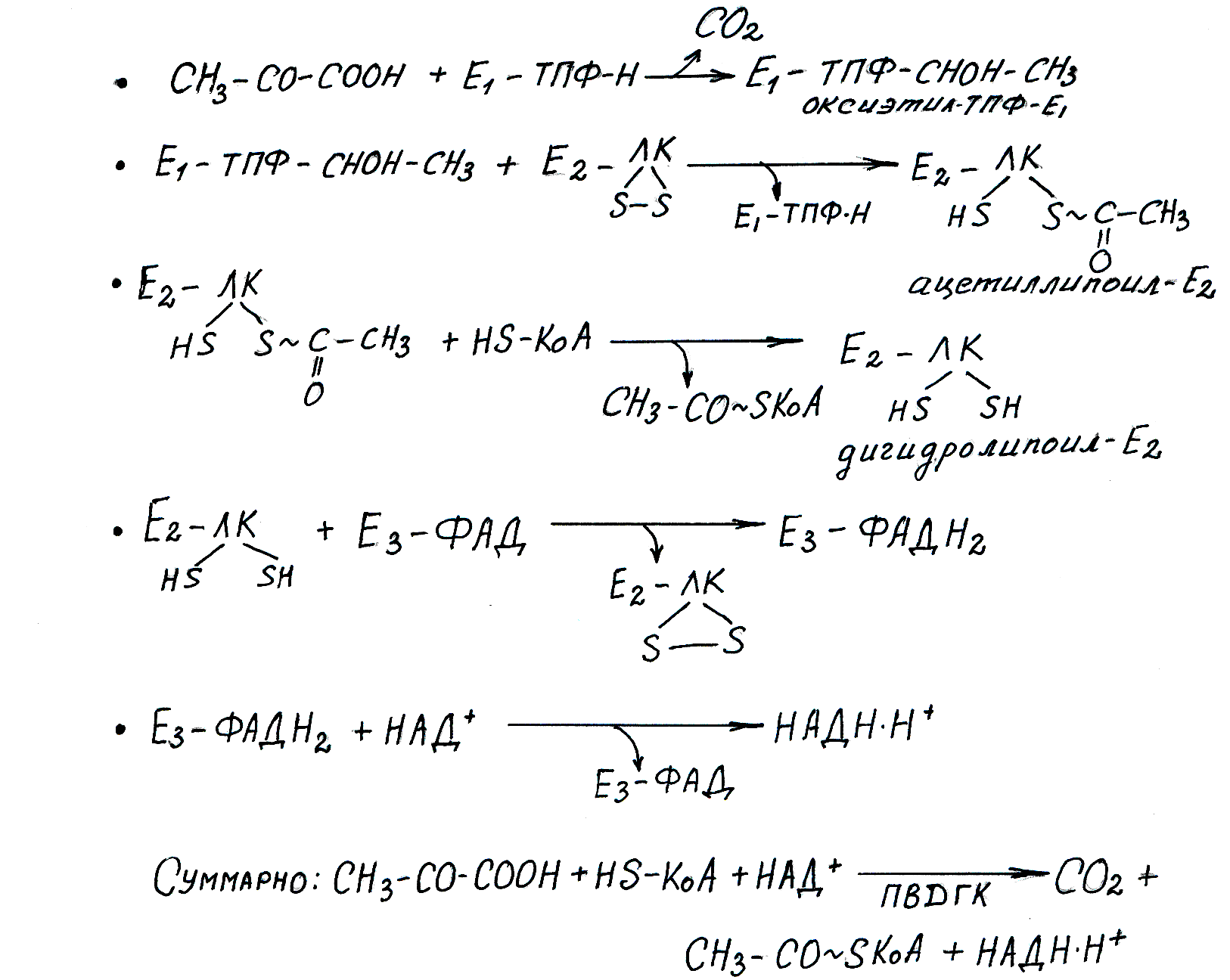
Осуществляется при участии набора ферментов, объединенных в пируватдегидрогеназный комплекс (ПВДГК).Это мультиферментная система, которая включает 3 фермента и 5 коферментов (все они являются водорастворимыми витаминами) (рис. 6.4).
Е1— пируватдекарбоксилаза. Коферментом является активная форма витамина В1, тиамина — ТПФ (тиаминпирофосфат).
Е2— дигидролипоилацетилтрансфераза. Коферментом является витаминоподобноевещество — липоевая кислота (липоил), которая может временно превращаться в дигидролипоил, присоединив 2 атома водорода. Липоил может также переносить ацетильные остатки.
С этим ферментом также работает активная форма пантотеновой кислоты — КоА-SH, которая принимает ацетильный остаток от липоевой кислоты.
Е3— дигидролипоилдегидрогеназа. Коферментом является ФАД — активная форма витамина В2, рибофлавина. С работой этого фермента связан также кофермент НАД + — активная форма витамина РР, никотиновой кислоты.
Рис. 6.4. Реакции окислительного декарбоксилирования пирувата
ПВГДК состоит из трех ферментов и пяти коферментов: Е1 – ТПФ-Н — пируватдекарбоксилаза (ТПФ — тиаминпирофосфат, активная форма витамина В1); Е 2 – ЛК — дигидролипоилацетилтрансфераза (ЛК — активная форма липоевой кислоты — витаминоподобного соединения); Е3 – ФАД — дигидролипоилдегидрогеназа (ФАД — флавинадениндинуклеотид — активная форма витамина В2); КоА-SH — активная форма пантотеновой кислоты; НАД + — никотинамидадениндинуклеотид — активная форма никотиновой кислоты. Схема регуляции ПВГДК предствалена на рисунке 6.5.
Таким образом, в результате образуются конечные продукты — СО2, атомы водорода для дыхательной цепи в составе НАДН·Н + и макроэргическое соединение ацетил-КоА. Лимитирующей реакцией в этом процессе является пируватдекарбоксилазная реакция. Поскольку фермент Е1в качестве кофермента использует ТПФ, при недостатке тиамина в пище нарушается окисление пирувата — процесса, который поставляет клеткам энергию. Возникает энергодефицит, что требует коррекции нарушения метаболизма с помощью тиамина.
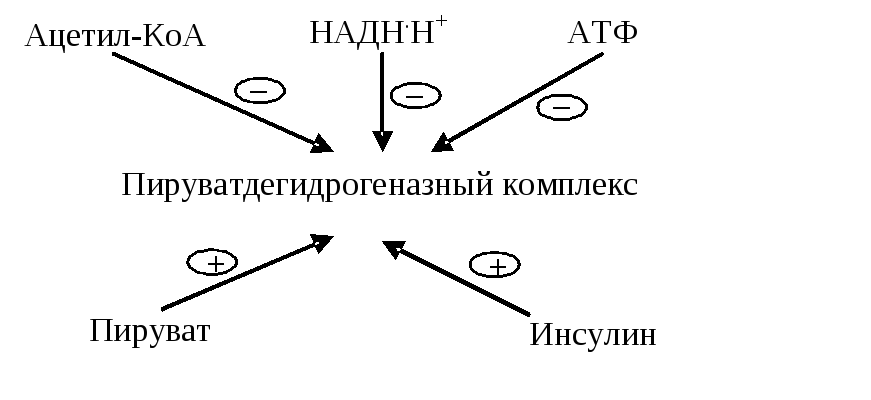
Рис. 6.5. Регуляция пируватдегидрогеназного комплекса
Лимоннокислый цикл Кребса, цикл трикарбоновых кислот (цтк)
Цикл лимонной кислоты локализован в матриксе митохондрий. Это циклический процесс из восьми последовательных реакций, в результате которых происходит декарбоксилирование и дегидрирование ацетил-КоА (универсального клеточного топлива) (рис. 6.6).
Цикл начинается с конденсации ацетил-КоА с 4-х углеродной кетокислотой — щавелевоуксусной (ЩУК). В результате образуется трикарбоновая кислота, цитрат. Изомеризация цитрата ведет к образованию изоцитрата. В ходе последовательных реакций изоцитрат декарбоксилируется и одновременно дегидрируется (фермент изоцитратДГ). Образовавшийся -кетоглутарат также декарбоксилируется и дегидрируется. Образовавшийся макроэрг сукцинил-КоА служит источником энергии для синтеза АТФ (субстратное фосфорилирование в цикле Кребса). В результате еще двух дегидрирований (ферменты сукцинатДГ и малатДГ) ЩУК регенерирует и запускает новый оборот цикла Кребса.
Таким образом, наряду с конечным продуктом обмена — СО2в четырех дегидрогеназных реакциях трижды восстанавливается НАД + (изоцитратДГ,-кетоглутаратДГ, малатДГ) и один раз восстанавливается ФАД (сукцинатДГ). Чтобы цикл мог функционировать, необходимо окислить эти коферменты, т. е. передать атомы водорода вдыхательную цепь,где происходит их окисление кислородом до воды.
Источник
Окислительное декарбоксилирование пировиноградной кислоты



Если в процессе катаболизма белков, жиров, углеводов образуется ПВК, для дальнейшего окисления необходим переход её в ацетил КоА. Этот процесс называется окислительным декарбоксилированием пировиноградной кислоты. В нём заключено два вида реакций: окисление и образование СО2 путём разрушения карбоксильной группы. Окислительное декарбоксилирование пирувата осуществляется при участии пируватдегидрогеназного комплекса.
Состав полиферментного пируватдегидрогеназного комплекса
Пируватдегидрогеназный комплекс (ПДК) молекулярной массой 6*10 6 дальтон, включает в себя три вида ферментов (Е1-Е3) и пять видов коферментов. 2 кофермента НАД и HS-КоА находятся в свободном состоянии и входят в состав комплекса только в момент реакции. Общий вид реакции окислительного декарбоксилирования пирувата:
Ферменты пируватдегидрогеназного комплекса:
Е1 – пируватдегидрогеназа (пируватдекарбоксилаза)
Е2 – дигидролипоилацетилтрансфераза (трансацетилаза)
Коферменты пируватдегидрогеназного комплекса:
- Тиаминдифосфат (ТДФ, ТПФ), содержащий витамин В1, кофактор пируватдегидрогеназы.
- Липоевая кислота, кофактор трансацетилазы.
- Кофермент ФАД, содержащий витамин В2, кофактор дегидрогеназы дигидролипоевой кислоты.
- Кофермент НАД, содержащий витамин РР.
- Кофермент НS-КоА, содержащий аденин, рибозу, два остатка фосфорной кислоты, пантотеновую кислоту (витамин В3).
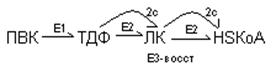
Окислительное декарбоксилирование ПВК протекает в несколько стадий, в процессе которых двухуглеродный фрагмент, образующийся из ПВК, переносится на липоевую кислоту, а затем на HS-КоА.
Биологическая роль окислительного декарбоксилирования пирувата заключается в том, что оно является важным этапом катаболизма, позволяющим включаться в цикл Кребса тем веществам, при распаде которых образуется ПВК. Образовавшаяся молекула НАДН2 окисляется в длинной дыхательной цепи с образованием 3-х молекул АТФ. Окислительное декарбоксилирование пирувата протекает внутри митохондрий.
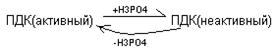
Регуляция пируватдегидрогеназного комплекса осуществляется путём фосфолирирования, дефосфолирирования пируватдегидрогеназы
Активаторами ПДК служат АДФ и НАД окисленный. Ингибиторами этого комплекса являются АТФ и НАДН2..
Источник
35. Окислительное декарбоксилирование пировиноградной кислоты. Состав пируватдегидрогеназного комплекса. Роль в этом процессе витаминов в1 и в3.
В аэробных условиях пировиноградная кислота подвергается окислительному декарбоксилированию с образованием ацетилКоА. Это превращение катализируется надмолекулярным пируватдегидрогеназным комплексом, локализованным в матриксе митохондрий. В состав пируватдегидрогеназного комплекса входят три различных фермента: пируватдекарбоксилаза, дигидролипоатацетилтрансфераза и дегидрогеназа дигидролипоевой кислоты, их количественные соотношения в составе комплекса зависят от источника выделения, как правило это соотношение приближается к 30:1:10.
Первый фермент этого комплекса пируватдекарбоксилаза ( Е1)
катализирует реакцию: СН3СОСООН + ТДФЕ1 > СО2 + СН3 СТДФ(тиаминдифосфат)Е1с образованием углекислого газа и активированного ацетальдегида, связанного с тиаминдифосфатом простетической группой фермента.
Второй фермент дигидролипоатацетильрансфераза ( Е2 ) катализирует два последовательных превращения:
а) на первом этапе идет перенос активированного остатка ацетальдегида на простетическую группу фермента липоевую кислоту, причем этот перенос сопровождается одновременным окислением альдегидной группы до карбоксильной группы
б) на втором этапе остаток ацетила переносится с липоевой кислоты, жестко связанной с ферментом, на свободный HSКоА:
Образуются ацетилКоА и фермент Е2 с восстановленной формой кофермента.
Третий фермент дегидрогеназа дигидролипоевой кислоты катализирует превращение восстановленной формы липоевой кислоты предыдущего фермента в окисленную форму, при окислении глюкозы образуется 2 молекулы пирувата, что следует учесть при написании суммарного уравнения окислительного декарбоксилирования пирувата:
2Пируват +2НАД+ +2HSКоА >2АцетилКоА +2НАДН+Н+ +2СО2
В ходе окисления 2 моль пирувата высвобождается около 120 ккал энергии, из них около 100 ккал накапливается ввиде энергии восстановленного НАД. Остальная энергия рассеивается в виде теплоты.
Превращение пирувата в ацетилКоА в ходе функционирования пируватдегидрогеназного комплекса необратимо, посколько сопровож дается потерей 11,5 ккал/моль энергии в расчете на 1 моль окис ленного пирувата.
Контроль интенсивности потока метаболитов по пируватдегидрогеназному комплексу осуществляется за счет работы двух механизмов: ковалентной модификации и аллостерической модуляции
Фосфорилирование усиливается при высоких соотношениях АТФ/АДФ, НАДН/НАД+ и ацетилКоА/КоА. Иначе говоря, активность комплекса снижается, если клетка хорошо обеспечена энергией
Образовавшийся ацетилКоА, как уже неоднократно упоминалось. поступает в цикл трикарбоных кислот, работа которого сопряжена с функционированием цепи дыхательных ферментов. При функционирова нии этих двух метаболических путей остаток ацетила окисляется до углекислого газа и воды.
36. Анаэробный распад глюкозы в клетках (гликолиз), последовательность реакций до образования лактата. Физиологическое значение этого процесса, его регуляция. Роль анаэробного распада глюкозы и гликогена в мышцах. Утилизация молочной кислоты в организме.
Человек является аэробным организмом, так как основным конечным акцептором отщепляемых от окисляемых субстратов атомов водорода является кислород. Парциальное давления кислорода в тканях составляет в среднем 3540 мм рт. ст. Торможение окислительных процессов при дефиците кислорода связано с тем, что клеточный пул НАД+ и других коферментов. способных акцептировать атомы водорода от окисляемых субстратов, весьма ограничен. Как только основная их масса переходит в восстановленное состояние из за дефицита кислорода, дегидрирование субстратов прекращается. Развивается гипоэнергетическое состояние, которое может стать причиной гибели клеток.
В подобного рода условиях в клетках различных органов и тканей включаются механизмы, обеспечивающие клетки энергией, не за висящие от наличия кислорода. Основными из них являются анаэробное расщепление гликогена и гликогенолиз. В анаэробных условиях расщепление глюкозы и гликогена идет абсолютно идентичными по сравнению с метаболическими путями до образования пирувата. Однако далее эти пути расходятся: если в аэробных условиях пируват подвергается окислительному декарбоксилированию, то в анаэробных условиях пировиноградная кислота восстанавливается в молочную кислоту. Реакция катализируется ферментом лактатдегидрогеназой.
Поскольку в ходе лактатдегидрогеназной реакции используются молекулы НАДН+Н+, ранее образовавшиеся при окислении 3фосфогли цериноваго альдегида в 1,3дифосфоглицериновую кислоту,
расщепление глюкозы до лактата сопровождается высвобождением лишь 1/12 — 1/13 всей заключенной в химических связях глюкозы энергии (
50 ккал/моль ), тем не менее на каждую распавшуюся в ходе анаэробного гликолиза молекулу глюкозы клетка получает 2 молекулы. При гликогенолизе клетка получит 3 молекулы АТФ на каждый остаток глюкозы из молекулы гликогена ( 1 АТФ расходуется и 4 АТФ синтезируется ). Несмотря на очевидную невыгодность в отношении количества высвобождаемой энергии анаэробные гликолиз и гликогенолиз позволяют клеткам существовать в условиях отсутствия кислорода.
Суммарное уравнение гликолиза:
Глюкоза + 2 АДФ + 2 Н3РО4Д> 2 Лактат + 2 АТФ + 2 Н2О Анаэробный путь окисления глюкозы и анаэробное расщепление гликогена играют важную роль в обеспечении клеток энергией, во первых, в условиях высокой экстренно возникающей функциональной нагрузки на тот или иной орган или организм в целом. Во вторых, эти процессы играют большую роль в обеспечении клеток энергией при гипоксичеких состояниях, например, при тромбозах артерий в период до развития коллатерального кровообращения или при тяжелых шоковых состояниях с выраженными расстройствами гемодинамики.
Активация анаэробного окисления углеводов приводит к увеличению продукции лактата в клетках и тканях. При сохранении кровообращения этот наработанный в клетках лактат выносится кровью и основная его часть метаболизируется в печени или в сердечной мышце. В миокарде лактат окисляется до углекислого газа и воды; в печени же лишь примерно 1/5 поступающего лактата подвергается окислению до конечных продуктов, а 4/5 ресинтезируются в глюкозу в ходе интенсивно идущего в печени процесса глюконеогенеза.
Если же вынос лактата из гипоксической ткани невозможен, то при его накоплении в клетках за счет повышения концентрации про тонов ингибируется фосфофруктокиназа, в результате чего ингибируются и гликолиз, и гликогенолиз. Клетки, лишенные последних источников энергии, обычно погибают, что наблюдается при инфарктах различных органов, в особенности при инфаркте миокарда.
Следует заметить, что в клетках некоторых органов и тканей человека образование молочной кислоты происходит и в обычных, т.е. в аэробных условиях. Так. в эритроцитах, не имеющих митохондрий. все необходимое для них количество энергии вырабатывается в ходе гликолиза. К тканям с относительно высоким уровнем аэробного гликолиза относятся также сетчатка глаза и кожа. Высокий уровень аэробного гликолиза присущ также многим опухолям.
Источник
Окислительное декарбоксилирование пировиноградной кислоты
Окисление пирувата до ацетил-КоА происходит при участии ряда ферментов и коферментов, объединенных структурно в мультиферментную систему, получившую название «пируватдегидрогеназный комплекс».
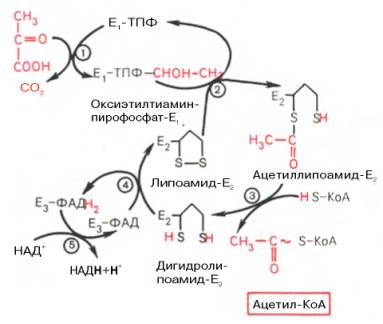
На I стадии этого процесса пируват (рис. 10.8) теряет свою карбоксильную группу в результате взаимодействия с тиаминпирофосфатом (ТПФ) в составе активного центра фермента пируватдегидрогеназы (E1). На II стадии оксиэтильная группа комплекса E1–ТПФ–СНОН–СН3 окисляется с образованием ацетильной группы, которая одновременно переносится на амид липоевой кислоты (кофермент), связанной с ферментом дигидроли-поилацетилтрансферазой (Е2). Этот фермент катализирует III стадию – перенос ацетильной группы на коэнзим КоА (HS-KoA) с образованием конечного продукта ацетил-КоА, который является высокоэнергетическим (макроэргическим) соединением.
На IV стадии регенерируется окисленная форма липоамида из восстановленного комплекса дигидролипоамид–Е2. При участии фермента дигидролипоилдегидрогеназы (Е3) осуществляется перенос атомов водорода от восстановленных сульфгидрильных групп дигидролипоамида на ФАД, который выполняет роль простетической группы данного фермента и прочно с ним связан. На V стадии восстановленный ФАДН2 дигидро-липоилдегидрогеназы передает водород на кофермент НАД с образованием НАДН + Н + .
Процесс окислительного декарбоксилирования пирувата происходит в матриксе митохондрий. В нем принимают участие (в составе сложного мультиферментного комплекса) 3 фермента (пируватдегидрогеназа, ди-гидролипоилацетилтрансфераза, дигидролипоилдегидрогеназа) и 5 кофер-ментов (ТПФ, амид липоевой кислоты, коэнзим А, ФАД и НАД), из которых три относительно прочно связаны с ферментами (ТПФ-E1, ли-поамид-Е2 и ФАД-Е3), а два – легко диссоциируют (HS-KoA и НАД).
Рис. 10.8. Механизм действия пируватдегидрогеназного комплекса.
Е1 — пируватдегидрогеназа; Е2 — ди-гидролипоилацетилтрансфсраза; Е3 -дигидролипоилдегидрогеназа; цифры в кружках обозначают стадии процесса.
Все эти ферменты, имеющие субъединичное строение, и коферменты организованы в единый комплекс. Поэтому промежуточные продукты способны быстро взаимодействовать друг с другом. Показано, что составляющие комплекс полипептидные цепи субъединиц дигидролипоил-ацетилтрансферазы составляют как бы ядро комплекса, вокруг которого расположены пируватдегидрогеназа и дигидролипоилдегидрогеназа. Принято считать, что нативный ферментный комплекс образуется путем самосборки.
Суммарную реакцию, катализируемую пируватдегидрогеназным комплексом, можно представить следующим образом:
Пируват + НАД + + HS-KoA –> Ацетил-КоА + НАДН + Н + + СO2.
Реакция сопровождается значительным уменьшением стандартной свободной энергии и практически необратима.
Образовавшийся в процессе окислительного декарбоксилирования аце-тил-КоА подвергается дальнейшему окислению с образованием СО2 и Н2О. Полное окисление ацетил-КоА происходит в цикле трикарбоновых кислот (цикл Кребса). Этот процесс, так же как окислительное декарбо-ксилирование пирувата, происходит в митохондриях клеток.
Источник