ОКИСЛИТЕЛЬНОЕ ДЕКАРБОКСИЛИРОВАНИЕ ПВК
Окислительное декарбоксилирование пировиноградной кислоты — многостадийный процесс, который катализирует пируватдегидрогеназный комплекс — митохондриальный мультиферментный комплекс, соединенный с внутренней мембраной со стороны матрикса. ПВК поступает к комплексу из матрикса, и туда же освобождаются продукты реакции.
Пируватдегидрогеназный комплекс включает три фермента (пируватдегидрогеназа (Е1), ацетилтрансфераза (Е2), дегидрогеназа дигидролипоевой кислоты (Е3)) и пять коферментов (НАД + , ФАД, тиаминпирофосфат, липоевая кислота, кофермент А (рис. 36)).
Тиаминпирофосфат связан с пируватдегидрогеназой (Е1), липоевая кислота — с ацетилтрансферазой (Е2), ФАД — с дегидрогеназой дигидролипоевой кислоты (Е3). Кофермент А и НАД + находятся в свободно растворенном состоянии.
В состав пируватдегидрогеназного комплекса входит примерно по три десятка молекул Е1 и Е2 и 10 молекул Е3. Комплекс работает как конвейер: промежуточные продукты не освобождаются в раствор, а передаются от фермента к ферменту.
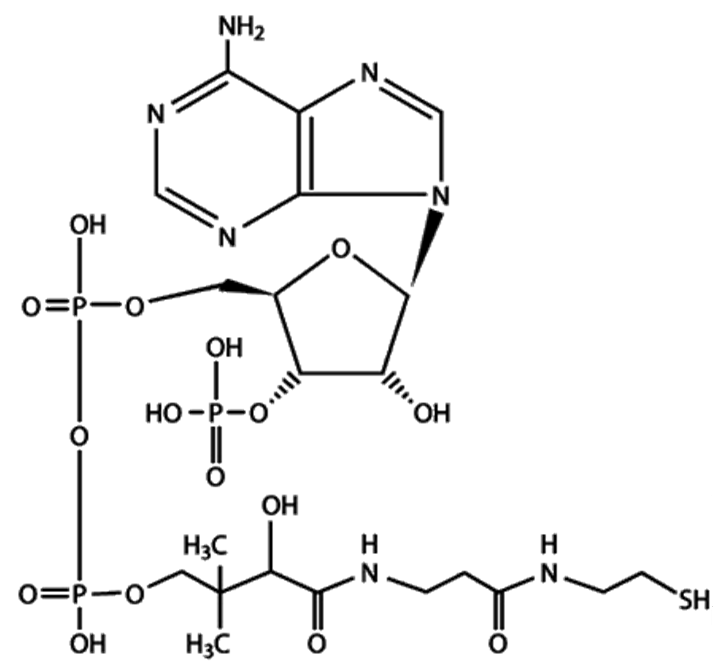 а а | 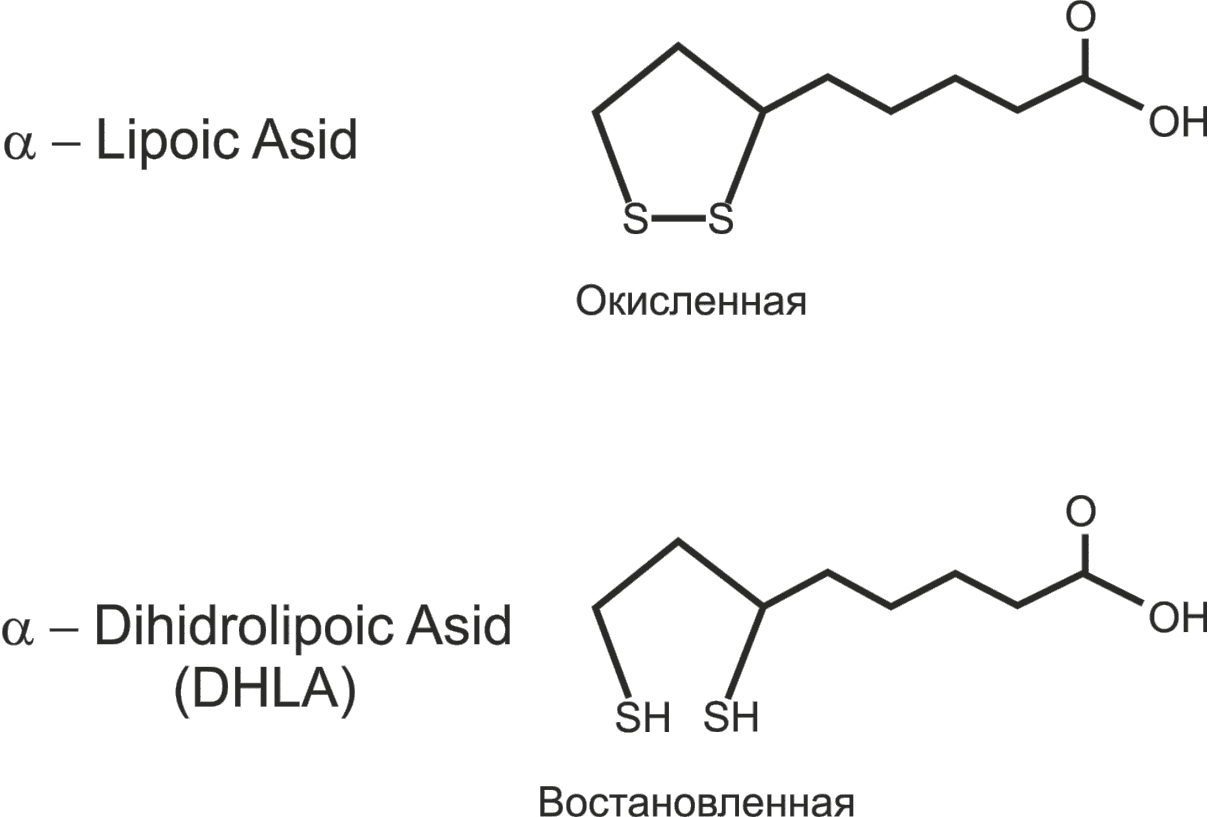 б б |
| Рис. 36. Структура кофермента А (а) и липоевой кислоты (б) |
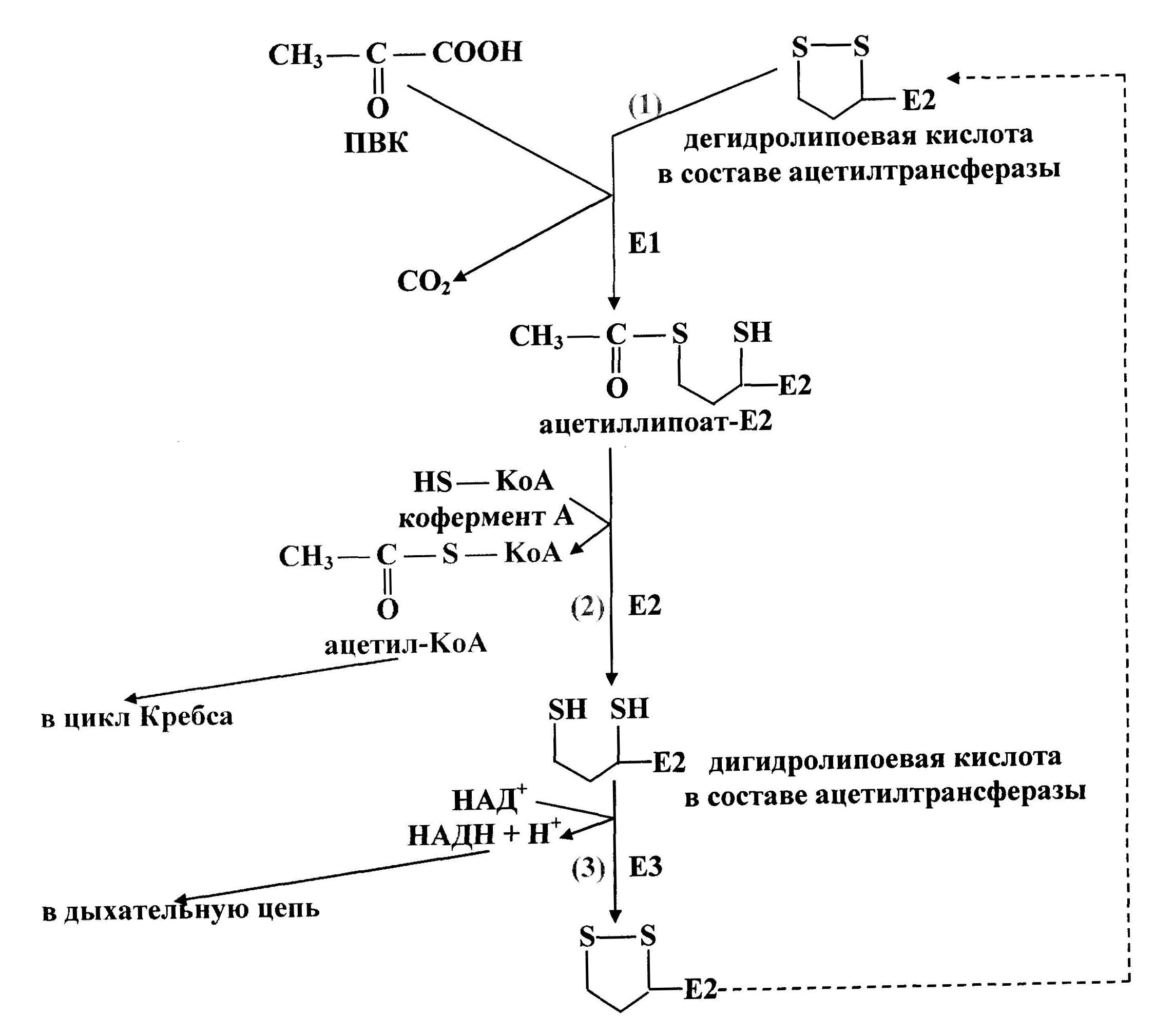
Первую реакцию (рис. 37) катализирует Е1, субстратами являются ПВК и дегидролипоевая кислота, являющаяся простетической группой Е2. От ПВК отщепляется карбоксильная группа и образуется СО2, а ацетильный остаток соединяется с атомом серы липоевой кислоты в составе ацетилтрансферазы. Образуется ацетиллипоат-Е2.
Во второй реакцииацетилтрансфераза (Е2) катализирует перенос ацетильного остатка, соединенного с его простетической группой, на коэнзим А. Продукты этой реакции — дигидролипоевая кислота в составе Е2 и ацетил-KоА.
В третьей реакциипроисходит дегидрирование дигидролипоевой кислоты в составе ацетилтрансферазы при воздействии фермента Е3 (дегидрогеназа дигидролипоевой кислоты), содержащего ФАД. ФАД передает водород на НАД + . Образуются НАДН+Н + и дегидролипоевая кислота в составе Е2. Последний фермент снова вступает в окислительное декарбоксилирование ПВК.
Ацетил-KоА (продукт второй реакции) затем окисляется в цикле Кребса. Водород с НАДН (продукт третьей реакции) поступает в дыхательную цепь, где образуется АТФ.
Энергетический выход окислительного декарбоксилирования пирувата – 3 АТФ.
Суммарное уравнение процесса:
СH3-CО-COOH + HS-KoA + НАД + ® СH3-CО-S-KoA + НАДН + Н + + СО2.
Рис. 37. Схема окислительного декарбоксилирования пирувата
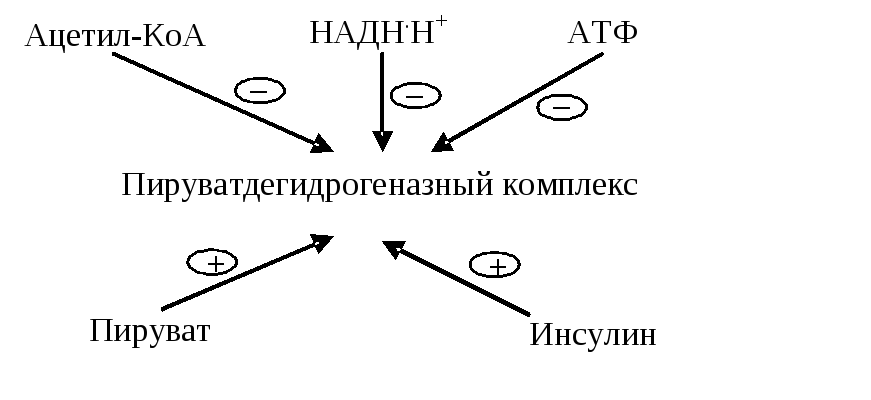
По механизму «обратной связи» работу пируватдегидрогеназного комплекса ингибируют конечные продукты окислительного декарбоксилирования — ацетил-KоА, НАДН+Н + , а также АТФ. Увеличивают активность комплекса пировиноградная кислота и АДФ.
Также имеет место гормональная регуляция: инсулин увеличивает активность пируатдегидрогеназного комплекса, глюкагон — снижает.
Источник
Окислительное декарбоксилирование пирувата
Осуществляется при участии набора ферментов, объединенных в пируватдегидрогеназный комплекс (ПВДГК).Это мультиферментная система, которая включает 3 фермента и 5 коферментов (все они являются водорастворимыми витаминами).
Е1— пируватдекарбоксилаза. Коферментом является активная форма витамина В1, тиамина — ТПФ (тиаминпирофосфат).
Е2— дигидролипоилацетилтрансфераза. Коферментом является витаминоподобноевещество — липоевая кислота (липоил), которая может временно превращаться в дигидролипоил, присоединив 2 атома водорода. Липоил может также переносить ацетильные остатки.
С этим ферментом также работает активная форма пантотеновой кислоты — КоА-SH, которая принимает ацетильный остаток от липоевой кислоты.
Е3— дигидролипоилдегидрогеназа. Коферментом является ФАД — активная форма витамина В2, рибофлавина. С работой этого фермента связан также кофермент НАД + — активная форма витамина РР, никотиновой кислоты.
Последовательность реакций, катализируемых пируватдегидрогеназным комплексом
Таким образом, в результате образуются конечные продукты — СО2, атомы водорода для дыхательной цепи в составе НАДН·Н + и богатое энергией макроэргическое соединение ацетил-КоА. Лимитирующей реакцией в этом процессе является пируватдекарбоксилазная реакция. Поскольку этот фермент в качестве кофермента использует ТПФ, при недостатке тиамина в пище нарушается окисление пирувата — процесса, который поставляет клеткам энергию. Возникает энергодефицит, что требует коррекции нарушения метаболизма с помощью тиамина.
Регуляция пируватдегидрогеназного комплекса
Лимоннокислый цикл Кребса, цикл трикарбоновых кислот (цтк)
Цикл лимонной кислоты локализован в матриксе митохондрий. Это циклический процесс из восьми последовательных реакций, в результате которых происходит декарбоксилирование и дегидрирование ацетил-КоА (универсального клеточного топлива).
Схема лимоннокислого цикла Кребса
Ферменты: 1 — цитратсинтаза; 2 — аконитаза; 3 — изоцитратдегидрогеназа; 4 — α-кетоглутаратдегидрогеназный комплекс; 5 — сукцинил-КоА синтетаза; 6 — сукцинатдегидрогеназа; 7 — фумаратгидратаза; 8 — малатдегидрогеназа.
Цикл начинается с конденсации ацетил-КоА с 4-углеродной кетокислотой — щавелевоуксусной (ЩУК). В результате образуется трикарбоновая кислота, цитрат. Изомеризация цитрата ведет к образованию изоцитрата. В ходе последовательных реакций изоцитрат декарбоксилируется и одновременно дегидрируется (фермент изоцитратДГ). Образовавшийся -кетоглутарат также декарбоксилируется и дегидрируется. Образовавшийся макроэрг сукцинил-КоА служит источником энергии для синтеза АТФ (субстратное фосфорилирование в цикле Кребса). В результате еще двух дегидрирований (ферменты сукцинатДГ и малатДГ) ЩУК регенерирует и запускает новый оборот цикла Кребса.
Таким образом, наряду с конечным продуктом обмена — СО2в четырех дегидрогеназных реакциях трижды восстанавливается НАД + (изоцитратДГ,-кетоглутаратДГ, малатДГ) и один раз восстанавливается ФАД (сукцинатДГ). Чтобы цикл мог функционировать, необходимо окислить эти коферменты, т. е. передать атомы водорода вдыхательную цепь,где происходит их окисление кислородом до воды.
Источник
Окислительное декарбоксилирование пировиноградной кислоты
Окисление пирувата до ацетил-КоА происходит при участии ряда ферментов и коферментов, объединенных структурно в мультиферментную систему, получившую название «пируватдегидрогеназный комплекс».
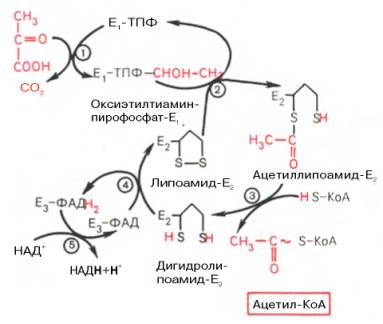
На I стадии этого процесса пируват (рис. 10.8) теряет свою карбоксильную группу в результате взаимодействия с тиаминпирофосфатом (ТПФ) в составе активного центра фермента пируватдегидрогеназы (E1). На II стадии оксиэтильная группа комплекса E1–ТПФ–СНОН–СН3 окисляется с образованием ацетильной группы, которая одновременно переносится на амид липоевой кислоты (кофермент), связанной с ферментом дигидроли-поилацетилтрансферазой (Е2). Этот фермент катализирует III стадию – перенос ацетильной группы на коэнзим КоА (HS-KoA) с образованием конечного продукта ацетил-КоА, который является высокоэнергетическим (макроэргическим) соединением.
На IV стадии регенерируется окисленная форма липоамида из восстановленного комплекса дигидролипоамид–Е2. При участии фермента дигидролипоилдегидрогеназы (Е3) осуществляется перенос атомов водорода от восстановленных сульфгидрильных групп дигидролипоамида на ФАД, который выполняет роль простетической группы данного фермента и прочно с ним связан. На V стадии восстановленный ФАДН2 дигидро-липоилдегидрогеназы передает водород на кофермент НАД с образованием НАДН + Н + .
Процесс окислительного декарбоксилирования пирувата происходит в матриксе митохондрий. В нем принимают участие (в составе сложного мультиферментного комплекса) 3 фермента (пируватдегидрогеназа, ди-гидролипоилацетилтрансфераза, дигидролипоилдегидрогеназа) и 5 кофер-ментов (ТПФ, амид липоевой кислоты, коэнзим А, ФАД и НАД), из которых три относительно прочно связаны с ферментами (ТПФ-E1, ли-поамид-Е2 и ФАД-Е3), а два – легко диссоциируют (HS-KoA и НАД).
Рис. 10.8. Механизм действия пируватдегидрогеназного комплекса.
Е1 — пируватдегидрогеназа; Е2 — ди-гидролипоилацетилтрансфсраза; Е3 -дигидролипоилдегидрогеназа; цифры в кружках обозначают стадии процесса.
Все эти ферменты, имеющие субъединичное строение, и коферменты организованы в единый комплекс. Поэтому промежуточные продукты способны быстро взаимодействовать друг с другом. Показано, что составляющие комплекс полипептидные цепи субъединиц дигидролипоил-ацетилтрансферазы составляют как бы ядро комплекса, вокруг которого расположены пируватдегидрогеназа и дигидролипоилдегидрогеназа. Принято считать, что нативный ферментный комплекс образуется путем самосборки.
Суммарную реакцию, катализируемую пируватдегидрогеназным комплексом, можно представить следующим образом:
Пируват + НАД + + HS-KoA –> Ацетил-КоА + НАДН + Н + + СO2.
Реакция сопровождается значительным уменьшением стандартной свободной энергии и практически необратима.
Образовавшийся в процессе окислительного декарбоксилирования аце-тил-КоА подвергается дальнейшему окислению с образованием СО2 и Н2О. Полное окисление ацетил-КоА происходит в цикле трикарбоновых кислот (цикл Кребса). Этот процесс, так же как окислительное декарбо-ксилирование пирувата, происходит в митохондриях клеток.
Источник
Пируват окисляется до уксусной кислоты
Пировиноградная кислота (ПВК, пируват) является продуктом окисления глюкозы и некоторых аминокислот. Ее судьба различна в зависимости от доступности кислорода в клетке. В анаэробных условиях она восстанавливается до молочной кислоты. В аэробных условиях пируват симпортом с ионами Н + , движущимися по протонному градиенту, проникает в митохондрии. Здесь происходит его превращение до уксусной кислоты, переносчиком которой служит коэнзим А.
Пируватдегидрогеназный мульферментный комплекс
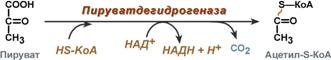
Суммарное уравнение отражает окислительное декарбоксилирование пирувата, восстановление НАД до НАДН и образование ацетил-SKoA.
Суммарное уравнение окисления пировиноградной кислоты
Превращение состоит из пяти последовательных реакций, осуществляется мультиферментным комплексом, прикрепленным к внутренней митохондриальной мембране со стороны матрикса. В составе комплекса насчитывают 3 фермента и 5 коферментов:
- Пируватдегидрогеназа (Е1, ПВК-дегидрогеназа), ее коферментом является тиаминдифосфат (ТДФ), катализирует 1-ю реакцию.
- Дигидролипоат-ацетилтрансфераза (Е2), ее коферментом является липоевая кислота, катализирует 2-ю и 3-ю реакции.
- Дигидролипоат-дегидрогеназа (Е3), кофермент – ФАД, катализирует 4-ю и 5-ю реакции.
Помимо указанных коферментов, которые прочно связаны с соответствующими ферментами, в работе комплекса принимают участие коэнзим А и НАД.
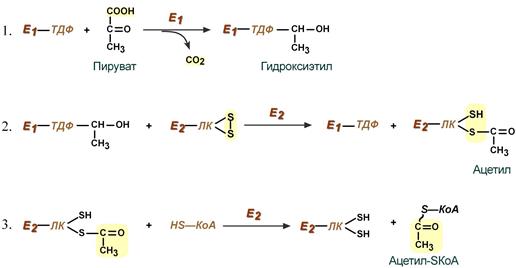
Суть первых трех реакций сводится к декарбоксилированию пирувата (катализируется пируватдегидрогеназой, Е1), окислению полученного гидроксиэтила до ацетила и переносу ацетила на коэнзим А (катализируется дигидролипоат-ацетилтрансферазой, Е2).
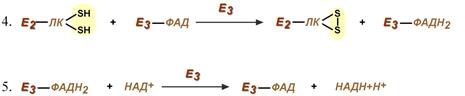
Реакции синтеза ацетил-SКоА
Оставшиеся 2 реакции необходимы для возвращения липоевой кислоты и ФАД в окисленное состояние (катализируются дигидролипоат-дегидрогеназой, Е3). При этом образуется НАДН.
Реакции образования НАДН
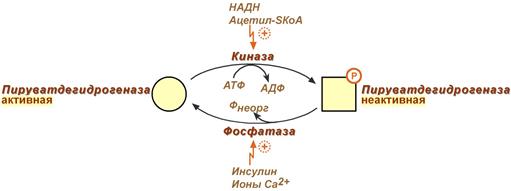
Регуляция пируватдегидрогеназного комплекса
Регулируемым ферментом ПВК-дегидрогеназного комплекса является первый фермент – пируватдегидрогеназа (Е1). Два вспомогательных фермента – киназа и фосфатаза обеспечивают регуляцию активности пируватдегидрогеназы путем ее фосфорилирования и дефосфорилирования.
Вспомогательный фермент киназа активируется при избытке конечного продукта биологического окисления АТФ и продуктов ПВК-дегидрогеназного комплекса – НАДН и ацетил-S-КоА . Активная киназа фосфорилирует пируватдегидрогеназу, инактивируя ее, в результате первая реакция процесса останавливается.
Фермент фосфатаза, активируясь ионами кальция или инсулином , отщепляет фосфат и активирует пируватдегидрогеназу.
Регуляция активности пируватдегидрогеназы
Таким образом, работа пируватдегидрогеназы подавляется при избытке в митохондрии (в клетке) ацетил-SКоА и НАДН, что позволяет снизить окисление пирувата и, следовательно, глюкозы в случае когда энергии достаточно.
Если АТФ мало или имеется влияние инсулина, то образуется ацетил-SКоА. Последний в зависимости от условий будет направляться либо в цикл трикарбоновых кислот с образованием энергии АТФ, либо на синтез холестерина и жирных кислот.
Источник
Окислительное декарбоксилирование пирувата
Осуществляется при участии набора ферментов, объединенных в пируватдегидрогеназный комплекс (ПВДГК).Это мультиферментная система, которая включает 3 фермента и 5 коферментов (все они являются водорастворимыми витаминами) (рис. 6.4).
Е1— пируватдекарбоксилаза. Коферментом является активная форма витамина В1, тиамина — ТПФ (тиаминпирофосфат).
Е2— дигидролипоилацетилтрансфераза. Коферментом является витаминоподобноевещество — липоевая кислота (липоил), которая может временно превращаться в дигидролипоил, присоединив 2 атома водорода. Липоил может также переносить ацетильные остатки.
С этим ферментом также работает активная форма пантотеновой кислоты — КоА-SH, которая принимает ацетильный остаток от липоевой кислоты.
Е3— дигидролипоилдегидрогеназа. Коферментом является ФАД — активная форма витамина В2, рибофлавина. С работой этого фермента связан также кофермент НАД + — активная форма витамина РР, никотиновой кислоты.
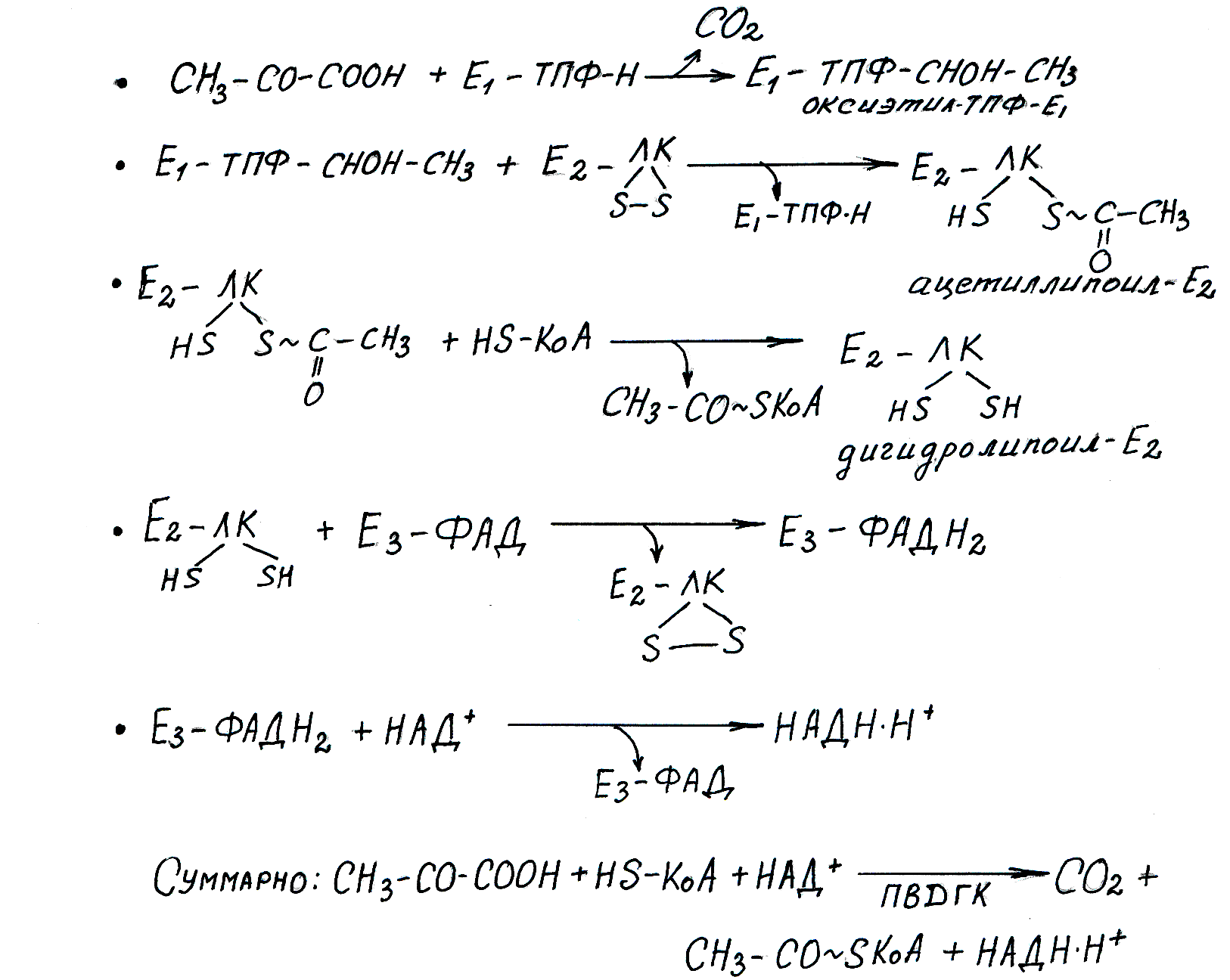
Рис. 6.4. Реакции окислительного декарбоксилирования пирувата
ПВГДК состоит из трех ферментов и пяти коферментов: Е1 – ТПФ-Н — пируватдекарбоксилаза (ТПФ — тиаминпирофосфат, активная форма витамина В1); Е 2 – ЛК — дигидролипоилацетилтрансфераза (ЛК — активная форма липоевой кислоты — витаминоподобного соединения); Е3 – ФАД — дигидролипоилдегидрогеназа (ФАД — флавинадениндинуклеотид — активная форма витамина В2); КоА-SH — активная форма пантотеновой кислоты; НАД + — никотинамидадениндинуклеотид — активная форма никотиновой кислоты. Схема регуляции ПВГДК предствалена на рисунке 6.5.
Таким образом, в результате образуются конечные продукты — СО2, атомы водорода для дыхательной цепи в составе НАДН·Н + и макроэргическое соединение ацетил-КоА. Лимитирующей реакцией в этом процессе является пируватдекарбоксилазная реакция. Поскольку фермент Е1в качестве кофермента использует ТПФ, при недостатке тиамина в пище нарушается окисление пирувата — процесса, который поставляет клеткам энергию. Возникает энергодефицит, что требует коррекции нарушения метаболизма с помощью тиамина.
Рис. 6.5. Регуляция пируватдегидрогеназного комплекса
Лимоннокислый цикл Кребса, цикл трикарбоновых кислот (цтк)
Цикл лимонной кислоты локализован в матриксе митохондрий. Это циклический процесс из восьми последовательных реакций, в результате которых происходит декарбоксилирование и дегидрирование ацетил-КоА (универсального клеточного топлива) (рис. 6.6).
Цикл начинается с конденсации ацетил-КоА с 4-х углеродной кетокислотой — щавелевоуксусной (ЩУК). В результате образуется трикарбоновая кислота, цитрат. Изомеризация цитрата ведет к образованию изоцитрата. В ходе последовательных реакций изоцитрат декарбоксилируется и одновременно дегидрируется (фермент изоцитратДГ). Образовавшийся -кетоглутарат также декарбоксилируется и дегидрируется. Образовавшийся макроэрг сукцинил-КоА служит источником энергии для синтеза АТФ (субстратное фосфорилирование в цикле Кребса). В результате еще двух дегидрирований (ферменты сукцинатДГ и малатДГ) ЩУК регенерирует и запускает новый оборот цикла Кребса.
Таким образом, наряду с конечным продуктом обмена — СО2в четырех дегидрогеназных реакциях трижды восстанавливается НАД + (изоцитратДГ,-кетоглутаратДГ, малатДГ) и один раз восстанавливается ФАД (сукцинатДГ). Чтобы цикл мог функционировать, необходимо окислить эти коферменты, т. е. передать атомы водорода вдыхательную цепь,где происходит их окисление кислородом до воды.
Источник