Образование комплексных соединений витамин в12
Цианокобаламин (Витамин В12)
CAS номер: 68-19-9
Брутто формула: C63H88CoN14O14P
Внешний вид: порошок темно-красного цвета без запаха
Химическое название и синонимы: Cyanocobalamin, Cyano-5,6-dimethylbenzimidazole-cobalamin; Vitamin B12.
Физико-химические свойства:
Молекулярная масса 1355.38 г/моль
Растворимость: в воде растворим.
pH: aq solns являются нейтральными
Давление паров: незначительное.
Плотность паров: нет.
Скорость испарения: незначительная.
Вязкость: отсутствует.
Температура замерзания / плавления:> 300 ° C
Температура разложения: недоступна.
Растворимость: умеренно растворим в воде.
Химическая стабильность: Стабилен при нормальных температурах и давлениях. Может разлагаться, когда подвергается воздействию света. Условия, которых следует избегать: свет, пыль, избыток тепла.
Несовместимость с другими материалами: сильные окислители, сильные кислоты.
Опасные продукты разложения: окись углерода, оксиды азота, оксиды фосфора, диоксид углерода, оксиды кобальта.
Витамин В12 (Кобаламин) – встречается большей степенью в печени, красном мясе, рыбе и почках. Организм человека может также сам синтезировать Витамин В12 в толстом отделе кишечника с помощью микроорганизмов, но так как всасывается витамин в подвздошной кишке, то польза от аутогенного кобаламина сомнительная.
B12 представляет собой тетрапиррольный комплекс, который содержит кобальт в молекуле и может относиться к нескольким формам кобаламина: цианокобаламин (CN-Cbl) и гидроксокобаламин (OH-Cbl) – эти формы витамина B12 доступны для медицинского использования. Аденозилкобаламин (Ado– Cbl), метилкобаламин Me-Cbl) и кобинамид (CN2-Cbn) такие формы витамина B12 обнаруживаются в биологических или пищевых образцах.
Впервые витамин был открыт в США и в Англии в 1948 году. Позже почти через 30 лет пробовали синтезировать предшественник витамина В12, но из- за сложности данного многостадийного процесса не начал производиться в крупных масштабах. Затем витамин пробовали получать непосредственно из печени, но выход витамина был очень не большой. В настоящее время получают витамин исключительно с помощью микробиологического синтеза.
Роль витамина В12 для организма заключается во множестве функций, включающих участие витамина в синтезе некоторых незаменимых аминокислот, нуклеиновых кислот, миелина (вещество, образующее нервную оболочку), холина, метионина, а также кобаламин стимулирует функцию костного мозга (который отвечает за гемопоэз), способствует образованию гема в эритроцитах. Витамин B12 может участвовать в поддержании сульфгидрильных (SH) групп в восстановленной форме, необходимой для многих SH-активируемых ферментных систем. Благодаря этим реакциям витамин B12 связан с жировым и углеводным обменом и синтезом белка. Дефицит витамина B12 приводит к некоторым видам анемии (например, мегабластной), поражениям пищеварительного тракта и неврологическим патологиям (которые начинаются с неспособности продуцировать миелин и сопровождаются постепенной дегенерацией аксона и нервной головки). Также д ефицит витамина B12 потенциально может привести к серьезным и необратимым повреждениям, особенно мозга и нервной системы. При даже небольшом дефиците В12 , могут наблюдаться такие симптомы, как усталость, вялость, депрессия, плохая память, одышка, головные боли и бледность кожи, в частности, особенно у пожилых людей (старше 60 лет). Дефицит витамина B12 также может вызывать симптомы мании и психоза.
Витамин в12 применяется в медицине и ветеринарии при гипо- и авитаминозах витамина. Существует огромное множество форм витамина в виде таблеток, капсул, пероральных жидкостей, спреев, порошков, в качестве БАДов, в составе мультивитаминных комплексов, в форме растворов для инфузий, даже в составе зубных паст и продуктах питания с целью обогащения пищи витамином. Назначают витамин в12 при различных анемиях, рассеянном склерозе, при недостаточности витаминов группы В, болезнях тройничного нерва и двигательного нейрона, параличе и парезе, при печеночной недостаточности, невралгии и многих других. Часто прием добавок с витамином В12 показан для приверженцев вегетерианского и веганского образа жизни с целью профилактики гиповитаминоза В12 или для устранения авитаминоза В12 и их последствий для организма ,по причине недостаточного потребления продуктов содержащих В12 или неупотребления их вовсе.
Получение витамина в12 осуществляют путем микробиологического синтеза из таких организмов, как актиномиценты, водоросли одноклеточные, а также фото- и метано синтезирующие бактерии. Например, источником В12 служат пропионовокислые бактерии, которых культивируют на средах с глюкозой, неорганическими солями, хлоридом кобальта, казеиновым гидролизатом и витаминами. Затем в среду добавляют 5,6-диметилбензимидазол( предшественник витамина), наблюдается активный рост в течение 5-6 суток и синтез витамина с выходом около 5,6-8,7 мг/л. Для более успешного синтеза и высокого выхода витамина активно также используют кукурузный субстрат и мутант пропионовокислых бактерий, выход витамина может составлять в таком случае до 30 мг/л витамина В12.
Действие на организм:
При пероральном попадании в организм В12 связывается с белком слюны — R-протеином, который защищает его в желудке от действия соляной кислоты. При поступлении в желудок, витамин, освободившись от R-протеина, соединяется с гликопротеидом – внутренним фактором Касла (Кастла) (который в свою очередь, вырабатывается париетальными клетками фундальных желез, расположенных в области дна тела и интрамедиальной части желудка) – проводящего его через агрессивную среду желудочного сока, защищая его от пищеварительных ферментов, а также от микрофлоры кишечника. В соединении с гликопротеидом В12 становится способен проникнуть через эпителиальные клетки подвздошной кишки и далее с помощью транспортных белков крови (альфа- и бетаглобулинов) в виде гидроксикобаламина разносится по организму и главным образом попадает в печень.
Сам по себе кобаламин не активен, для включения себя в два основных процесса — окисления остатка жирных кислот и трансаминирования аминокислоты гомоцистеина с последующим образованием метионина — принимает две коферментные формы: дезоксиаденозин-кобаламин и метилкобаламин соответсвенно.
Дезоксиаденозин-кобаламин участвует в реакции изомеризации – переноса радикальной группы на место водорода, а водорода на свободную связь углерода. В реакциях окисления незаменимых аминокислот (валин, изолейцин, цистеин и т.д.), это приводит к образованию большого количества энергии в виде сукценил-SKoA, используемого в цикле трикарбоновых кислот.
Метилкобаламин помогает образованию метионина из гистидина. Метионин является предшественником таких незаменимых веществ, как – адреналин, креатин, карнитина и др. Кроме того, реакция образования метионина способствует удержанию фолиевой кислоты (Витамин В9) внутри клетки.
Гиповитаминозы проявляются чаще всего не в следствии неправильного питания, а из-за нарушения в одном из звеньев проникновения кобаламина в организм, будь то дефицит внутреннего фактора Касла, поражение эпителиальных клеток нисходящей части подвздошной кишки и прочие нарушения мешающие нормальному транспорту витамина. Как правило, дефицит можно восполнить добавлением в рацион витамина В12 или применением инъекционных форм цианокобаламина (Естественно, это не будет являться лечением основного заболевания в большинстве случаев).
Цианокобаламин вводят интраназально, перорально и парентерально, тогда как гидроксокобаламин вводят только парентерально. Хранится витамин в основном в печени, но в костном мозге также содержится значительное количество поглощенного витамина В12. Этот витамин проникает через плаценту и распространяется в грудное молоко. Энтерогепатическая рециркуляция сохраняет системные запасы. Период полувыведения составляет около 6 суток (а в печени в среднем 400 дней). Ликвидация происходит главным образом через желчь. Однако избыток цианокобаламина из организма экскретируется и в неизмененном виде с мочой.
Из культуральной жидкости выделяют витамин, с помощью экстракции применяя органические растворители, ионообменной хроматографией. Если необходим витамин В12 для животноводческих целей, то продуцентами могут служить метанобразующие бактерии, а для медицинского использования витамин В12 получают обычно из бактерий Propionibacterium shermanii.
LD50 при внутривенном введении — мышь — 2 г / кг
Источник
Биологическая роль комплексных соединений
Комплексные соединения, рассмотренные нами выше, содержали лиганды, в основном, неорганической природы. Однако, в биологи-ческих системах огромную роль играют комплексные соединения, в которых в качестве лигандов выступают сложные органические молекулы, обладающие полидентатными свойствами (т. е., способны образовывать с комплексообразователем несколько связей).
Металлопротеины
К металлопротеинам относят биополимеры, которые, помимо белка, содержат простетическую группу (компонент небелкового характера), включающую ионы металлов.
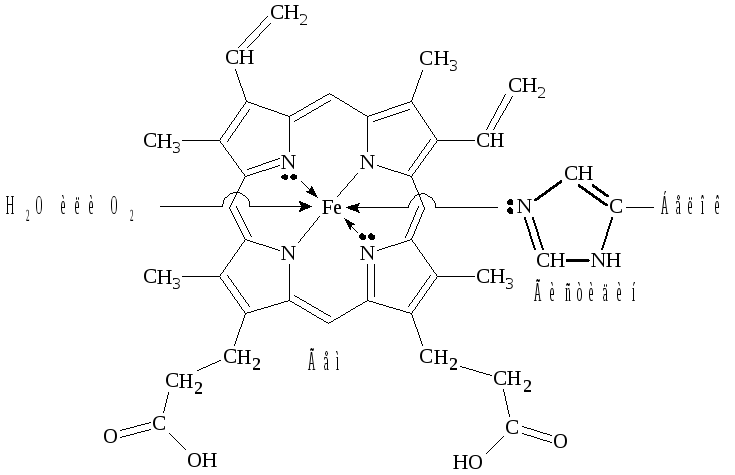
Отдельную группу металлопротеинов составляют гемопро-теины, содержащие в качестве простетической группы соединения железа. Одним из важнейших гемопротеинов является гемоглобин. Он состоит из белка (глобина) и комплекса железа с порфирином (гема). В геме ион Fe 2+ (комплексообразователь), связан с двумя атомами азота, принадлежащими порфириновому кольцу, ковалентной связью, а еще с двумя координационной. Координа-ционное число Fe 2+ равно шести: в порфириновом комплексе пятое координационное место занимает гистидиновая группа белка, образуя координационую связь атома азота с Fe 2+ . В отсутствие кислорода шестым лигандом является вода. В случае, когда вода замещается на кислород, образуется оксигемоглобин. Кроме воды и кислорода ион Fe 2+ может связывать и некоторые другие лиганды, например, СО, CN и оксиды азота. Так, с молекулами угарного газа гемоглобин образует карбоксигемоглобин, а с оксидами азота метгемоглобин, содержащий ионы Fe 3+ . Накопление этих видов гемоглобина в крови приводит к снижению снабжения тканей кровью.
Схема образования связей в гемоглобине
Гем в виде гем-порфирина является простетической группой производных гемоглобина: миоглобина, каталазы, пероксидазы и цитохромов.
Отличительной особенностью гемоглобина (миоглобина) являет-ся постоянство степени окисления железа Fe 2+ . Равновесие:
О2 + гемоглобин ⇄ оксигемоглобин
в легких смещено вправо, а в клетках – влево.
Таким образом, гемоглобин (миоглобин) является переносчиком молекул (Н2О, О2).
Транспортные функции выполняют и цитохромы, в которых связь между гемом и полипептидной цепью осуществляется при помощи остатков цистеина белковой цепи.
Однако, в отличие от гемоглобина и миоглобина, механизм их действия основан на изменении степени окисления железа:
Fe 2+ 
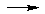
Fe 3+ + 
Передавая электроны от цитохрома b к цитохромооксидазе, ионы железа участвуют в процессе окислительного фосфорилирования.
С кислородом и СО цитохромы не взаимодействуют.
Витамины
Единственным витамином, содержащим в своей структуре металл, является витамин В12 (кобаламин).
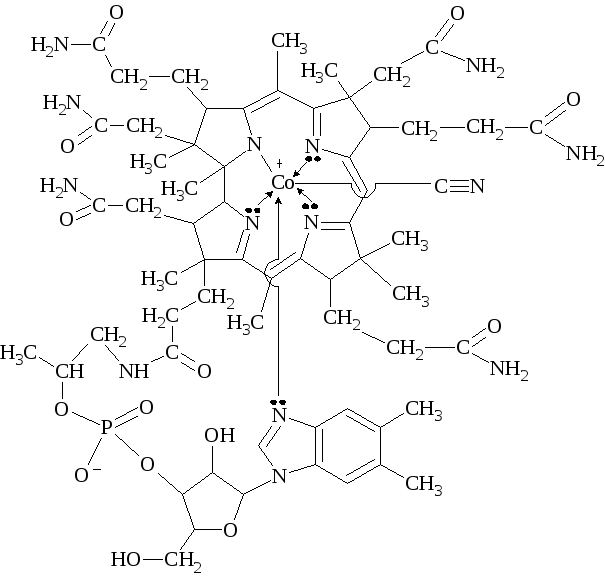
В его состав входит ион Со 3+ , который находится в центре плос-кой корриновой системы (подобна порфириновой) и связан с атомами азота восстановленных пиррольных колец. Перпендикулярно плос-кости корриновой системы расположен нуклеотидный лиганд, состо-ящий из 5,6-диметилбензимидазола и рибозы с остатком фосфорной кислоты. Наконец, шестым лигандом является цианид-ион.
Витамин В12 содержится в ферментных системах в виде В12-ко-ферментов или кобамидных коферментов метилкобаламина, содер-жащего дополнительную метильную группу, и дезоксиаденозин-кобаламина, содержащего 5-дезоксиаденозинкобаламин.
Так, метил-кобаламин выполняет функции переносчика метильной группы в реакции синтеза метионина. Кроме того, витамин В12 необходим для образования эритроцитов.
Недостаток витамина12 приводит к нарушениям деятельности нервной системы и вызывает резкое снижение кислотности желудоч-ного сока.
Схема образования связей в витамине B12 (кобаламине)
Источник
Образование комплексных соединений витамин в12
Роль комплексных соединений в жизнедеятельности живых организмов огромна. Организм представляет систему, состоящую из множества комплексообразователей и лигандов, с определенным соотношением между ними. Нарушение баланса компонентов (металло-лигандного гомеостаза) приводит к развитию патологических состояний. Поэтому изучение процессов взаимодействия «металл–лиганд» является ключом к поиску новых лекарственных средств. В процессах обмена веществ фундаментальную роль играет биокатализ, в котором принимают участие металлоферменты, представляющие собой биокомплексы Fe, Co, Mn, Zn, Мо, Mg, Сu, Сr. Ферменты – уникальные катализаторы, обладающие непревзойденной эффективностью действия и высокой селективностью. Биокомплексы различаются по устойчивости. Одни из них настолько прочны, что постоянно находятся в организме и выполняют определенную функцию. Примерами таких соединений является хлорофилл, полифенилоксидаза, витамин В12, гемоглобин и некоторые металлоферменты (специфические ферменты). Роль металлов таких комплексов высокоспецифична: замена его даже на близкий по свойствам элемент приводит к значительной или полной утрате физиологической активности. Ферменты, синтезируемые на период выполнения определенной функции, в которой ион металла выполняет роль активатора и может быть заменен ионом другого металла без потери физиологической активности, относят к неспецифичным ферментам. В настоящее время известно и изучено около 700 различных ферментов, 25 % которых составляют металлоферменты.
Важнейшим классом бионеорганических комплексов металлов являются транспортные комплексы, в которых один или несколько атомов металла связаны с атомами азота, кислорода или серы белковых молекул, выступающие в роли полидентатных лигандов. Одним из основных переносчиков ионов металлов в человеческом организме является низкомолекулярный белок металлотионеин (Мr=6500), содержащий большое число цистеиновых фрагментов. Один моль металлотионеина способен перенести 7-12 моль таких жизненно необходимых элементов, как Zn, Cu и Se. При отравлениях тяжелыми металлами (Сd, Hg, Pb, Ag, As) данный белок выполняет защитную функцию, связывая их в прочные и относительно малотоксичные комплексы. Железосодержащий белок трансферрин выполняет преимущественно транспортные функции. Несмотря на сравнительно низкое содержание железа (2 моль ионов Fe3+ на одну молекулу белка), трансферриновые комплексы обеспечивают высокую скорость тканевого обмена данного элемента и являются важными переносчиками железа.
Изучение бионеорганических комплексов дает важную информацию об особенностях их метаболизма и позволяет разрабатывать эффективные способы коррекции заболеваний, связанных с недостатком (или, наоборот, с избытком) тех или иных элементов в человеческом организме.
Применение комплексных соединений в медицине и фармации связано также с их использованием в методах качественного и количественного анализа – в комплексонометрии. Широкое распространение получила комплексонометрия в медико-биологических исследованиях. Этот метод необходим для определения в живых организмах кальция, магния и многих микроэлементов. Комплексонометрия применяется в анализе лекарственного сырья, питьевых, минеральных и сточных вод. В биологии и медицине комплексоны используются не только в аналитических целях, но и в качестве стабилизаторов при хранении крови, так как комплексоны связывают ионы металлов, катализирующих реакции окисления. Комплексоны применяются также для выведения из организма ионов токсичных металлов (Рb2+, Cd2+ , Hg2+ и др.), радиоактивных изотопов и продуктов их распада.
Источник