Ферменты и неорганические катализаторы
ПОНЯТИЕ О ФЕРМЕНТАХ.
Ферменты — это биологические катализаторы в основном белковой природы.
Роль ферментов в организме огромна. В каждой клетке организма находится до 10000 молекул ферментов, которые катализируют более 2000 различных химических реакций. Ферменты начинают своё каталитическое действие в ЖКТ, продолжают его в тканях, на этапе выведения и образования конечных продуктов. Энзимология (ферменты — энзимы) — раздел науки, изучающий ферменты.
ОБЩИЕ ЧЕРТЫ ФЕРМЕНТОВ И НЕБИОЛОГИЧЕСКИХ КАТАЛИЗАТОРОВ.
1. Повышают скорость реакции.
2. В реакциях они не расходуются.
3. Для обратимых процессов и прямая, и обратная реакция катализируется одним и тем же ферментом.
ОТЛИЧИТЕЛЬНЫЕ ПРИЗНАКИ ФЕРМЕНТОВ.
1 .Ферменты обладают более высокой эффективностью действия (повышают скорость реакции в большее число раз, чем неорганические катализаторы).
2.Ферменты чувствительны к температуре (термолабильны)
3.Ферменты чувствительны к значениям рН среды.
4.Ферменты, в отличие от неорганических катализаторов, обладают высокой специфичностью действия.
5.Ферменты — это катализаторы с регулируемой активностью.
| Предыдущий раздел | Раздел верхнего уровня | Следующий раздел |
Строение ферментов
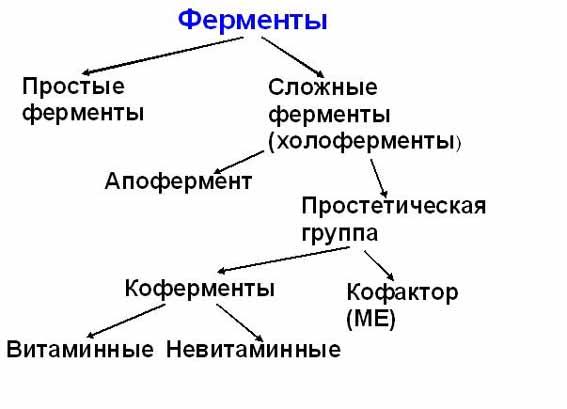
Ферменты, являясь белками, повторяют все особенности структуры и состава белков (состоят из аминокислот, имеют 4 уровня структурной организации), физико-химические свойства белков. Ферменты, как и все функциональные белки, могут быть простыми и сложными.
Простые ферменты представлены только белковой частью (состоят из аминокислот) — пепсин, трипсин, фосфатазы.
Сложные ферменты представлены:
1 .Белковой частью (состоит из аминокислот) — апофермент;
Небелковая часть может быть представлена:
· ионами металлов (К, Na, Ca, Mg, Mn);
· коферментами — низкомолекулярные органические вещества.
Для многих ферментов его апофермент вместе с небелковой частью образуют каталитически активную молекулу, которая называется холоферментом.
В роли биокатализаторов могут выступать и небелковые соединения. Рибозимы — биокатализаторы, которые по химической природе являются РНК.
Рибозимы катализируют разрыв фосфодиэфирных связей нуклеиновых кислот.
В пространственной структуре фермента можно выделить отдельные участки, которые выполняют те или иные функции (активный центр, контактный участок, каталитический участок, аллостерический центр).
Активный центр — это участок в молекуле фермента, где происходит связывание и превращение субстрата. Активный центр обычно располагается в гидрофобном углублении (недоступном для молекул воды), изолируя субстрат от воды. В образовании активного центра, участвуют боковые группы АК (12-20 АК), причём эти АК могут находиться на разных участках полипептидной цепи, но при формировании пространственной конфигурации фермента они укладываются т.о., что располагаются в области активного центра. В образовании активного центра принимают участие следующие группы боковых цепей АК:
– имидазольное кольцо (гис);
– гуанидиновая группа (арг);
– фенольное кольцо (тир).
Остальные АК поддерживают пространственную конфигурацию активного центра фермента
и обеспечивают его реакционную способность.
Контактный (субстрат-связывающий ) участок — это место в активном центре фермента, где происходит связывание субстрата с его активным центром. Контактный участок обеспечивает специфическое сродство субстрата к ферменту.
Каталитический участок — место, где проходит сама каталитическая реакция.
Аллостерический центр — участок в молекуле фермента, пространственно удаленный от активного центра. К аллостерическому центру могут присоединяться различные вещества, которые отличаются по структуре от молекул субстрата. Эти вещества называются аллостерические эффекторы. Они могут влиять на конформацию активного центра фермента, изменяя её, т.е. могут или повышать скорость реакции, или тормозить её.
рис. Активный центр фермента
| Предыдущий раздел | Раздел верхнего уровня | Следующий раздел |
Коферменты
Коферменты – небелковая часть сложных ферментов. Их делят на две группы:
1.Тиаминовые коферменты содержат в своём составе витамин В1 (тиамин).
ТДФ связан с ферментами — декарбоксилазами альфа – кетокислот (входит в состав пируватдегидрогеназного и альфа-кетоглутаратдегидрогеназного комплексов);
Является коферментом трансктолаз.
2.Флавиновые коферменты содержат в своём составе витамин В 2.
ФМН и ФАД связаны с ферментами дегидрогеназами. Участвуют в реакциях дегидрирования.
3. Пантотеновые коферменты содержат в своём составе витамин ВЗ (пантотеновая кислота).
Представитель – кофермент А.
1. Переносе ацильных радикалов;
2. Активации жирных кислот;
3. Синтезе холестерола и кетоновых тел;
4. Обезвреживании ксенобиотиков.
4. Никотинамидные коферменты содержат в своём составе витамин РР (никотинамид).
Кофермент могут быть в окисленной и восстановленной форме.
НАД и НАДФ связаны с ферментами дегидрогеназами, которые ускоряют окислительно-восстановительные реакции.
5. Пиридоксиновые коферменты содержат в своём составе витамин В6.
Кофермент – пиридоксальфосфат (ПФ).
Участвует в реакциях превращения АК:
1.Реакции переаминирования (трансаминирование). Связан с ферментами аминотрансферазами.
2.Реакции декарбоксилирования аминокислот.
Не содержат в своём составе витаминов, но участвуют в каталитических превращениях.
1. Нуклеотиды: АТФ, ЦТФ (участвуют в синтезе фосфолипидов); УДФ, УТФ, ГТФ (участвуют в синтезе гликогена).
2. Производные порфирина: гем, цитохромы, каталаза.
Глутатион — трипептид, содержащий ГЛУ-ЦИС-ГЛИ. Он связан с ферментами оксидоредуктазами. Участвует в окислительно-восстановительных реакциях.
| Предыдущий раздел | Раздел верхнего уровня | Следующий раздел |
Свойства ферментов
1 .Высокая каталитическая активность.
2.Ферменты, являясь белками, проявляют термолабильные свойства — чувствительность к изменению температуры.
При повышении температуры на каждые 10 градусов Цельсия, скорость ферментативных реакций повышает в 1,5 — 2 раза (правило Вант — Гоффа). Это правило применимо для ферментов в очень узком интервале температуры, т.к. уже при 50-60 градусах наблюдается денатурация, а при 100 градусов Цельсия — полная денатурация с потерей активности. При 1-3 градусов Цельсия Активность фермента также понижается, но при понижении температуры структура его сохраняется, поэтому при последующем повышении температуры активность восстанавливается. Это свойство используется в клинической практике при проведении оперативных вмешательств. Температура, при которой фермент проявляет максимальную активность, называется оптимальной.
3.Ферменты чувствительны к изменениям рН среды. Для большинства ферментов оптимальные значения РН лежат в нейтральной среде (для каталазы рН = 7).
Есть ферменты, для которых оптимальные значения рН лежат в кислой среде (пепсин рН = 1 ,5-2,5). Некоторые ферменты проявляют активность в щелочной среде (аргиназа рН = 10 — 11). Изменения рН приводит к изменению степени ионизации кислых и основных групп в активном центре фермента, т.к. эти группы участвуют в связывании субстрата и его превращении. Изменение рН приводит к конформационной перестройке не только активного центра фермента, но и всей молекулы фермента. Это может сопровождаться нарушением третичной структуры фермента. При оптимальном значении рН функциональные группы активного центра находятся в наиболее реакционно-способном состоянии, и это обеспечивает образование фермент-субстратного комплекса.
Источник
Чем ферменты отличаются от неорганических катализаторов
в Наука и образование 03.01.2016 3,845 Просмотров
Неорганические катализаторы и ферменты (биокатализаторы), не расходуясь сами, ускоряют течение химических реакций и их энергетические возможности. В присутствии любых катализаторов энергия в химической системе сохраняет постоянство. В процессе катализа направление химической реакции остается неизменным.
Что такое ферменты и неорганические катализаторы
Ферменты являются биологическими катализаторами.
Их основа – белок. Активная часть ферментов содержит неорганическое вещество, к примеру, атомы металлов.
При этом каталитическая эффективность металлов, включенных в молекулу фермента, увеличивается в миллионы раз.
Примечательно то, что органический и неорганический фрагменты фермента не способны по отдельности проявлять свойства катализатора, тогда как в тандеме являются мощными катализаторами.
Неорганические катализаторы ускоряют всевозможные химические реакции.
Сравнение ферментов и неорганических катализаторов
В чем разница между ферментами и неорганическими катализаторами?
Неорганические катализаторы по своей природе – неорганические вещества, а ферменты – белки. В составе неорганических катализаторов нет белка.
Ферменты по сравнению с неорганическими катализаторами обладают специфичностью действия к субстрату и наиболее высокой эффективностью.
Благодаря ферментам реакция протекает быстрее в миллионы раз.
Например, перекись водорода без присутствия катализаторов разлагается довольно медленно. При наличии неорганического катализатора (обычно солей железа) реакция несколько убыстряется. А при добавлении фермента каталазы пероксид разлагается с невообразимой скоростью.
Ферменты способны работать в ограниченном диапазоне температур (как правило, 370 С). Скорость действия неорганических катализаторов с каждым увеличением температуры на 10 градусов повышается в 2-4 раза. Ферменты подвергаются регуляции (существуют ингибиторы и активаторы ферментов).
Неорганическим катализаторам свойственна нерегулируемая работа.
Для ферментов характерна конформационная лабильность (их структура подвергается незначительным изменениям, образующимся в процессе разрыва старых связей и образования новых связей, прочность которых слабее). Реакции с участием ферментов протекают лишь в физиологических условиях.
Ферменты способны работать внутри организма, его тканей и клеток, где создаются необходимый температурный режим, давление и рН.
Источник
Витамины – катализаторы метаболизма
Витамины – катализаторы метаболизма
В регуляции процессов метаболизма, а также для нормальной жизнедеятельности организма важно, чтобы в состав рациона питания входили витамины. Они играют роль биологических катализаторов, которые направляют и ускоряют процессы метаболизма. В организме витамины либо не синтезируются, либо синтезируются в недостаточном количестве. Они поступают или с продуктами питания, в которых содержатся, или в виде синтетических препаратов. Естественные носители витаминов наиболее полезны для организма.
Количество витаминов, поступающих в организм, должно соответствовать его потребностям. Недостаточное или избыточное поступление витаминов может вызвать серьезные заболевания, которые называются авитаминозами, гиповитаминозами или гиперавитаминозами.
Витамины подразделяются на 2 группы: водорастворимые и жирорастворимые. К жирорастворимым витаминам относятся витамины A, D, Е и К.
Витамин А оказывает влияние на рост организма, на его устойчивость по отношению к инфекциям. Он необходим для поддержания нормального зрения, состояния кожи и слизистых оболочек. В большом количестве витамин А содержится в рыбьем жире, сливках, сливочном масле, яичном желтке, печени. Также некоторые растительные продукты: морковь, помидор, шпинат, зеленый горошек, абрикос, апельсин – содержат каротин, или провитамин А, который в организме превращается в витамин А.
Витамин D способствует образованию костной ткани и стимулирует развитие организма. При недостатке его в пище нарушается нормальное усвоение организмом кальция и фосфора. Наибольшее количество витамина D содержится в рыбьем жире, яичном желтке, печени, икре.
Витамин Е (токоферол) влияет на функцию эндокринных желез, на метаболизм белков, углеводов, обеспечивает внутриклеточный обмен. Витамин Е благоприятно влияет на течение беременности и развитие плода. Больше всего этого витамина содержится в моркови, зернах кукурузы, капусте, зеленом горошке, яйцах, в сливочном и оливковом масле, мясных и рыбных продуктах.
Витамин К участвует в тканевом дыхании, способствует сохранению нормальной свертываемости крови. Этот витамин синтезируется в организме бактериями кишечника. Недостаток его может возникнуть при заболеваниях органов пищеварения или при приеме различных антибактериальных препаратов. Витамин К содержится в помидорах, крапиве, шпинате, капусте.
К водорастворимым витаминам относятся витамин С и витамины группы В.
Витамин С (аскорбиновая кислота) активно участвует в окислительно-восстановительных процессах, влияет на белковый и углеводный обмен, повышает сопротивляемость организма к различным инфекциям. Этот витамин содержится во многих овощах и фруктах. Наиболее богаты им шиповник, черная смородина, черноплодная рябина, облепиха, крыжовник, лиственные овощи, картофель, цитрусовые.
Витамины группы В включают из 15 биологически активных, растворимых в воде, самостоятельных витаминов, принимающих участие в многообразных процессах обмена веществ. Витамины этой группы необходимы для нормального течения углеводного, жирового и водного обменов. Они играют важную роль в окислительно-восстановительных и других процессах. Содержатся в гречневой и овсяной крупе, ржаном хлебе, пивных и пекарских дрожжах, молоке, зеленых листовых овощах, мясе, печени, яичном желтке.
Между действием различных витаминов существует тесная взаимосвязь: недостаток в пище хотя бы одного из них влечет нарушение обмена. Надлежащее воздействие на организм витамины оказывают только при правильном питании. Их недостаток может быть обусловлен как малым содержанием в рационе, так и недостаточным поступлением других пищевых веществ. Например, недостаточное потребление белка приводит к тому, что витамины выводятся из организма. А витамины A, D, Е, К усваиваются организмом лишь в том случае, если в пище содержится достаточное количество жира. При недостатке в пище ненасыщенных жирных кислот повышается потребность в витаминах В 1 и В 6. При избыточном содержании в пище углеводов возрастает потребность в витамине B 1.
Данный текст является ознакомительным фрагментом.
Продолжение на ЛитРес
Читайте также
Наследственные заболевания с нарушением метаболизма нутриентов
Наследственные заболевания с нарушением метаболизма нутриентов При наследственных заболеваниях, характеризующихся нарушением метаболизма того или иного вещества, принцип диетотерапии одинаков – исключение из рациона продуктов, богатых данным веществом.Болезнь
Определение уровня метаболизма
Определение уровня метаболизма Почти половина всей энергии, получаемой в результате катаболизма, теряется в виде тепла в процессе образования молекул АТФ. Мышечное сокращение – процесс еще менее эффективный. Около 80% энергии, используемой при мышечном сокращении,
Патология «Я» и ослабление информационного метаболизма
Патология «Я» и ослабление информационного метаболизма Нарушения границы оказываются, как уже отмечалось, тесно связанными с нарушениями «Я». Следует начать с нарушений «Я» как основной точки отсчета и основного интегрирующего центра, так как они наиболее доступны
Токсические продукты нормального метаболизма
Токсические продукты нормального метаболизма Среди основных продуктов питания лишь белки и сопутствующие им нуклеиновые кислоты, образуют в процессах метаболизма и усвоения токсические соединения, аммиак и пурины, требующие ферментативной детоксификации и удаления
Замедление метаболизма
Замедление метаболизма Метаболизм (обмен веществ) – процесс, который происходит в организме, а именно – превращение питательных веществ, поступающих с пищей, в энергию. Энергия необходима для жизни, и не только когда вы идете, бежите трусцой или работаете в саду. Она
ДЕТИ С ПРОБЛЕМАМИ МЕТАБОЛИЗМА
ДЕТИ С ПРОБЛЕМАМИ МЕТАБОЛИЗМА Дети с кистозным фиброзом и фенолкетонурией могут продолжать грудное вскармливание. Часто грудное вскармливание облегчает лечение этих серьезных заболеваний и для матери, и для бригады
Увеличение скорости метаболизма
Увеличение скорости метаболизма Вы знаете, что для того чтобы сбавить вес, нужно иметь хороший обмен веществ. Не боритесь с низким уровнем метаболизма. Одного желания улучшить его мало, надо правильно вести себя. Обратите внимание на эффективные способы увеличения
Базовая скорость метаболизма
Базовая скорость метаболизма Существует такое понятие, как базовая скорость метаболизма — то есть скорость, с которой и происходят все эти процессы в организме человека в состоянии покоя.Базовая скорость метаболизма зависит от потребностей организма. То есть
Основа здоровья – регуляция процессов метаболизма
Основа здоровья – регуляция процессов метаболизма От обмена веществ зависит ваше здоровье! Регуляция метаболизма является основой физиологических процессов в организме. Она представляет собой комплекс взаимосвязанных процессов: синтеза, распада и изменения
Скорость метаболизма – от чего она зависит
Скорость метаболизма – от чего она зависит Скорость обмена веществ определяется количеством калорий, расходуемых в данный момент, независимо от того, смотрит ли человек телевизор или выполняет физические упражнения. При этом процессы метаболизма, то есть скорость
Особенности метаболизма при различных видах питания
Особенности метаболизма при различных видах питания В наши дни под напором негативных факторов (шум, раздражение, частые стрессы, пища с консервантами и другими химическими добавками, вредные вещества окружающей среды, алкоголь, кофеин и др.) человек становится все более
Особенности белкового метаболизма при вегетарианском питании
Особенности белкового метаболизма при вегетарианском питании Выше упоминалось о том, что белок – один из трех основных пищевых компонентов (наряду с жирами и углеводами). Во всех живых организмах он играет важную роль, так как является основной частью цитоплазмы –
Особенности метаболизма в разных возрастах
Особенности метаболизма в разных возрастах На метаболические процессы влияют многие факторы и условия: пол, конституция тела, гены, рост, состояние нервной системы, психики, гормоны. Во многом метаболические процессы зависят от возраста человека. У совершеннолетних
Особенности регуляции метаболизма в детском и молодом возрасте
Особенности регуляции метаболизма в детском и молодом возрасте Обмен веществ у детей гораздо более интенсивен, чем у взрослых. Основными его особенностями являются:1) преобладание процессов ассимиляции (усвоения) над процессами диссимиляции (расщепления) пищи (то есть
Роль метаболизма в омоложении
Роль метаболизма в омоложении Человек всегда стремился оставаться жить долго и оставаться молодым, но порой он забывает, что тайна продления жизни прежде всего заключается в том, чтобы не сокращать ее себе самому. Во все времена для возвращения молодости, отдаления
ГЛАВА 4 Правила ускорения метаболизма
ГЛАВА 4 Правила ускорения метаболизма Теперь, когда мы знаем, как и почему работает диета, настало время, чтобы она начала работать на вас. В этой главе я собираюсь установить правила. Я собираюсь рассказать вам, что нужно есть в следующие 28 дней и что есть не рекомендуется,
Источник