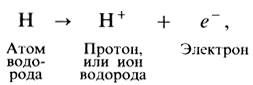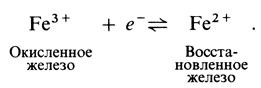35. витамины II С-U
Витамин С – аскорбиновая кислота – пожалуй, самый известный из витаминов. Это связано и с тем, что она требуется организму человека постоянно и в больших (по витаминным меркам) дозах – примерно 100 мг\сутки. Это водорастворимый витамин, синтезируется всеми зелеными растениями, пресмыкающимися и земноводными.
Аскорбиновая кислота участвует в разнообразных биохимических процессах благодаря её окислительно-восстановительным свойствам. Окисление происходит в две стадии. На первой стадии аскорбиновая кислота (восстановленная форма) превращается в дегидроаскорбиновую (окисленная форма), эта стадия обратима. На второй стадии более глубокого окисления происходит расщепление молекулы с образованием двух карбоновых кислот:
Окислительным расщеплением аскорбиновой кислоты объясняется её неустойчивость при хранении и при нагревании.
Аскорбиновая кислота участвует в гидроксилировании лизина и пролина при образовании коллагена, гидроксилировании ДОФамина при образовании адреналина, предотвращает окисление SH-групп белков и глютатиона, а также восстанавливает Fe 3+ до Fe 2+ в кишечнике, обеспечивая всасывание железа.
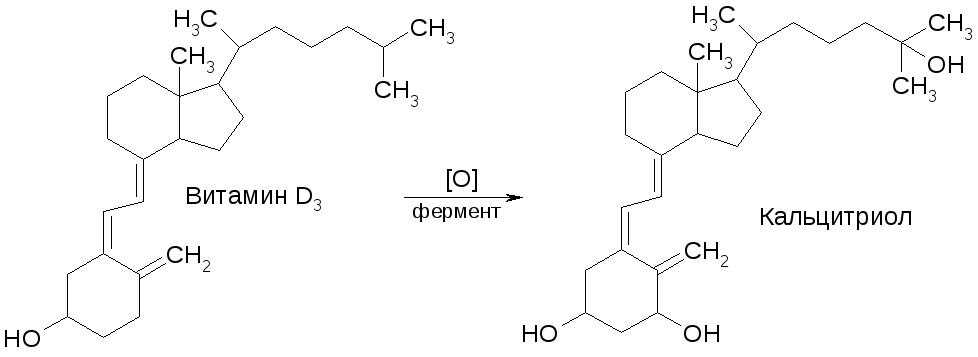
Под витамином D подразумевается группа очень близких по структуре жирорастворимых соединений (D1-D4), называемых также кальциферолами («переносчик кальция») и обладающих антирахитическим действием. Витамин D содержится в печени морских животных и рыб, а также может образовываться при УФ-облучении эргостерина (последний продуцируется дрожжами и грибами):
Функция витамина D в организме – обеспечение всасывания кальция в кишечнике. Эту функцию он выполняет в виде активной формы – кальцитриола, которая образуется при ферментативном гидроксилировании исходного витамина в печени и почках:
Кальцитриол за счет своих гидроксильных групп комплексно связывает ион Са +2 , окружая его липофильной оболочкой. Такой комплекс становится способным переходить через липидный слой биомембраны.
Витамином Е называется группа природных жирорастворимых соединений под общим названием токоферолы. Все они представляют собой производные бензопи-рана с гидроксильной группой в бензольном кольце и длинным углеводородным остатком в пирановом цикле. Различные токоферолы отличаются между собой разным количеством и положением метильных групп в бензольном кольце.
Токоферолы – это «ловушки радикалов». Будучи фенолами, они легко вступают в реакции радикального окисления, образуя хиноны:
Биологическая роль токоферолов заключается в том, что они как антиоксиданты защищают липидные компоненты клеток от окисления, и кроме того они обеспечивают репродуктивную функцию животных: недостаток витамина Е вызывает беспло-дие у самок крыс.
Природные источники витамина Е – различные растительные масла.
Витамином F называются природные полиненасыщенные жирные кислоты: линолевая, линоленовая и арахидоновая. Эти кислоты необходимы в организме для синтеза фосфолипидов и на их основе биологических мембран, но в организме они не синтезируются и должны поступать с пищей. Источник витамина F – растительные масла.
Витамин Н – биотин – широко распространен в природе: его много в печени и почках, зернах ржи, цветной капусте.
Биотин по химической структуре представляет собой бициклическую систему, состоящую из гидрированных циклов имидазола и тиофена. Он является коферментом в реакциях карбоксилирования карбоновых кислот. С помощью карбоксильной группы он ковалентно связывается с апоферментом амидной связью.
На следующей схеме представлена реакция карбоксилирования ацетил-КоА с участием биотина, в результате которой образуются производные малоновой кислоты:
Витаминами К – антигеморрагическими факторами – называются природные производные нафтохинона, содержащие в хиноидном кольце метильную группу и изопреноидный остаток. У животных и человека присутствуют менахиноны (витамин К2), синтезируемые микроорганизмами. Помимо природных соединений высокой К-витаминной активностью обладают более простые соединения – 2-метилбензохинон (менадион) и его водорастворимый аналог – викасол, применяющийся в медицинской практике.
Антигеморрагическое действие витамина К (способность повышать свертываемость крови) связано с тем, что он в качестве кофермента катализирует реакцию карбоксилирования остатков глутаминовой кислоты в составе белка протромбина – одного из факторов свертывания крови:
После этого протромбин связывает ионы Са 2+ , превращаясь в тромбин, последний вызывает коагуляцию фибриногена – происходит свертывание крови.
Витамином К богаты зеленые растения, кроме того он в достаточных количествах вырабатывается микрофлорой кишечника.
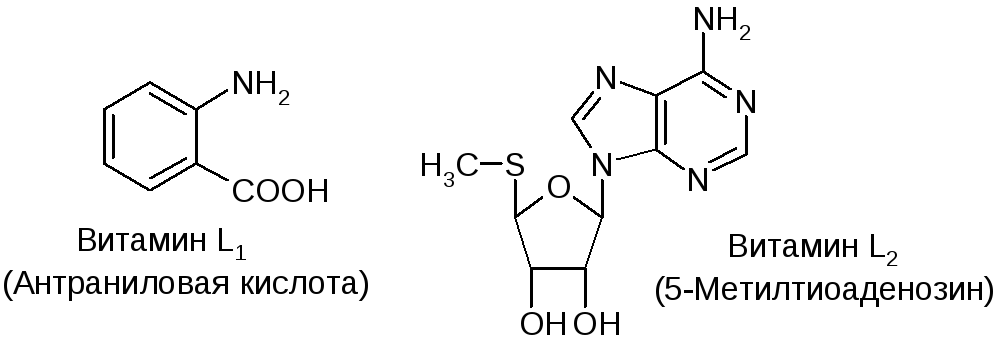
Витаминами L – факторами лактации – называются два вещества: антраниловая кислота (витамин L1) и 5-метилтиоаденозин (витамин L2):
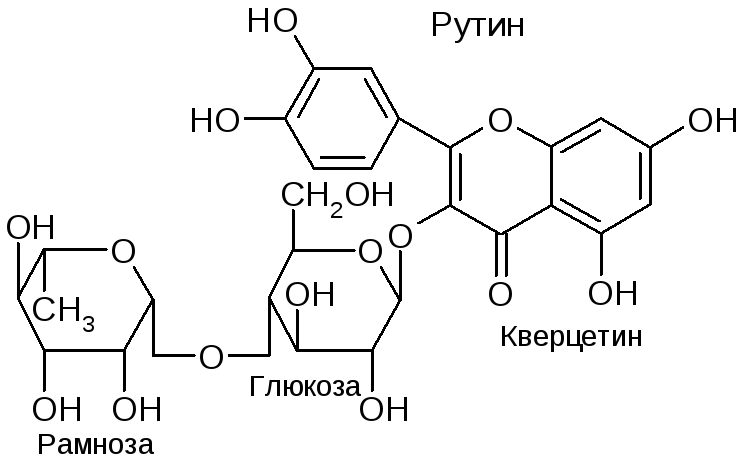
Витамином Р называется группа растительных веществ т.н. биофлавоноидов, содержащихся в чае, желтых цветах, апельсиновой корке, плодах аронии (черноплодной рябины). Это производные флавона, в основе которого лежит цикл бензопирана:
Один из главных биофлавоноидов – рутин – представляет собой гликозид кверцетина (пигмент желтых цветов):
Все биофлавоноиды – это природные антиоксиданты. Витамин Р – синэргист аскорбиновой кислоты, повышающий эффективность её действия.
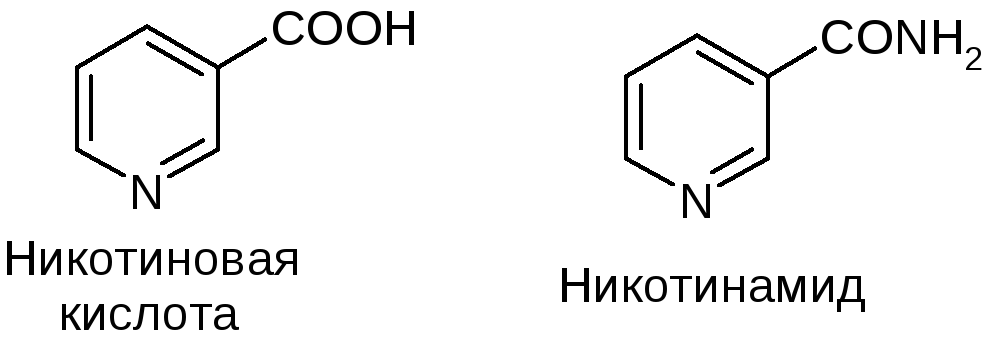
Витамин РР – ниацин, pellagra protective factor – это никотиновая кислота и её амид, обладающие одинаковым витаминным действием:
Их витаминное действие заключается в том, что они формируют активный центр пиридиновых коферментов НАД и НАДФ, выполняющий функции переноса водорода в реакциях биологического окисления:
Витамин РР синтезируется микрофлорой кишечника, но в недостаточных количествах. Много витамина РР содержится в дрожжах, сушеных грибах, некоторых крупах, а также в мясе и печени.
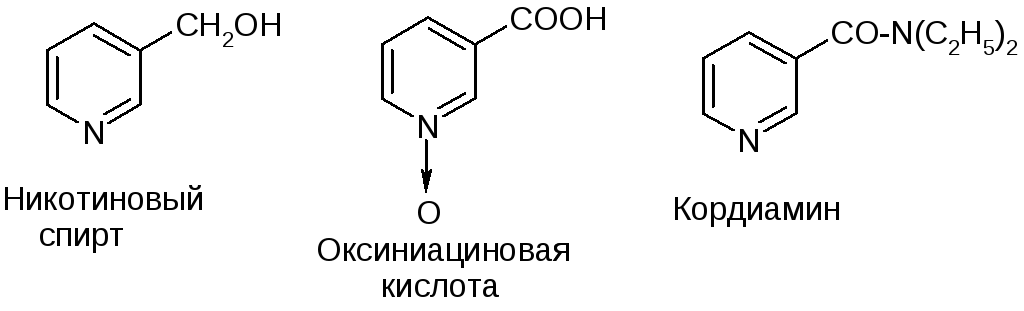
Некоторые синтетические производные никотиновой кислоты обладают невитаминной биологической активностью и применяются в медицине: никотиновый спирт – сосудорасширяющий препарат, кордиамин – аналептик, оксиниациновая кислота снижает содержание β-липопротеидов в крови и нормализует липидный обмен:
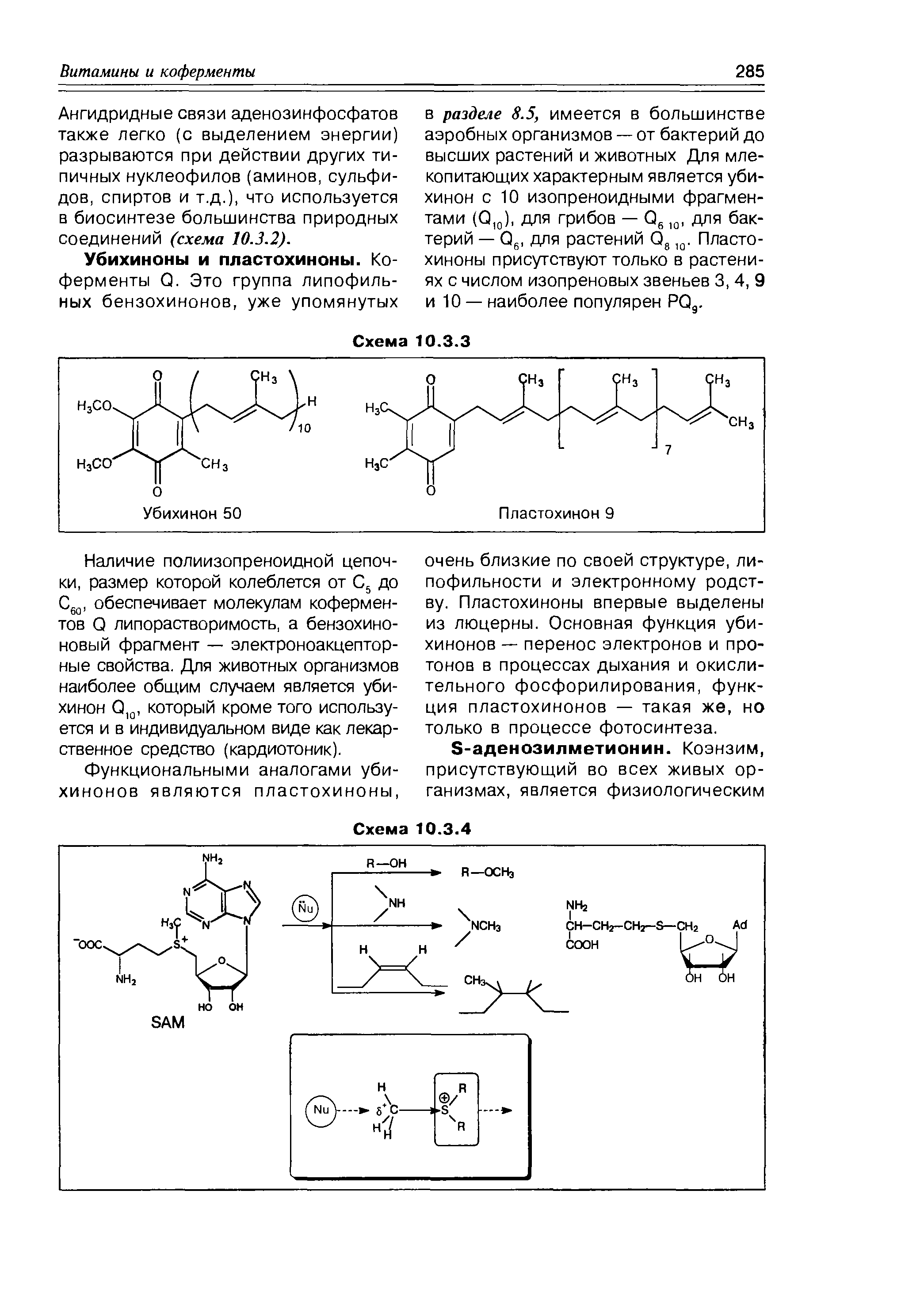
Убихинонами – коэнзимами Q – называется группа липофильных производных бензохинона, которые присутствуют во всех аэробных организмах – от бактерий до высших растений и животных. Убихиноны являются частью дыхательной цепи митохондрий, их функция – перенос электронов и протонов по схеме:
В нормальных условиях убихиноны синтезируются в организме человека в достаточных количествах. Но при белковой недостаточности у детей возникает анемия, которая снимается введением витамина Q.
S-Аденозилметионин и витамин U
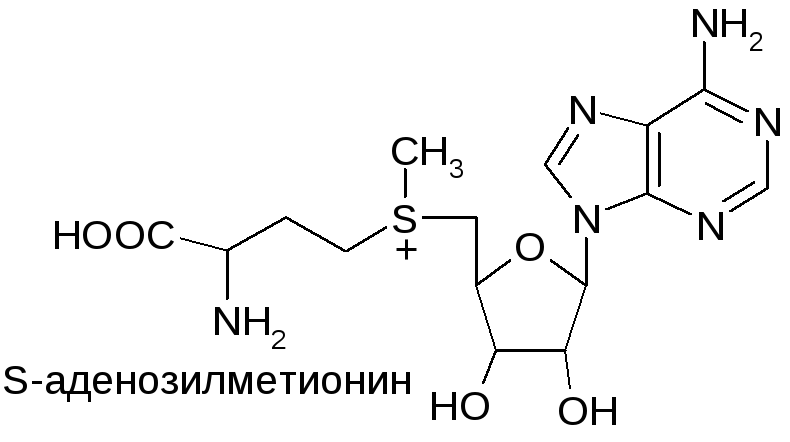
В организме образуются соединения, содержащие метилтиониевые группировки, которые являются донорами метильных групп в реакциях трансметилирования. Главный метаболит этого типа – S-аденозилметионин (SAM):
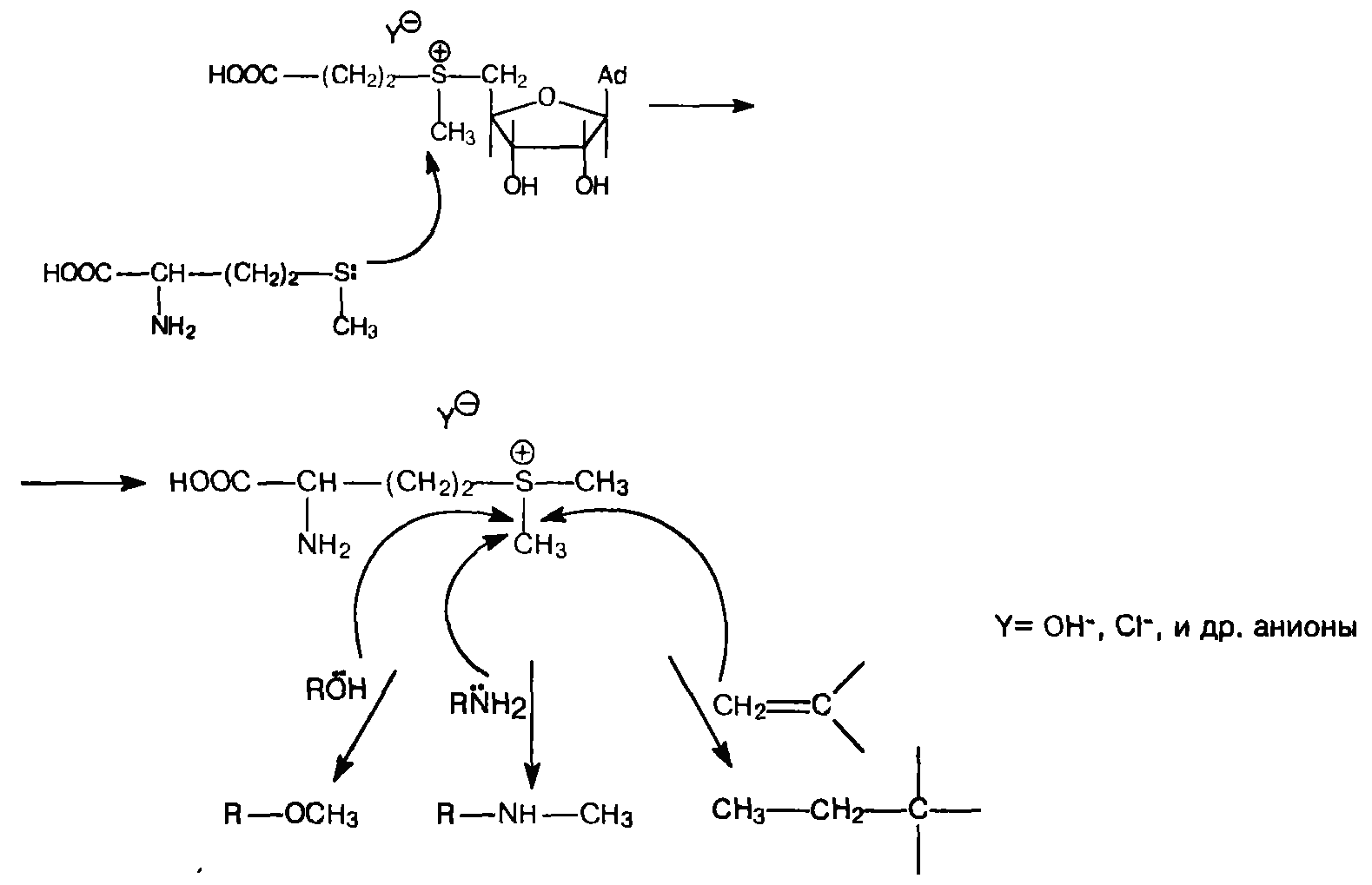
Подвижная СН3-группа тиониевого фрагмента, реагируя с нуклеофилами, переходит на другие атомы:
В реакции S-аденозилметионина с метионином метильная группа переходит на атом серы метионина и образуется метионинметилсульфоний, называемый витамином U:
Витамин U, как и S-аденозилметионин, является биологическим метилирующим агентом и по причине бóльшей устойчивости служит накопителем и резервом метильных групп в организме:
Витамин U содержится в капусте, петрушке, спарже, сельдерее, шпинате, томатах и молоке. Он обладает противоязвенным действием: снимает боли и способствует эпителизации стенки желудка у язвенных больных.
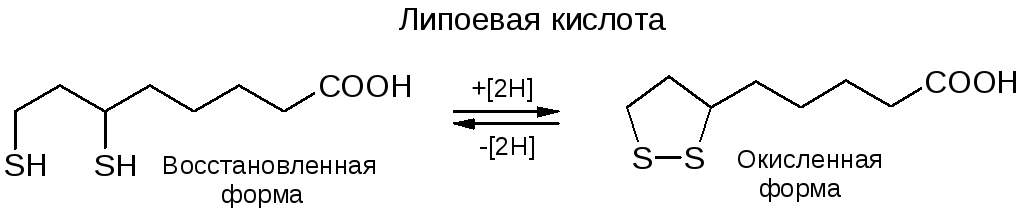
Липоевой кислотой называется 6,8-димеркаптооктановая кислота, которая при окислении обратимо образует внутренний дисульфид:
Липоевая кислота – это липофильное природное соединение, играющее роль кофермента, переносящего атомы водорода и ацильные группы в ПВКДГ и α-КГДГ ферментных комплексах. С помощью карбоксильной группы через остаток лизина липоевая кислота ковалентно связывается в апоферментом:
У животных и человека липоевая кислота синтезируется микрофлорой кишечника.
В медицине липоевая кислота применяется при заболеваниях печени, атеросклерозе и диабетическом полиневрите.
1. Н.А.Тюкавкина, Ю.И.Бауков – Биоорганическая химия – ДРОФА, М., 2007 г., с. 498-503.
1. В.В.Племенков – Введение в химию природных соединений – Учебное пособие для химических, биологических и медицинских специальностей ВУЗов, Казань, 2001, с. 267-290.
2. Ю.А.Овчинников – Биоорганическая химия – М., Просвещение, 1987 г.,
Источник
Накопителем атомов водорода является витамин
11.3.7. Переносчики водорода и электронов
НАД и НАДФ — два очень близких по своей структуре кофермента. Оба они представляют собой производные никотиновой кислоты (одного из витаминов группы В). Молекулы того и другого кофермента электроположительны (у них отсутствует один электрон) и могут играть роль переносчика как электронов, так и атомов водорода. Когда акцептируется пара атомов водорода, один из атомов диссоциирует на протон и электрон:
а второй присоединяется к НАД или НАДФ целиком.
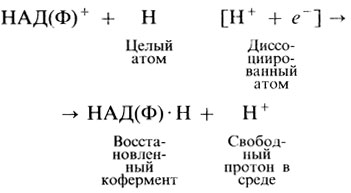
Суммарную реакцию можно записать так:
Свободный протон позднее, при отщеплении водорода, используется для обратного окисления кофермента.
Флавопротеины — это коферменты, в состав которых входит витамин В2. ФАД (флавинадениндинуклеотид) играет роль простетической группы, белковая же часть молекулы флавопротеина действует как фермент. В дыхательной цепи эта белковая часть выступает в качестве НАД-дегидрогеназы, катализируя окисление восстановленного НАД. Водород переносится флавопротеином в виде целых атомов.
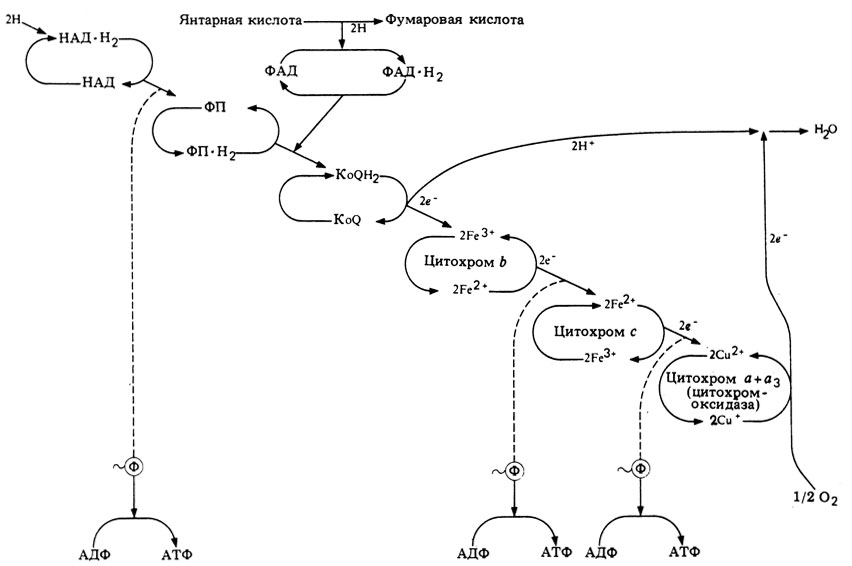
В цикле Кребса белковая часть флавопротеина, простетической группой которого служит ФАД, действует как сукцинатдегидрогеназа. Она катализирует окисление янтарной кислоты в фумаровую. Восстановленный ФАД располагается в дыхательной цепи после первого пункта окислительного фосфорилирования (т. е. синтеза АТФ). Поэтому за счет его обратного окисления синтезируются только две молекулы АТФ (рис. 11.10).
Рис. 11.10. Развернутая схема дыхательной цепи. Каждый цитохром способен передавать только один электрон. Предполагается, что на каждом дыхательном пути действуют два ряда цитохромов. Здесь показан только один, но цифры удвоены, чтобы количества образующихся конечных продуктов соответствовали действительности. В энергетическом смысле электроны перемещаются ‘вниз’
Молекула этого кофермента содержит цикл из шести атомов углерода. Кофермент Q принимает водород от флавопротеина и передает его цитохрому b.
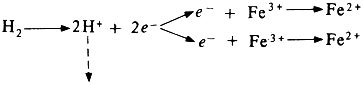
Все цитохромы — это белки с относительно небольшой молекулярной массой. Они содержат тем в качестве прочно связанной простетической группы и переносят не водородные атомы, а электроны. Роль переносящего электроны компонента в цитохромах играет железо гема. Обычно оно находится в окисленной форме (Fe 3+ ), но после присоединения электрона, переходит в восстановленную форму (Fe 2+ ). Каждый водородный атом, поступающий от кофермента Q, распадается на ион водорода и электрон:
Этот электрон присоединяется к иону железа:
Ионы водорода поступают на время в окружающую среду: они понадобятся вновь позднее, в конце дыхательной цепи.
Электрон от цитохрома b переходит к цитохрому с и далее к цитохрому а + а3 — прочному комплексу двух цитохромов, называемому обычно цитохромоксидазой. Этот комплекс, помимо железа, содержит еще и медь и вступает в окислительно- восстановительную реакцию, когда цитохром а3 в конце концов передает электроны кислороду (рис. 11.10). Любой цитохром может переносить только по одному электрону; поэтому полагают, что во всякой дыхательной цепи имеются два ряда цитохромов, которые и осуществляют перенос электронных пар:
Теперь, когда читатель уже кое-что знает о переносчиках водорода и электронов, ему будет легче разобраться и в более подробной схеме дыхательной цепи, приведенной на рис. 11.10.
Источник
Фолиевая кислота обеспечивает накопление в клетках радикалов



Нуклеотиды в ДНК и РНК соединяются между собой
Т-РНК содержит
4) промотор, оператор
5) полиадениловый хвост, антикодон
Железосодержащим белком не является:
Вещество, которое при гидролизе дает только аминокислоты
Миоглобин состоит из:
1) 4 гемов и четырех белковых цепей. .
2 ) 1 гема и одной полипептидной цепи
3 ) 1 гема и четырех полипептидных цепей
4 ) 1 гема и двух полипептидных цепей
5 ) нет правильного ответа
Для максимального связывания кислорода в легких молекула гемоглобина
1) изменяет валентность железа в геме
2) распадается на отдельные субъединицы
3) уменьшает размеры путем сближения субьединиц
4) увеличивает размеры путем расхождения субъединиц
5) отделяет гем от глобина
Полиадениловый «хвост» в иРНК необходим для
1) прикрепления ее к ДНК
2) отсчета времени функционирования иРНК на рибосоме
3) ускорения разрушения нуклеиновой кислоты
4) прикрепления ее к т-РНК
5) узнавания ее белком
Апобелок липопротеина выполняет функцию
Карбоксигемоглобин представляет собой комплекс белка с:
1) с железом в степени окисления +3
3) с углекислым газом
5) с угарным газом
Альбумин крови обладает свойством
1) транспортировать плохо растворимые в воде вещества
2) регулировать иммунные процессы в организме
3) переносить кислород из легких к тканям
4) транспортировать углекислый газ из тканей в легкие
5) ослаблять процесс заживления ран
Небелковой частью протеогликана является:
1) гиалуроновая кислота
2) глютаминовая кислота
3) нейраминовая кислота
4) сиаловая кислота
Наличие пролина в полипептидной цепи препятствует образованию
1) гидрофобных взаимодействий
2) четвертичной структуры
3) водородных связей
4) дисульфидных мостиков
5) глобулярной структуры
Высаливание белков имеет место при:
1) воздействии высоких концентраций солей
2) избытке белка в растворе
3) низкой температуре
4) высокой температуре
5) действии сильных кислот
К фибриллярным белкам относится
Нормальное содержание белка в сыворотке крови в г/л
При гидролизе нуклеозидов образуются:
1) азотистые основания, пентозы и H3PO4;
2) аминокислоты и фосфорная кислота;
3) азотистые основания и пентозы;
5) азотистые основания и H3PO4
Кальцитриол оказывает свое влияние через:
1) аденилатциклазный механизм
2) мембрано-локальный механизм
3) генетический аппарат клетки
4) эндокринную систему
5) нейро-гуморальную систему
В гидроксилировании остатка пролина при синтезе коллагена участвует:
4) двухвалентное железо
5) все ответы правильные
После длительного применения внутрь антибиотиков развивается недостаточность:
При недостатке витамина С происходит нарушение синтеза:
Молекула витамина А обладает:
1) цис-транс- изомерией
2) изомерией углеродной цепи
3) оптической изомерией
4) изомерией положения спиртовой группы
5) кето-енольной изомерией
Органом мишенью альдостерона является:
3) головной мозг
Вазопрессин в почках:
1) стимулирует образование камней
2) увеличивает количество мочи
3) вызывает антидиуретический эффект
4) вызывает блокаду мочеотделения
5) увеличивает клубочковую фильтрацию
Предшественником тироксина является:
Микседема возникает при нарушении функции:
1) передней доли гипофиза
2) задней доли гипофиза
4) паращитовидной железы
5) щитовидной железы
В состав ферментов класса оксидоредуктаз входят витамины:
В состав ферментов АлАТ и АсАТ входит витамин:
Реабсорбцию ионов Са 2+ в почечных канальцах активирует витамин:
Накопителем атомов водорода является активная форма витамина
Витамин В1 участвует в превращении:
2) жирных кислот
3) пировиноградной кислоты
4) молочной кислоты
5) янтарной кислоты
Витамин В2 участвует в превращении:
2) жирных кислот
3) пировиноградной кислоты
4) молочной кислоты
5) янтарной кислоты
Витамин В6 участвует в превращении:
2) жирных кислот
4) молочной кислоты
5) янтарной кислоты
Витамин В12 участвует в синтезе:
1) глутаминовой кислоты
Анемия чаще возникает при недостатке витамина
Анемия чаще возникает при недостатке витамина
2) фолиевой кислоты
3) пантотеновой кислоты
4) амида никотиновой кислоты
Пантотеновая кислота входит в состав
1) никотинамидаденин динуклеотида (НАД)
2) флавинаденин динуклеотида (ФАД)
4) активной формы биотина
5) фолиевой кислоты
Фолиевая кислота обеспечивает накопление в клетках радикалов
Ряд перечисленных витаминов представлены в активной форме:
1) ФАД, ФМН, тиамин
2) НАД, КоА, кокарбоксилаза
3) кальцитриол, пиридоксаль, ФАД
4) кальциферол, тиамин, НАД
5) биотин, фолиевая кислота, кобаламин
Витамин биотин необходим для:
1) накопления атомов водорода
2) переноса аминогруппы
3) превращении пирувата в уксусную кислоту (ацетат)
4) переноса метильных радикалов
5) синтеза жирных кислот
Дерматид, диарея и деменция возникают при отсутствии в пище витамина:
Нарушения функций центральной и периферической нервной систем возникают при отсутствии в пище витамина:
Водорастворимые витамины входят в состав:
2) костной ткани
3) жировой ткани
4) белка коллагена
Витамины обладают лечебным действием, поскольку они:
1 взаимодействуют с гормонами
2 способствуют лучшей растворимости фермента в воде
3 проявляют свойства неорганических катализаторов
4 препятствуют процессу денатурации белка-фермента
5) входят в состав активного центра фермента, участвуя в реакции
Полипептидная часть сложного фермента называется:
5) Простетическая группа.
Ферментом, не относящийся к гидролазам является:
В первые часы после инфаркта миокарда в крови повышается активность:
3) Щелочной фосфатазы.
5) Всех перечисленных ферментов.
Конкурентное ингибирование устраняют:
1) Повышением температуры.
2) Добавление продукта реакции.
3) Добавлением избытка субстрата.
4) Ионами тяжелых металлов.
5) Добавлением избытка фермента.
К классу оксидоредуктаз относят:
Для рассасывания рубцов используют фермент:
Изоферментами называют ферменты:
1) Катализирующие реакцию только в одном направлении
2) Катализирующие превращение близких по строению субстратов.
3) Ферменты разных классов
4) Ферменты, принадлежащие к классу изомераз.
5) Катализирующие одну и ту же реакцию, но различающиеся по строению молекул
Изофермент ЛДГ-1 содержится преимущественно в:
Источник