У эйкозаноидов широкие возможности
К эйкозаноидам (είκοσι, греч.-двадцать) относят окисленные производные эйкозановых кислот: эйкозотриеновой (С20:3), арахидоновой (С20:4), тимнодоновой (С20:5) жирных кислот. Активность эйкозаноидов значительно разнится от числа двойных связей в молекуле, которое зависит от строения исходной жирной кислоты.
Выделяют три основные группы эйкозаноидов: простагландины , лейкотриены , тромбоксаны .
Простагландины (Pg) синтезируются практически во всех клетках, кроме эритроцитов и лимфоцитов. Выделяют типы простагландинов A, B, C, D, E, F. Функции простагландинов сводятся к изменению тонуса гладких мышц бронхов, мочеполовой и сосудистой системы, желудочно-кишечного тракта, при этом направленность изменений различна в зависимости от типа простагландинов, типа клетки и условий. Они также влияют на температуру тела.
Простациклины являются подвидом простагландинов (Pg I), вызывают дилатацию мелких сосудов, но еще обладают особой функцией – ингибируют агрегацию тромбоцитов. Их активность возрастает при увеличении числа двойных связей в исходных жирных кислотах. Синтезируются в эндотелии сосудов миокарда, матки, слизистой желудка.
Тромбоксаны (Tx) образуются в тромбоцитах, стимулируют их агрегацию и вызывают сужение сосудов. Их активность снижается при увеличении числа двойных связей в исходных жирных кислотах.
Лейкотриены (Lt) синтезируются в лейкоцитах, в клетках легких, селезенки, мозга, сердца. Выделяют 6 типов лейкотриенов A, B, C, D, E, F. В лейкоцитах они стимулируют подвижность, хемотаксис и миграцию клеток в очаг воспаления, в целом они активируют реакции воспаления, предотвращая его хронизацию. Также вызывают сокращение мускулатуры бронхов (в дозах в 100-1000 раз меньших, чем гистамин).
Депонироваться эйкозаноиды не могут, разрушаются в течение нескольких секунд, и поэтому клетка должна синтезировать их постоянно из поступающих жирных кислот ω6- и ω3-ряда.
Синтез эйкозаноидов
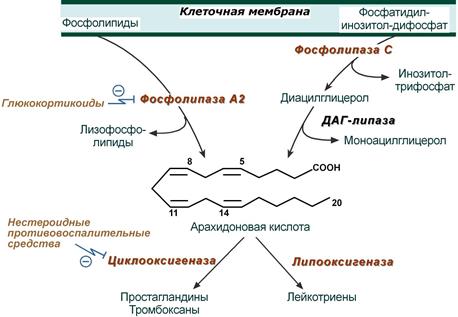
Источником свободных эйкозановых кислот являются фосфолипиды клеточной мембраны .
Под влиянием гистамина, комплекса антиген-антитело, цитокинов, кининов активируются фосфолипаза А2 или комбинация фосфолипазы С и ДАГ-липазы, которые отщепляют жирную кислоту из положения С2 мембранных фосфолипидов.
Синтез эйкозаноидов на примере арахидоновой кислоты.
Химизм реакций циклооксигеназы и липоксигеназы показан здесь .
Полиненасыщенная жирная кислота метаболизирует в основном двумя путями: циклооксигеназным и липоксигеназным , активность которых в разных клетках выражена в разной степени. Циклооксигеназный путь отвечает за синтез простагландинов и тромбоксанов, липоксигеназный – за синтез лейкотриенов.
Лекарственная регуляция синтеза
Гормоны коры надпочечников глюкокортикоиды опосредованно, через синтез специфических белков, подавляют активность фосфолипазы А2 и, следовательно, образование всех типов эйкозаноидов. На этом основано широкое использование препаратов кортизола (преднизолон, дексаметазон) для лечения воспалительных, аутоиммунных и аллергических состояний.
Нестероидные противовоспалительные средства (аспирин, индометацин, ибупрофен) ингибируют циклооксигеназу и снижают выработку простагландинов и тромбоксанов. Они нашли применение как противовоспалительные, жаропонижающие и анальгезирующие средства, и в кардиологии для профилактики тромбозов (аспирин).
Блокирование циклооксигеназы в почках, как побочный эффект салицилатов, вызывает уменьшение синтеза простагландинов в почечных сосудах и снижение кровообращения в почках.
В зависимости от исходной жирной кислоты и, соответственно, числа двойных связей все эйкозаноиды делят на три группы:
Первая группа – синтезируется из эйкозотриеновой кислоты (С20:3), которая образуется из линоленовой (С18:3). В соответствии с количеством двойных связей простагландинам и тромбоксанам присваивается индекс 1, лейкотриенам – индекс 3: например, Pg E1, Pg I1, Tx A1, Lt A3.
Интересно, что PgE1 ингибирует аденилатциклазу в жировой ткани и препятствует липолизу, также он участвует в патогенезе бронхоспазма.
Вторая группа синтезируется из арахидоновой кислоты (С20:4). По тому же правилу ей присваивается индекс 2 или 4, например, Pg E2, Pg I2, Tx A2, Lt A4.
Третья группа эйкозаноидов происходит из тимнодоновой кислоты (С20:5). По числу двойных связей присваиваются индексы 3 или 5: например, Pg E3, Pg I3, Tx A3, Lt A5.
Подразделение эйкозаноидов на группы имеет клиническое значение. Особенно ярко это проявляется на примере простациклинов и тромбоксанов:
| Исходная жирная кислота | Число двойных связей в молекуле | Активность простациклинов | Активность тромбоксанов |
| Линоленовая, С18:3 | 1 |  |  |
| Арахидоновая, С20:4 | 2 | ||
| Тимнодоновая, С20:5 | 3 |
Результирующим эффектом пищевого приема или фармакологического применения более полиненасыщенных жирных кислот является образование тромбоксанов и простациклинов с большим числом двойных связей, что изменяет реологические свойства крови и снижает ее вязкость, понижает тромбообразование, расширяет мелкие сосуды и улучшает кровоснабжение тканей, сн ижает повышенное артериальное давление . Все эти эффекты ценны при нарушениях кровообращения, при атеросклерозе, у кардиологических больных.
Источник
Арахидоновая кислота
Опубликовано сб, 08/06/2019 — 11:12
Арахидоновая кислота ( AA ) представляет собой полиненасыщенную омега-6 жирную кислоту 20: 4 (ω-6) или 20: 4 (5,8,11,14). Это название структурно связано с насыщенной арахидовой кислотой, содержащейся в масле купуацу ( L. arachis — арахис). По своей химической структуре , арахидоновая кислота представляет собой карбоновую кислоту с цепью 20-углерода и четыре циса — двойные связи ; первая двойная связь расположена в шестом углероде от конца омеги.
Арахидоновая кислота представляет собой полиненасыщенную жирную кислоту, присутствующую в фосфолипидах (особенно фосфатидилэтаноламине , фосфатидилхолине и фосфатидилинозитидах ) мембран клеток организма , и она находится в большом количестве в мозге , мышцах и печени. Скелетные мышцы являются особенно активным участком аккумуляции арахидоновой кислоты, на долю которых обычно приходится примерно 10-20% содержания фосфолипидных жирных кислот. Помимо участия в клеточной передаче сигналов в качестве липидного вторичного мессенджера, участвующего в регуляции сигнальных ферментов, таких как изоформы PLC -γ, PLC-δ и PKC -α, -β и -γ, арахидоновая кислота является ключевым воспалительным средством ( промежуточным звеном) и может также действовать как вазодилататор.
Арахидоновая кислота не является одной из незаменимых жирных кислот . Тем не менее, она становится необходимой, если существует дефицит линолевой кислоты или если имеет место невозможность превращения линолевой кислоты в арахидоновую кислоту. У некоторых млекопитающих отсутствует способность или очень ограниченная способность превращать линолевую кислоту в арахидоновую кислоту, что делает ее неотъемлемой частью их рациона.
Арахидоновая кислота освобождается из молекулы фосфолипидов под действием фермента фосфолипазы А2(PLA 2 ), которая расщепляет ее от жирной кислоты , но также может быть получена из группы DAG с помощью диацилглицерола липазы . Арахидоновая кислота, генерируемая для передачи сигналов, по-видимому, образуется под действием цитозольной фосфолипазы A2 группы IVA (cPLA 2 , 85 кДа), тогда как воспалительная арахидоновая кислота генерируется под действием низкомолекулярного секреторного PLA 2 (sPLA 2 , 14-18 кДа).
Арахидоновая кислота является предшественником, который метаболизируется различными ферментами до широкого спектра биологически и клинически важных эйкозаноидов и метаболитов этих эйкозаноидов:
- Ферменты циклооксигеназы -1 и -2 (то есть простагландина G / H-синтазы 1 и 2 < PTGS1 и PTGS2 >) метаболизируют арахидоновую кислоту в простагландин G2 и простагландин H2 , которые, в свою очередь, могут превращаться в различные простагландины , в простациклин , в тромбоксаны , и 17-углеродному продукту метаболизма тромбоксана простагландина G2 / H2, 12-гидроксигептадекатриеновой кислоты (12-HHT).
- Фермент 5-липоксигеназа метаболизирует арахидоновую кислоту до 5-гидропероксиэйкозатетраеновой кислоты ( 5-HPETE ), которая, в свою очередь, метаболизируется с различными лейкотриенами (т.е. лейкотриеном B4 , лейкотриеном C4 , лейкотриеном D4 и лейкотриеновой кислотой E4, а также 5-гидрокси) ( 5-HPETE ) 5-HETE ), который затем может быть далее метаболизирован до более сильного 5-кето-аналога 5-HETE , 5-оксо-эйкозатетраеновой кислоты (5-оксо-ETE)
- Ферменты 15-липоксигеназы-1 ( ALOX15 и 15-липоксигеназы-2 ( ALOX15B метаболизировать арахидоновую кислоту в 15-гидропероксиэйкозатетраеновой кислоты (15-HPETE) , которые затем могут быть дополнительно метаболизируется до 15- гидроксиэйкозатетраеновой кислоты (15-НЕТЕ) и липоксины ; 15-Липоксигеназы-1 может также дополнительно метаболизировать 15-HPETE в эоксины в пути, аналогичном (и предположительно с использованием тех же ферментов, которые используются в) пути, который метаболизирует 5-HPETE в лейкотриены.
- Фермент 12-липоксигеназы ( ALOX12 ) метаболизирует арахидоновую кислоту до 12-гидропероксиэйзатетраеновой кислоты (12-HPETE), которая затем может метаболизироваться до 12-гидроксиейкозатетраеновой кислоты (12-HETE) и до гепоксилинов .
- Арахидоновая кислота также используется в биосинтезе анандамида .
- Некоторая арахидоновая кислота превращается в гидроксиэйкозатетраэновую кислоту (HETEs) и эпоксиэйкозариеновую кислоту (EETs) по эпоксигеназе .
PLA 2 , в свою очередь, активируется связыванием лиганда с рецепторами, включая:
Кроме того, любой агент, увеличивающий внутриклеточный кальций, может вызывать активацию некоторых форм PLA 2
Альтернативно, арахидоновая кислота может отщепляться от фосфолипидов после того, как фосфолипаза с (PLC) отщепляет трифосфатную группу инозита , образуя диацилглицерин (DAG), который впоследствии расщепляется липазой DAG с получением арахидоновой кислоты
Рецепторы, которые активируют этот путь, включают в себя:
PLC также может быть активирован киназой MAP . Активаторы этого пути включают PDGF и FGF/
Арахидоновая кислота способствует восстановлению и росту ткани скелетных мышц путем преобразования в простагландины PGF2-альфа во время и после физических упражнений . PGF2-альфа способствует синтезу мышечного белка путем передачи сигналов через путь Akt / mTOR , подобный лейцину , β-гидрокси β-метилбутировой кислоте и фосфатидной кислоте .
Арахидоновая кислота является одной из самых распространенных жирных кислот в мозге и присутствует в таких же количествах, что и докозагексаеновая кислота (DHA) ( На эти два продукта приходится около 20% содержания жирных кислот. . Помимо прочего, арахидоновая кислота помогает поддерживать текучесть клеточной мембраны гиппокампа . Онf также помогает защитить мозг от окислительного стресса, активируя гамма-рецептор, активируемый пролифератором пероксисом . ARA также активирует синтаксин- 3 (STX-3), белок, участвующий в росте и восстановлении нейронов.
Арахидоновая кислота также участвует в раннем развитии нервной системы . В одном исследовании младенцы (18 месяцев), получавшие дополнительную арахидоновую кислоту в течение 17 недель, продемонстрировали значительное улучшение интеллекта, измеряемое индексом психического развития. Этот эффект дополнительно усиливается одновременным дополнением арахидоновой кислоты докозагексаеновой кислотой.
У взрослых нарушение метаболизма AA может способствовать развитию психоневрологических расстройств, таких как болезнь Альцгеймера и биполярное расстройство . Имеются данные о значительных изменениях в превращении арахидоновой кислоты в другие биоактивные молекулы (избыточная экспрессия или нарушения в каскаде ферментов AA) в этих условиях.
Исследования арахидоновой кислоты в патогенезе болезни Альцгеймера противоречивы : одно исследование АА и его метаболитов предполагает, что они связаны с началом болезни Альцгеймера, в то время как другое исследование предполагает добавление арахидоновой кислоты на ранних стадиях. этого заболевания может быть эффективным в ослаблении симптомов и замедлении прогрессирования заболевания.Необходимы дополнительные исследования по добавкам арахидоновой кислоты для пациентов с болезнью Альцгеймера. Другое исследование показывает, что загрязнение воздуха является источником воспаления, а метаболиты арахидоновой кислоты способствуют воспалению, сигнализируя иммунной системе о повреждении клеток.
Повышенное потребление арахидоновой кислоты не вызовет воспаления при нормальных метаболических условиях, если не смешивать продукты перекисного окисления липидов . Арахидоновая кислота метаболизируется до провоспалительных и противовоспалительных эйкозаноидов во время и после воспалительного ответа соответственно.
Источник
эйкозаноиды
Эйкозаноиды:пути образования,биохимическе эффекты. Действие эйкозаноидов на различные системы организма.
студенты 5п группы
2 курса ІІ мед ф-та
Эйкозаноиды — это общая группа физиологически и фармакологически активных соединений включающая в себя простаноиды (простагландины, простоциклины, тромбоксаны) и лейкотриены. Они имеют очень короткий Т1/2, поэтому оказывают эффекты как «гормоны местного действия». Главный субстрат для синтеза эйкозаноидов у человека — арахидоновая кислота, так как её содержание в организме человека значительно больше остальных полиеновых кислот — предшественников эйкозаноидов. Хотя субстраты для синтеза эйкозаноидов имеют довольно простую структуру (полистовые жирные кислоты), из них образуется большая и разнообразная группа веществ. Наиболее распространены в организме человека простагландины, которые впервые были выделены из предстательной железы, откуда и получили свое название. Позже было показано, что и другие ткани организма синтезируют простагландины и другие эйкозаноиды. Простагландины обозначают символами, например PG А, где PG обозначает слово «простагландин», а буква А обозначает заместитель в пятичленном кольце в молекуле эйкозаноида.Обнаружено шесть первичных природных простагландинов, три из них серии Е (PGE1, PGE2, PGE3) и три — серии F (PGF1a, PGF2a, PGF3a). Простагландины серии Е содержат в положении 9 кетогруппу, а простагландины серии F — гидроксигруппу.
Механизмы действия эйкозаноидов, основные биологические эффекты
Эйкозаноиды — гормоны местного действия по ряду признаков:
— образуются в различных тканях и органах, а не только в эндокринных железах;
— действуют по аутокринному или паракринному механизмам;
— концентрация эйкозаноидов в крови меньше, чем необходимо, чтобы вызвать ответ в клетках-мишенях.
Механизмы действия эйкозаноидов
Один и тот же тип эйкозаноида может действовать по паракринному и по аутокринному механизму. Например, ТХА2, продуцируемый тромбоцитами при их активации, действует на сами тромбоциты, увеличивая их способность к агрегации, и в то же время действует на окружающие ГМК кровеносных сосудов, способствуя их сокращению. Таким образом создаются условия для образования тромба и предотвращения кровотечения в области повреждения сосудов.
Эйкозаноиды действуют на клетки через специальные рецепторы. Некоторые рецепторы эйкозаноидов связаны с аденилатциклазной системой и протеинкиназой А — это рецепторы PGE, PGD, PCI. PGF2α, ТХА2 эндоперекиси (ГПЭТЕ) и лейкотриены действуют через механизмы, увеличивающие уровень кальция в цитозоле клеток-мишеней. Во многих клетках эйкозаноиды влияют на степень активации аденилатциклазной системы в ответ на действие других факторов, например гормонов. В этих случаях эйкозаноиды влияют на конформацию G-белков в плазматической мембране клеток. Если эйкозаноид связывается со стимулирующими Gs-белками, то эффект основного стимулирующего агента увеличивается; если с Gi-ингибирующими — эффект снижается. Эйкозаноиды действуют на клетки почти всех тканей организма. Избыточная продукция эйкозаноидов наблюдается при многих заболеваниях.
После отделения арахидоновой кислоты от фосфолипида она выходит в цитозоль и в различных типах клеток превращается в разные эйкозаноиды. В клетках имеется 2 основных пути превращения арахидоновой кислоты: циклооксигеназный, приводящий к синтезу простагландинов, простациклинов и тромбоксанов, и липоксигеназный, заканчивающийся образованием лейкотриенов. Циклооксигеназный путь: синтез простагландинов и тромбоксанов
С20-три-, тетра — и пентаеновая жирные кислоты, служащие предшественниками простагландинов, входят в состав внутриклеточных фосфоглицеридов, из которых они высвобождаются под действием фосфолипазы А2. Активация фосфолипаз, ассоциированных с мембранами, происходит под действием многих факторов: гормонов, гистамина, цитокинов, механического воздействия. Этот процесс высвобождения предшественника, вероятно, играет роль регулирующей стадии в биосинтезе простагландинов, с помощью которой варьирует количество субстрата, подвергающегося последующему действию простагландинсинтазы. Последняя представляет собой связанный в мембране мультиферментный комплекс, содержащийся в микросомальной фракции тканевых гомогенатов. Необходимо отметить, что ингибиторное действие кортикостероидов на биосинтез простагландинов, связанное с торможением активности фосфолипазы А2, может служить объяснением антивоспалительного действия этих стероидных гормонов.
Фермент, катализирующий первый этап синтеза простагландинов, называется PG Н2 синтазой и имеет 2 каталитических центра. Один из них называют циклооксигеназой, другой — пероксидазой. Этот фермент представляет собой димер гликопротеинов, состоящий из идентичных полипептидных цепей. Фермент имеет гидрофобный домен, погружённый в липидный слой мембран ЭР, и каталитический домен, обращённый в полость ЭР. В активном центре циклооксигеназы находится тирозин (385), в активном центре пероксидазы — простетическая группа — гем. В организме имеются 2 типа циклооксигеназ (PGН2 синтаз). Циклооксигеназа 1 — конститутивный фермент, синтезирующийся с постоянной скоростью. Синтез циклооксигеназы 2 увеличивается при воспалении и индуцируется соответствующими медиаторами — цитокинами. Оба типа циклооксигеназ катализируют включение 4 атомов кислорода в арахидоновую кислоту и формирование пятичленного кольца. В результате образуется нестабильное гидропероксидпроизводное, называемое PG G2. Гидропероксид у 15-го атома углерода быстро восстанавливается до гидроксильной группы пероксидазой с образованием PG Н2. До образования PG Н2 путь синтеза разных типов простагландинов одинаков. Дальнейшие превращения PG Н2специфичны для каждого типа клеток.
Превращение арахидоновой кислоты в PGG2 блокируется ингибиторами циклооксигеназы жирных кислот. Наиболее известным среди этих ингибиторов являются аспирин (ацетилсалициловая кислота) и ряд других противовоспалительных лекарств. Торможение аспирином обусловлено переносом ацетильного остатка от молекулы аспирина к активному центру фермента с инактивацией последнего; такого рода механизм был предложен в качестве объяснения некоторых известных фармакологических эффектов аспирина.
Аспирин — препарат, подавляющий основные признаки воспаления. Механизм противовоспалительного действия аспирина стал понятен, когда обнаружили, что он ингибирует циклооксигеназу. Следовательно, он уменьшает синтез медиаторов воспаления и, таким образом, уменьшает воспалительную реакцию. Циклооксигеназа необратимо ингибируется путём ацетилирования серина в положении 530 в активном центре. Однако эффект действия аспирина не очень продолжителен, так как экспрессия гена этого фермента не нарушается и продуцируются новые молекулы фермента. Другие нестероидные противовоспалительные препараты (например, ибупрофен и ацетаминофен) действуют по конкурентному механизму, связываясь в активном центре фермента, и также снижают синтез простагландинов.
Действие эйкозаноидов на сердечно-сосудистую систему
Внутривенное введение PGE1 или PGE2 увеличивает кровоток путем общего расширения сосудов с уменьшением периферического сопротивления. Эти изменения находят отражение в увеличении сердечного выброса, сопровождающегося уменьшением артериального кровяного давления.
При изучении факторов риска инфаркта миокарда было показано, что люди, потребляющие большое количество рыбьего жира, значительно меньше подвержены этому заболеванию, так как у них реже образуются тромбы в сосудах сердца. Оказалось, что на семейства эйкозаиоидов, синтезируемых в организме, влияет состав жирных кислот пищи. Если с пищей поступает больше эйкозапентаеновой кислоты (20: 5, ω-3), в большом количестве содержащейся в рыбьем жире, то эта кислота включается преимущественно в фосфолипиды мембран (вместо арахидоновой) и после действия фосфодипазы А2 служит основным субстратом для синтеза эйкозаноидов. Это имеет существенное влияние на свёртывание крови. При обычной диете с преобладанием арахидоновой кислоты (20: 4, ω-6) над эйкозапентаеновой действие ТХА2 уравновешено действием PG I2 и другими простагландинами. В случае диеты с преобладанием ω-3 кислот в клетках эндотелия образуются более сильные ингибиторы тромбообразования (PGI3, PGE3, PGD3), что снижает риск образования тромба и развития инфаркта миокарда.
Действие на водно-электролитный обмен
Все изученные простагландины усиливают ионный поток через эпителиальные мембраны. Введение PGE1 или PGA1 в почечную артерию собак увеличивает объем мочи и выделение Na + , K + и Сl — . Напротив, сообщалось, что местное образование PGE2 в почке подавляет выведение Na+.
Действие на нервную систему
Простагландины присутствуют в нервной ткани и освобождаются при раздражении периферических нервов. Введенные простагландины повышают температуру тела, оказывают седативное и транквилизирующее действие и являются антагонистами противосудорожных препаратов. Простагландины модулируют действие адренергическнх факторов, например норадреналина, и являются антагонистами некоторых эффектов этих катехоламинов.
Действие на желудочно-кишечный тракт
Простагландины тормозят желудочную секрецию, но стимулируют секрецию поджелудочной железы и секрецию слизи в кишечнике, а также заметно усиливают моторику кишечника. Стимулируя кишечную аденилатциклазу, простагландины могут ингибировать поступление Na+ в клетки слизистой оболочки, что сопровождается увеличением секреции Сl — . Эти эффекты в сочетании с увеличением секреции Н2О и кишечной моторики являются основанием для развития вызываемой простагландинами диареи.
Влияние на репродуктивную систему
Простагландины, особенно PGF2a, стимулируют активность матки в период беременности; это нашло практическое применение при вызывании аборта, а именно изгнании плода и плаценты. Что бы вызвать аборт, требуются очень маленькие количества простагландинов, введенных внутривенно или непосредственно в полость матки. Как in vitro, так и in vivo PGF2a вызывают рассасывание функционирующего желтого тела и могут таким образом облегчать прерывание беременности, снижая уровень прогестерона в плазме крови.
Воздействия на бронхи, трахею и гладкие мышцы
Простагландины серии F вызывают сокращение, а простагландины серии Е раслабление мышц бронхов и трахеи у животных различных видов, в том числе у человека. Как PGE1 так и PGE2 являются сильными бронходилятаторами (средствами, расширяющими просвет бронхов и бронхиол) при применении их в аэрозолях как людьми, так и животными, страдающими бронхоспазмами. В противоположность этому PGF2a вызывает интенсивное сокращение бронхов и бронхоспазм.
Влияние PGF2a на гладкие мышцы матки было описано выше. В течение ряда лет было известно, что специфический модулятор, названный веществом, сокращающим аорту кролика (rabbit aorta contracting substance (RCS)), выделяется при анафилаксии в легких сенсибилизированных морских свинок. Недавно установили, что это вещество является смесью PGG2, PGH2 и тромбоксана А2, причем большая часть RCS-активности связана именно с тромбоксаном А2. Согласно существующему мнению, выделение RCS контролируется декапептидом, который стимулирует образование эндопероксидов PG и тромбоксана А2 путем ускорения освобождения арахидоновой кислоты из легочной ткани.
Использование производных эйкозаноидов в качестве лекарств
Хотя действие всех типов эйкозаноидов до конца не изучено, имеются примеры успешного использования лекарств — аналогов эйкозаноидов для лечения различных заболеваний. Например, аналоги PGЕ1 и PGЕ2подавляют секрецию соляной кислоты в желудке, блокируя гистаминовые рецепторы II типа в клетках слизистой оболочки желудка. Эти лекарства, известные как Н2-блокаторы, ускоряют заживление язв желудка и двенадцатиперстной кишки. Способность PGЕ2 и PGF2α стимулировать сокращение мускулатуры матки используют для стимуляции родовой деятельности.
Березов Т.Т. , Коровкин Б.Ф. Биологическая химия. Под ред. Дебова С.С. / М., «Медицина», 1990.
Николаев А.Я. Биохимия. / М., «Высшая школа», 1989.
Строев Е.А. Биологическая химия. / М., «Высшая школа», 1986.
Филиппович Ю.Б. Основы биохимии.– М.: Высшая школа, 1994.
Gennis R. Biomembranes, molecular structure and function.– 1992
Источник