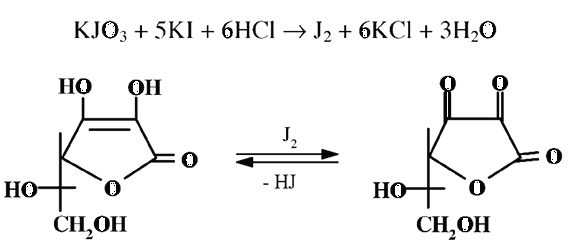Ход работы
Задание 2. Количественное определение витамина с 2,6–дихлорфенолиндофенолом (по Тильмансу)
Метод количественного определения аскорбиновой кислоты основан на ее способности восстанавливать 2,6–дихлорфенолиндофенол, которым титруют исследуемый раствор в кислой среде, предохраняющей аскорбиновую кислоту от разрушения. Точному количественному определению аскорбиновой кислоты могут мешать другие легко окисляемые вещества, такие, как глютатион, цистеин и др.
Ход работы
1. Приготовьте вытяжку из хвои. Точную навеску хвои массой1 г тщательно разотрите в фарфоровой ступке со щепоткой битого стекла (песка) с 5 мл
2 % – го раствора соляной кислоты, затем без потерь (обмывая ступку и пестик тем же раствором соляной кислоты) перенесите содержимое ступки в мерную колбу емкостью 50 мл и доведите дистиллированной водой до метки. Содержимое колбы тщательно перемешайте, профильтруюете через бумажный фильтр, фильтрат используйте для определения витамина С.
2. Титрование. В 2 конические колбочки отмерьте пипеткой по 5 мл фильтрата, и протитруйте из бюретки0,001 Мрастаором 2,6–дихлорфенолиндофенола до появления розового окрашивания, не исчезающего около 30 с.
Расчет количества аскорбиновой кислоты в пробе проведите исходя из того, что 1 мл 0,001 М раствора 2,6 – дихлорфенолиндофенола соответствует 0,088 мг аскорбиновой кислоты. При расчете на 100 г вещества необходимо учитывать также разведение и количество исходного вещества.
Источник
Методические рекомендации по выполнению лабораторной работы № 13
на заседании комиссии математического и общего естественнонаучного цикла
Протокол № __ от «__»________2013 г.
Пр. № __от «__»_______ 2013 г.
По дисциплине: «Естествознание»
Наименование работы: «Определение содержания витамина С в напитках»
По специальности:080110 «Банковское дело» (базовая и углубленная подготовка)
Работа рассчитана на 2 часа
ЛАБОРАТОРНАЯ РАБОТА № 13
Тема: «Определение содержания витамина С в напитках»
Цели урока:
1. Образовательная: научиться определять содержание витамина С в напитках. Закрепить навыки составления уравнений химических реакций.
2. Развивающая: развивать навыки решения задач, логическое мышление и творческое воображение. Формирование умений пользоваться теоретическими и экспериментальными методами химической науки для обоснования выводов по изучаемой теме.
3. Воспитательная: развитие самостоятельности, взаимопомощи.
Формируемые компетенции: ОК 2, ОК 3, ОК 11.
Литература: , , под ред. Алексашиной 10 класс (базовый уровень) — М.: Просвещение, 2010, Гл.2, §32, стр.96-101.
Карпенков естествознание Гл. 6, §4, стр.307-312.
Оборудование: стаканы, пипетка или шприц на 5 мл (без иглы), спиртовая горелка, реактивы (крахмал, дистиллированная вода, спиртовый раствор иода, таблетки аскорбиновой кислоты, образцы соков, железные гвозди, лимонная кислота)
Инструктаж по технике безопасности и проведению эксперимента (5 мин.)
Контрольные вопросы допуска
1. Что представляет собой витамин С?
2. Какими физическими свойствами обладает витамин С?
3. В каких продуктах питания содержат много витамина С?
1. Приготовление крахмального клейстера
Всыпьте в стакан с небольшим количеством холодной воды немного крахмала. Тщательно перемешайте. Добавьте к полученной смеси горячую воду и опять перемешайте. Крахмальный клейстер готов.
2. Приготовление водного раствора йода
Растворите в 100 мл воды 20-30 капель спиртового раствора йода, чтобы окраска раствора по цвету напоминала крепкий чай. Наполните пипетку или шприц раствором йода.
3. Приготовление контрольного раствора аскорбиновой кислоты
Растворите 2 таблетки аскорбиновой кислоты (по 0,025г) в 50 мл воды. Отберите 5мл полученного раствора в стакан для титрования. Добавьте несколько капель крахмального клейстера. Медленно, по каплям, из пипетки или шприца добавляйте раствор йода к анализируемому раствору, постоянно его взбалтывая. Продолжайте добавлять йод, пока не появится устойчивая синяя окраска (не исчезает более 20 с).
4.Запишите объем раствора йода, пошедший на титрование.
5. Повторите опыт еще раз с 5 мл контрольного раствора аскорбиновой кислоты.
6. Возьмите среднее значение. Этот объем раствора йода V0 соответствует 5 мг аскорбиновой кислоты.
7. Проведите анализ различных соков на содержание аскорбиновой кислоты. Для этого в чистый стакан отмерьте 5 мл исследуемого сока и выполните пункты 2-6 приведенной выше методики.
8. Занесите результаты в таблицу.
Количество мл раствора йода
Количество мг аскорбиновой кислоты в 5 мл раствора
Для расчета массы аскорбиновой кислоты воспользуйтесь формулой: m1=5V1:V0 , m2=5V2:V0 и т. д.
9. Проведите дополнительное исследование на устойчивость аскорбиновой кислоты к кипячению. Приготовьте контрольный раствор (пункт 1) и прокипятите его в течение 10 минут. Возьмите 5 мл пробы и повторите пункты 2-6. Сравните полученный результат с данными для контрольного раствора.
10. Проведите дополнительное исследование на устойчивость аскорбиновой кислоты к контакту с железом. Опустите в контрольный раствор аскорбиновой кислоты гвозди на 30 минут. Возьмите 5 мл пробы и повторите пункты 2-6. Сравните полученный результат с данными для контрольного раствора.
11. Проведите дополнительное исследование на повышение стабилизации аскорбиновой кислоты при добавлении небольшого количества лимонной кислоты. Добавьте в контрольный раствор аскорбиновой кислоты немного лимонной кислоты. Возьмите 5 мл пробы и повторите пункты 2-6. Сравните полученный результат с данными для контрольного раствора.
12. Результаты занесите в таблицу.
Количество мг аскорбиновой кислоты
в 5 мл раствора
Контакт с железом
Добавление лимонной кислоты
13. Запишите уравнение реакции:
1. Какое воздействие оказывает витамин С на человеческий организм?
2. Какова суточная потребность человека в витамине С?
3. Какие овощи и фрукты наиболее богаты витамином С?
4. Форма отчета о работе: заполненная таблица в тетради для лабораторных работ
Краткие теоретические сведения
Витамин С, известный также как аскорбиновая кислота относится к водорастворимым витаминам. Аскорби́новая кислота́ — органическое соединение, родственное глюкозе, является одним из основных веществ в человеческом рационе, которое необходимо для нормального функционирования соединительной и костной ткани. Выполняет биологические функции восстановителя и кофермента некоторых метаболических процессов, является антиоксидантом. Биологически активен только один из изомеров — L-аскорбиновая кислота, который называют витамином C. Из всех необходимых для человеческого организма витаминов больше всего по количеству нужно витамина С – в среднем 80 мг в сутки, в то время как потребность во всех остальных витаминах составляет в сумме 20 мг в сутки.
По физическим свойствам аскорбиновая кислота представляет собой белый кристаллический порошок кислого вкуса. Легко растворим в воде, растворим в спирте. Очень неустойчив, легко реагирует с кислородом и теряет активность под действием света и тепла.
Витамин C – самый мощный естественный водорастворимый антиоксидант, предохраняющий от разрушительного действия окислителей. Он нейтрализует потенциально вредные реакции в насыщенных водой частях организма, например, в крови и в около — и внутриклеточной жидкости. Кроме того, антиокислительные свойства витамина C защищают «здоровый» (LDL) холестерин от воздействия свободных радикалов, а также способствуют предотвращению рака, сердечных болезней, симптомов старения и множества других недугов
При нехватки в организме витамина С появляется слабость иммунной системы, кровоточивость дёсен, бледность и сухость кожи, замедленное восстановление тканей после физических повреждений (раны, синяки), потускнение и выпадение волос, ломкость ногтей, вялость, быстрая утомляемость, ослабление мышечного тонуса, ревматоидные боли в крестце и конечностях (особенно нижних, боли в ступнях), расшатывание и выпадение зубов; хрупкость кровеносных сосудов приводит к кровоточивости дёсен, кровоизлияниям в виде тёмно-красных пятен на коже. Однако достаточно надежно не установлена связь между упомянутыми симптомами и недостатком в организме витамина C. Лишь когда его количество принимает крайне малые значения, проявляются некоторые из перечисленных симптомов, сигнализирующих о возникновении крайне редкого ныне заболевания — цинги.
Избыток витамина C может вызывать раздражение мочевого тракта (при длительном употреблении), кожный зуд, понос.
Организм не способен сам синтезировать витамин С, поэтому необходимо, по возможности, круглогодично есть свежие фрукты, овощи, зелень, употреблять настои лекарственных растений, содержащих витамин С. В природе аскорбиновая кислота содержится во многих фруктах и овощах. Наиболее богаты аскорбиновой кислотой плоды барбадосской вишни (1000-3300 мг/100 г), свежего шиповника (650 мг/100 г), болгарского красного перца (250 мг/100 г), чёрной смородины и облепихи (200 мг/100 г), перец зелёный сладкий и петрушка (150 мг/100 г), брюссельская капуста (120 мг/100 г), укроп и черемша (колба) (100 мг/100 г), киви (90 мг/100 г), земляника садовая (60 мг/100 г), цитрусовые (38-60 мг/100 г), яблоки (содержат 4,6 мг/100 г), недозрелые плоды грецкого ореха, хвоя сосны и пихты.
Источник
Пищевая химия: учебник для студентов вузов
Лабораторная работа 35. Титриметрические методы определения витамина С
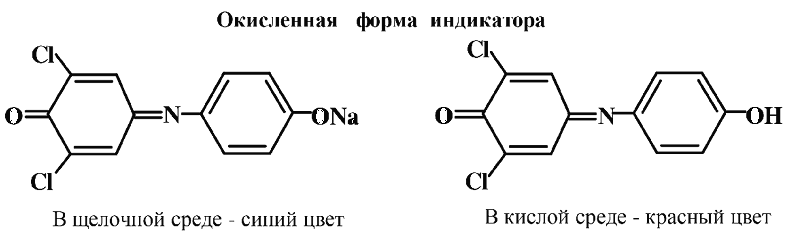
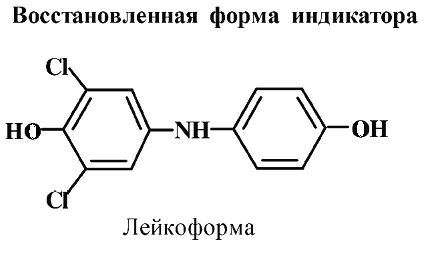
Сущность титриметрического метода заключается в том, что 2, 6-дихлорфенолиндофенол выступает не только как окислитель, но и как индикатор, по которому определяют окончание титрования. Окраска раствора 2, 6-дихлорфенолиндофенола зависит от рН среды, а при восстановлении он переходит в лейкоформу.
Количественное определение ведут путем добавления к подкисленному раствору, содержащему витамин С, щелочного раствора краски Тильманса. Пока в титруемом растворе содержится витамин С, добавляемый раствор 2, 6-дихлорфенолиндофенола, имеющий глубокий синий цвет, обесцвечивается с образованием лейкоформы (индикатор), за счет присутствия восстановленной формы АК. Как только все количество АК в анализируемом растворе окислится до ДАК, раствор приобретает красную окраску, характерную для окисленной формы 2, 6-дихлорфенолиндофенола в кислой среде. Метод стандартизирован (ГОСТ 30627.2–98 – Методы измерений массовой доли витамина С (аскорбиновой кислоты).
Ход анализа . Точную навеску (около 5–10 г) предварительно измельченного исследуемого материала поместить в фарфоровую ступку. Небольшими порциями добавить 20 мл 1%-го раствора соляной кислоты, тщательно растирая пробу до получения однородной кашицы. Смесь количественно перенести в мерную колбу вместимостью 100 мл (общий объем соляной кислоты не должен превышать 50 мл). Ступку и пестик ополоснуть 1%-м раствором щавелевой кислоты и собрать смывы в ту же мерную колбу. Объем раствора довести до метки раствором щавелевой кислоты.
Содержимое колбы перемешать и через 5 минут отфильтровать через складчатый фильтр в сухую колбу или центрифугировать. Полученный фильтрат или фугат в количестве 1–10 мл (в зависимости от содержания витамина) отобрать пипеткой в коническую колбу и довести объем раствора дистиллированной водой до 15 мл. Анализируемый раствор оттитровать из микробюретки 0,001 н раствором 2, 6-дихлор-фенолиндофенола до появления розового окрашивания, не исчезающего в течение 30–60 с.
Контрольный опыт . Для оценки поправки на присутствие других редуцирующих веществ в используемых реагентах к 10 мл фильтрата или фугата прилить 0,1 мл 10%-го раствора сернокислой меди и выдержать при температуре 110 0 С в течение 10 минут для разложения АК. После охлаждения добавить 5 мл дистиллированной воды и оттитровать анализируемый раствор из микробюретки 0,001 н раствором 2, 6-дихлорфенолиндофенола. Для титруемого объема в 15 мл объем титранта, пошедшего на контрольный опыт, обычно составляет 0,04–0,06 мл. Эту поправку необходимо вычесть из объема титранта, пошедшего на титрование опытного образца. Рассчитать массовую долю аскорбиновой кислоты ( С АК , мг %) в анализируемом материале по формуле
C A K = T × V 1 × V 2 m × V 3 × 100 ,
где Т – титр 0,001 н раствора 2, 6-дихлорфенолиндофенола по аскорбиновой кислоте, 0,088 мг/мл;
V 1 – объем 0,001 н раствора 2, 6-дихлорфенолиндофенола, пошедшего на титрование экстракта с учетом поправки на реагенты, мл;
V 2 – общий объем экстракта, 100 мл;
V 3 – объем экстракта, взятого на титрование, 15 мл;
m – масса навески исследуемого материала, г;
100 – коэффициент пересчета на 100 г.
Определение витамина С в окрашенных растворах
Многие растительные материалы дают окрашенные экстракты, что затрудняет определение АК путем прямого титрования краской Тильманса. В этом случае титрование ведут в присутствии растворителей, которые сами нерастворимы в воде, но растворяют краску и не растворяют пигменты экстракта, таких как хлороформ или смесь толуола и изобутилового спирта (1:1).
Ход анализа . Точную навеску (около 5–10 г) растительного материала растереть в фарфоровой ступке в 20 мл 1%-ной соляной кислоты. Полученный гомогенат количественно перенести в мерную колбу вместимостью 100 мл и довести объем до метки 1%-ным раствором щавелевой кислоты. Соотношение соляной и щавелевой кислот должно составить 1:5. Содержимое колбы перемешать и через 5 минут отфильтровать через складчатый фильтр в сухую колбу.
В пробирку вместимостью 20 мл отмерить пипеткой 5 мл отфильтрованного окрашенного экстракта, добавить мерным цилиндром 5 мл хлороформа и оттитровать 0,001 н раствором 2, 6-дихлор-фенолиндофенола при осторожном перемешивании, наклоняя пробирку. Титрование прекратить при появлении красного окрашивания в слое хлороформа.
Для оценки поправки на реагенты приготовить контрольный раствор. В качестве контрольного раствора использовать 5 мл смеси из 1%-ных растворов соляной и щавелевой кислот (в соотношении объемов 1:5) и 5 мл хлороформа. Объем титранта, пошедший на контрольный опыт, необходимо вычесть из объема титранта, пошедшего на титрование опытного образца. Рассчитать массовую долю аскорбиновой кислоты ( С АК , мг %) по формуле
C A K = T × V 1 × V 2 m × V 3 × 100 ,
где Т – титр 0,001 н раствора 2, 6-дихлорфенолиндофенола по аскорбиновой кислоте, 0, 088 мг/мл;
V 1 – объем 0,001 н раствора 2, 6-дихлорфенолиндофенола, пошедшего на титрование экстракта с учетом поправки на контрольный опыт, мл;
V 2 – общий объем экстракта, 100 мл;
V 3 – объем экстракта, взятого на титрование, 5 мл;
m – масса навески исследуемого материала, г;
100 – коэффициент пересчета на 100 г.
Определение содержания витамина С в молочных продуктах
Содержание витамина С в сыром молоке зависит от времени года, индивидуальных особенностей животного и колеблется в интервале 0,3–2 мг%. В свежем молоке 67–68% приходится на восстановленную форму витамина С (АК) и 22–33% на окисленную (ДАК). Окисление витамина С в молоке катализирует аскорбатоксидаза и ускоряется в присутствии металлов (железа, меди), света, воздуха. Прямому определению АК в молоке препятствуют белки, способные связывать 2, 6-дихлорфенолиндофенол. В связи с этим определение АК ведут в безбелковом фильтрате. Белки осаждают с помощью насыщенного раствора хлорида натрия или раствора кислоты (метафосфорной, щавелевой, соляной).
Ход анализа . Навеску анализируемого молочного продукта (10 г) растворить 15–25 мл 6%-го раствора метафосфорной кислоты, количественно перенести в мерную колбу вместимостью 50 мл и довести объем смеси до метки тем же раствором кислоты (вместо метафосфорной кислоты можно использовать 2%-ный раствор соляной кислоты). Полученную смесь перемешать и отфильтровать. В коническую колбу для титрования отобрать пипеткой 1 мл фильтрата, довести объем до 15 мл дистиллированной водой и оттитровать из микробюретки 0,001 н раствором 2,6-дихлорфенолиндофенола до появления слаборозового окрашивания, не исчезающего в течение 30–60 с.
Рассчитать массовую долю аскорбиновой кислоты ( С АК , мг %) в анализируемом молоке по формуле
C A K = T × V 1 × V 2 m × V 3 × 100 ,
где Т – титр 0,001 н раствора 2, 6-дихлорфенолиндофенола по аскорбиновой кислоте, 0,088 мг/мл;
V 1 – объем 0,001 н раствора 2, 6-дихлорфенолиндофенола, пошедшего на титрование анализируемого образца с учетом поправки на реагенты, мл;
V 2 – общий объем раствора, 50 мл;
V 3 – объем раствора, взятого на титрование, 1 мл;
m – масса навески исследуемого материала, г;
100 – коэффициент пересчета в проценты.
Упрощенный йодатный метод определения витамина С в молоке
В основе йодатного метода лежит реакция окисления АК йодноватокислым калием до ДАК.
Определение витамина С упрощенным йодатным методом не применяют для анализа жидких концентратов из плодов шиповника, консервированных продуктов, свежеотжатых соков, свежих плодов, овощей, сушенных продуктов, витаминизированных чаев.
Ход анализа . Экстракцию витамина С провести с использованием 2%-го раствора соляной кислоты по методике, указанной выше. На анализ отобрать 1–5 мл экстракта (в зависимости от содержания витамина С) в коническую колбу вместимостью 100 мл, куда заранее добавить 0,5 мл 1%-го раствора йодистого калия, 1 мл 1%-го раствора крахмала и воды (3,5–7,5мл) с таким расчетом, чтобы общий объем смеси составил 10 мл. Полученный раствор оттитровать из микробюретки 0,001 н раствором йодноватокислого калия до появления устойчивого слабо синего окрашивания. Рассчитать содержание аскорбиновой кислоты ( С АК , мг %) в анализируемом молоке по формуле
C A K = T × V 1 × V 2 m × V 3 × 100 ,
где Т – титр 0,001 н раствора йодноватокислого калия по аскорбиновой кислоте, 0,088 мг/мл;
V 1 – объем 0,001 н раствора йодноватокислого калия, пошедшего на титрование анализируемого образца с учетом поправки на контрольный раствор, мл;
V 2 – общий объем экстракта, 1–5 мл;
V 3 – объем раствора, взятого на титрование, 10 мл;
m – масса навески исследуемого материала, г;
100 – коэффициент пересчета в проценты
Контрольный опыт . В коническую колбу отмерить 0,5 мл 1%-го раствора йодистого калия, 1 мл 1%-го раствора крахмала, 1 мл 2%-го раствора соляной кислоты и воды с таким расчетом, чтобы общий объем жидкости составил 10 мл, и оттитровать из микробюретки 0,001 н раствором йодноватокислого калия до появления устойчивого слабо синего окрашивания.
Необходимые реактивы, посуда, оборудование :
§ 1-, 2%-ные растворы соляной кислоты, 1%-ный раствор щавелевой кислоты, 6%-ный раствор метафосфорная кислота (Н n P n O 3n ), 10%-ный раствор сульфата меди, 2%-ный раствор серной кислоты, аскорбиновая кислота кристаллическая, 1%-ный раствор крахмала, 0,001 н раствор 2,6-дихлор-фенолиндофенола, аскорбиновая кислота кристаллическая, хлороформ, 1%-ный раствор йодистого калия, 0,001 н раствор йодноватокислого калия ( KJO 3 ), кристаллический йодид калия;
§ колбы для титрования, пипетки, микробюретки, фарфоровые ступки с пестиком, мерные колбы вместимостью 50 мл, 100 мл, делительные воронки, воронки для фильтрования, мерные цилиндры, пробирки;
§ аналитические весы, центрифуга, термостат на 110 0 С.
1%-ный раствор соляной кислоты . В мерную колбу вместимостью 1000 мл отмерить 23 мл соляной кислоты плотностью 1,185 г/мл, развести 300 мл дистиллированной воды и довести объем раствора до метки.
0,001 н раствор йодноватокислого калия ( KJO 3 ) . Навеску йодата калия 0,03568 г растворить в небольшом количестве дистиллированной воды в мерной колбе вместимость 1 л и довести объем раствора до метки.
0,001 н раствор 2,6-дихлорфенолиндофенола ( краска Тильманса ) . Навеску краски около 0,2 г растворить в 300 мл свежепрокипяченной теплой дистиллированной воды, добавить 20–30 капель 0,01 н раствора гидроксида калия или натрия и количественно перенеси в колбу вместимостью 1000 мл. Объем раствора довести до метки и отфильтровать. Титр раствора определить по йодноватокислому калию.
Определение титра раствора 2,6-дихлорфенолиндофенола по йодноватокислому калию. В мерной колбе вместимостью 50 мл растворить 1 мг кристаллической аскорбиновой кислоты в 30 мл раствора 2%-ной серной кислоты и довести объем до метки тем же раствором кислоты. В две конические колбы для титрования отобрать по 5 мл приготовленного раствора аскорбиновой кислоты. Раствор в одной колбе оттитровать 0,001 н раствором 2,6-дихлорфенолиндофенолом до появления розового окрашивания, не исчезающего в течение 30 с. Во вторую колбу добавить несколько кристалликов йодида калия (около 1–2 мг), 5 капель 1%-го раствора крахмала и оттитровать 0,001 н раствором йодноватокислого калия до появления едва заметного синего окрашивания.
Исходя из того, что 1 мл 0,001 н раствора йодноватокислого калия, а следовательно, и 2,6-дихлорфенолиндофенола, эквивалентен 0,088 мг аскорбиновой кислоты, рассчитать титр раствора 2,6–дихлор-фенолиндофенола ( Т, мг/мл) по аскорбиновой кислоте по формуле
T = 0 , 088 × V 1 V 2 ,
где 0,088 – количество аскорбиновой кислоты, соответствующее 1 мл 0,001 н раствора йодноватокислого калия, мг/мл;
V 1 – объем 0,001 н раствора йодата калия, израсходованного на титрование раствора аскорбиновой кислоты, мл;
V 2 – объем раствора 2,6-дихлорфенолиндофенола, израсходованное на титрование, мл.
Источник