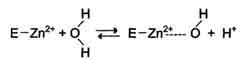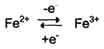Коферментом может являться витамин ион металла
Название работы: Кофакторы ферментов: ионы металлов и коферменты. Коферментные функции витаминов (на примере витаминов В6, РР, В2)
Предметная область: Биология и генетика
Описание: Коферментные функции витаминов на примере витаминов В6 РР В2. Большинство ферментов для проявления ферментативной активности нуждается в низкомолекулярных органических соединениях небелковой природы коферментах и или в ионах металлов кофакторах. В ряде случаев ион металла может способствовать присоединению кофермента.
Дата добавления: 2015-02-20
Размер файла: 115.95 KB
Работу скачали: 17 чел.
Кофакторы ферментов: ионы металлов и коферменты. Коферментные функции витаминов (на примере витаминов В6, РР, В2).
Большинство ферментов для проявления ферментативной активности нуждается в низкомолекулярных органических соединениях небелковой природы (коферментах) и/или в ионах металлов (кофакторах).
Кофакторы выполняют функцию стабилизаторов молекулы субстрата, активного центра фермента и конформации белковой молекулы фермента, а именно третичной и четвертичной структур. В некоторых случаях ионы металла служат «мостиком» между ферментом и субстратом. Они выполняют функцию стабилизаторов активного центра, облегчая присоединение к нему субстрата и протекание химической реакции. В ряде случаев ион металла может способствовать присоединению кофермента. Перечисленные выше функции выполняют такие металлы, как Mg2+, Mn2+, Zn2+, Co2+, Мо2+. В отсутствие металла эти ферменты активностью не обладают. Такие ферменты получили название «металлоэнзимы». Схематично данный процесс взаимодействия фермента, субстрата и металла можно представить следующим образом:
Кофермент , локализуясь в каталитическом участке активного центра, принимает непосредственное участие в химической реакции, выступая в качестве акцептора и донора химических группировок, атомов, электронов. Кофермент может быть связан с белковой частью молекулы ковалентными и нековалентными связями. В первом случае он называется простетической группой (например, FAD, FMN, биотин, липоевая кислота). Вместе с тем известны примеры, когда кофермент присоединяется к ферменту нековалентными связями настолько прочно, что не диссоциирует от белковой молекулы, например тиаминдифосфат. Во втором случае кофермент взаимодействует с ферментом только на время химической реакции и может рассматриваться в качестве второго субстрата. Примеры — NAD+, NADP+. Апофермент обеспечивает специфичность действия и отвечает за выбор типа химического превращения субстрата. Один и тот же кофермент, взаимодействуя с различными апоферментами, может участвовать в разных химических превращениях субстрата. Например, пиридоксальфосфат в зависимости от того, с каким апоферментом взаимодействует, участвует в реакциях трансаминирования или декарбоксилирования аминокислот.
Химическая природа коферментов, их функции в ферментативных реакциях чрезвычайно разнообразны. Традиционно к коферментам относят производные витаминов, хотя помимо них есть значительный класс небелковых соединений, принимающих участие в проявлении каталитической функции ферментов.
К коферментам относят следующие соединения:
- производные витаминов;
- гемы, входящие в состав цитохромов, каталазы, пероксидазы, гуанилатциклазы, NO-синтазы и являющиеся простетической группой ферментов;
- нуклеотиды — доноры и акцепторы остатка фосфорной кислоты;
- убихинон, или кофермент Q, участвующий в переносе электронов и протонов в ЦПЭ;
- фосфоаденозилфосфосульфат, участвующий в переносе сульфата;
- S-аденозилметионин (SAM) — донор метильной группы;
- глутатион, участвующий в окислительно-восстановительных реакциях.
Витамин РР входит в состав кофермента НАД+ и НАДФ+, который принимает участие в ферментативных реакциях по последовательному механизму. Две ферментативные реакции, катализируемые ферментами Е1 и Е2, сопряжены друг с другом посредством кофермента NAD+, служащего в каждом из этих случаев субстратом. Для первого фермента субстратом служит окисленная форма NAD, в качестве второго субстрата выступает донор водорода — пример последовательных реакций, продуктом — восстановленная форма NAD, для фермента Е2 — наоборот.
Витамин В5 принимает участие в синтезе кофермента А (Ацетил-КоА). Кофермент А (КоА) кофермент ацетилирования; один из важнейших коферментов; принимает участие в реакциях переноса ацильных групп . Молекула КоА состоит из остатка адениловой кислоты , связанной пирофосфатной группой с остатком пантотеновой кислоты , соединённой пептидной связью с остатком β-меркаптоэтаноламина .
С КоА связан ряд биохимических реакций, лежащих в основе окисления и синтеза жирных кислот , биосинтеза жиров, окислительных превращений продуктов распада углеводов. Во всех случаях КоА действует в качестве промежуточного звена, связывающего и переносящего кислотные остатки на другие вещества. При этом кислотные остатки в составе соединения с КоА подвергаются тем или иным превращениям, либо передаются без изменений на определённые метаболиты.
Витамин В2 принимает участие в формировании кофактора ФАД и ФМН. Флавинадениндинуклеотид кофактор , принимающий участие во многих окислительно-восстановительных биохимических процессах. FAD существует в двух формах окисленной и восстановленной, его биохимическая функция, как правило, заключается в переходе между этими формами. FAD может быть восстановлен до FADH2, при этом он принимает два атома водорода. Молекула FADH2 является переносчиком энергии и восстановленный кофермент может быть использован как субстрат в реакции окислительного фосфорилирования в митохондрии . Молекула FADH2 окисляется в FAD, при этом выделяется энергия, эквивалентная (запасаемая в форме) двум молям ATФ.
Источник
Кофакторы ферментов: ионы металлов и коферменты. Коферментные функции витаминов, (на примере трансаминаз и дегидрогеназ, витаминов В6 , РР, В2)
Кофакторы ферментов: ионы металлов и коферменты.
Активность ряда ферментов (простые белки) в норме зависит только от их структуры, тогда как для других, названных холоферментами (сложные белки), требуются кофакторы — вещества небелковой природы, в роли которых могут быть сложные органические соединения (коферменты) и ионы металлов.
Кофактор может образовывать с апоферментом прочные ковалентные связи. В этом случае кофермент называют простетической группой фермента. Примерами могут служить ФАД, ФМН, биотин, ковалентно связанный с остатком лизина в активном центре, Zn 2+ , который содержится в активном центре карбоксипептидазы. В том случае, если кофермент связывается с апоферментом нековалентными связями только на время химической реакции (НАД + и НАДФ + ), он может рассматриваться в качестве второго субстрата данного фермента Один и тот же кофермент может участвовать в разных биохимических реакциях, комплементарно связываясь с разными апоферментами. Собственной каталитической активностью коферменты не обладают.
Апофермент формирует активный центр, отвечает за специфичность действия фермента, фиксирует и ориентирует субстрат в активном центре и создает условия для преобразования субстрата в продукты реакции. Ионы металла выполняют две главные функции.
I). Стабилизируют нативную конформацию фермента, структуру его активного центра и субстрата. 2). Участвуют в ферментативном катализе.
1). Металлоферменты, лишенные ионов металла, либо сохраняют способность к химическому катализу, утрачивая стабильность, либо полностью теряют активность. Например, щелочная фосфатаза — металлофермент, в активном центре которого находится Zn 2+ , лишенная ионов цинка щелочная фосфатаза, теряет ферментативную активность, но восстанавливает ее после добавления металла. В некоторых металлоферментах ион металла (Mg 2+ , Mn 2+ , Zn 2+ , Co 2+ , Мо 2+ ) участвует в образовании связи между молекулой субстрата и активным центром кофермента. в отсутствие иона эти ферменты не обладают активностью. Ряд ферментов в качестве субстрата используют комплекс превращаемого вещества с ионом. Для большинства киназ одним из субстратов служит не молекула АТФ, а комплекс Mg 2+ -ATФ.
2). Ферментативный электрофильный катализ. Ионы металла непосредственно участвуют в катализе и локализованы в активном центре фермента.В активном центре ферментов могут содержатся Zn 2+ , Mn 2+ , Fe 2+ , Си 2+ . Пример элек-трофильного катализа — действие карбоангидразы, содержащей ион цинка в активном центре.
B6 Коферментные функции выполняют два фосфорилированных производных пиридоксина: пиридоксальфосфат и пиридоксаминофосфат. Распад коферментов идет путем дефосфорилирования и окисления с образованием 4-пиридоксиловой кислоты. которая выводится из организма.
Коферментные формы витамина В6 включены в реакции, катализируемые почти всеми классами ферментов. Наиболее значительная группа пиридоксалевых ферментов — аминотрансферазы. Пиридоксальзависимые (пиридоксалевые ферменты) ферменты катализируют взаимопревращения и распад аминокислот (регулируют аминокислотный состав крови при разном аминокислотном составе пиши), участвуют в специфических реакциях метаболизма отдельных аминокислот (серина, треонина, триптофана). Участвуют в обмене липидов, синтезе сфинголипидов. В качестве кофактора ферментов участвуют в начальных стадиях синтеза гема. Влияют на обмен жирных кислот.
PP — предшественник коферментов -никотинамидадениндинуклеотида (НАД + ) и никотинамидадениндинуклеотид-фосфата (НАДФ ), входящих в состав дегидрогеназ и редуктаз.
НАД + и НАДФ + приобретают коферментные функции после присоединения к никотинамиду радикала, включающего остаток рибозы, пирофосфат и нуклеотид — аденин. Витамин РР такими функциями не обладает.
1. НАД + — кофермент дегидрогеназ, участвующих в реакциях окисления глюкозы, жирных кислот, глицерола, аминокислот после их дезаминирования; является коферментом дегидрогеназ цикла Кребса (кроме сукцинатдегидрогеназы). В этих реакциях кофермент выполняет функцию промежуточного акцептора электронов и протонов.
2. НАДН и НАДФН — коферменты реакций (НАДН-оксидазной и НАДФН-оксидазной), способствующих возникновению активных форм кислорода в фагоцитах.
B2 Кофермент ФМН и ФАД
1. ФМН и ФАД — коферменты оксидаз, переносящих электроны с окисляемого субстрата на кислород. Это ферменты распада аминокислот (оксидазы D- и L-аминокислот), нуклеотидов (ксантиноксидаза), биогенных аминов (моно- и диа-минооксидазы).
2. ФАД — кофермент пируват- и альфа-кетоглутаратдегидрогеназных комплексов. Совместно с тиаминпирофосфатом и другими коферментами катализируют окислительное декарбоксилирование кетокислот.
Источник
16. Кофакторы ферментов: ионы металлов их роль в ферментативном катализе. Коферменты как производные витаминов. Коферментные функции витаминов в6, рр, в2 на примере трансаминаз и дегидрогеназ.
Большинство ферментов для проявления ферментативной активности нуждается в низкомолекулярных органических соединениях небелковой природы (коферментах) и/или в ионах металлов (кофакторах).
Термин. «кофермент» был введён в начале XX века и обозначал часть некоторых ферментов, которая легко отделялась от белковой молекулы фермента и удалялась через полупроницаемую мембрану при диализе. Несколько позже было выяснено, что большинство ферментов состоит из термолабильной белковой части и термостабильного небелкового фактора — кофермента. Белковая часть получила название «апофермент», который в отсутствие кофермента не обладает каталитической активностью. Кофермент с белковой молекулой (апоферментом) формируют молекулу холофермента, обладающую каталитической активностью.
Более 25% всех ферментов для проявления полной каталитической активности нуждается в ионах металлов. Рассмотрим роль кофакторов в ферментативном катализе.
Роль металлов в ферментативном катализе
Не менее важную роль отводят ионам металлов в осуществлении ферментативного катализа.
Участие в электрофильном катализе
Наиболее часто эту функцию выполняют ионы металлов с переменной валентностью, имеющие свободную d-орбиталь и выступающие в качестве электрофилов. Это, в первую очередь, такие металлы, как Zn 2+ , Fe 2+ , Mn 2+ , Cu 2+ . Ионы щёлочно-земельных металлов, такие как Na + и К+ , не обладают этим свойством. В качестве примера можно рассмотреть функционирование фермента карбоангидразы. Карбоангидраза — цинксодержащий фермент, катализирующий реакцию образования угольной кислоты:
Ион Zn 2+ в результате электрофильной атаки участвует в образовании Н + и ОН — ионов из молекулы воды:
Протон и гидроксйльная группа последовательно присоединяются к диоксиду углерода с образованием угольной кислоты.
В ходе электрофильного катализа ионы металлов часто участвуют в стабилизации промежуточных соединений.
Участие в окислительно-восстановительных реакциях
Ионы металлов с переменной валентностью могут также участвовать в переносе электронов. Например, в цитохромах (гемсодержащих белках) ион железа способен присоединять и отдавать один электрон:
Благодаря этому свойству цитохромы участвуют в окислительно-восстановительных реакциях.
Другой пример участия ионов металлов в окислительно-восстановительных реакциях — работа фермента дофамингидроксилазы, катализирующего реакцию образования норадреналина при участии витамина С
За окислительно-восстановительные свойства у дофамингидроксилазы отвечает ион меди
Фермент, содержащий ион Сu 2+ , не вступает в реакцию с молекулой кислорода. При восстановлении Си 2+ до Си + с помощью аскорбиновой кислоты образуется ион меди, способный взаимодействовать с кислородом с образованием перекисного соединения. Далее гидроксильная группа переносится на молекулу дофамина с образованием норадреналина.
Как уже было сказано, для проявления каталитической активности большинству ферментов необходимо наличие кофермента. Исключение составляют гидролитические ферменты (например, протеазы, липазы, рибонуклеаза), выполняющие свою функцию в отсутствие кофермента.
Кофермент, локализуясь в каталитическом участке активного центра, принимает непосредственное участие в химической реакции, выступая в качестве акцептора и донора химических группировок, атомов, электронов. Кофермент может быть связан с белковой частью молекулы ковалентными и нековалентными связями. В первом случае он называется простетической группой (например, FAD, FMN, биотин, липоевая кислота). Вместе с тем известны примеры, когда кофермент присоединяется к ферменту нековалентными связями настолько прочно, что не диссоциирует от белковой молекулы, например тиаминдифосфат.
Во втором случае кофермент взаимодействует с ферментом только на время химической реакции и может рассматриваться в качестве второго субстрата. Примеры — NAD + , NADP + .
Апофермент обеспечивает специфичность действия и отвечает за выбор типа химического превращения субстрата. Один и тот же кофермент, взаимодействуя с различными апоферментами, может участвовать в разных химических превращениях субстрата. Например, пиридоксальфосфат в зависимости от того, с каким апоферментом взаимодействует, участвует в реакциях трансаминирования или декарбоксилирования аминокислот.
Химическая природа коферментов, их функции в ферментативных реакциях чрезвычайно разнообразны. Традиционно к коферментам относят производные витаминов, хотя помимо них есть значительный класс небелковых соединений, принимающих участие в проявлении каталитической функции ферментов.
К коферментам относят следующие соединения:
-гемы, входящие в состав цитохромов, каталазы, пероксидазы, гуанилатциклазы, NO-синтазы и являющиеся простетической группой ферментов;
-нуклеотиды — доноры и акцепторы остатка фосфорной кислоты;
-убихинон, или кофермент Q, участвующий в переносе электронов и протонов в ЦПЭ;
-фосфоаденозилфосфосульфат, участвующий в переносе сульфата;
-S-аденозилметионин (SAM) — донор метильной группы;
-глутатион, участвующий в окислительно-восстановительных реакциях.
Строение и функции этих коферментов подробно рассмотрены в соответствующих разделах учебника.
Водораствор витамины являются энзимовитаминами, то есть выполняют коферментные функции в составе ферментов. Проявления и механизмы гиповитаминозов по различным энзимовитаминам взаимосвязаны и перекрываются, хотя для большинства из них описаны и специфические авитаминозы. Витамин В2, рибофлавин. входит в состав двух коферментов ФМН и ФАД, являющихся компонентами таких ферментов как сукцинатдегидрогеназа, дегидрогеназы жирных кислот, оксидаз аминокислот, МАО, цитохромредуктазы.Витамин В5, РР входит в состав коферментов НАД и НАДФ,которые являются коферментами более ста дегидрогеназ, участвующих в тканевом дыхании, окислении молочной, яблочной, кетоглутаровой, изолимонной кислот, фосфоглицеринового альдегида, жирных кислот и т.п.Витамин В6, пиридоксин Этот витамин в виде коферментов ПАЛФ (пиридоксальфосфата) и ПАМФ(пиридоксаминфосфата) входит в состав ферментов переаминирования, дезаминирования и декарбоксилирования аминокислот. В реакциях с участием пиридоксина, осуществляется всасывание и транспорт аминокислот, балансируется аминокислотный состав организма.Витамин Н, биотин служит коферментом карбоксилаз, таких как пируваткарбоксилаза, ацетил-КоА-карбоксилаза, пропионил-КоА-карбоксилаза. Биотин связывает молекулу углекислого газа и включает его в органическое вещество. Как кофермент витамин Н участвует т в синтезе жирных кислот, стеринов, пуриновых оснований, мочевины, превращении пиовиноградной кислоты в щавелевоуксусную кислоту.Витамин В3, пантотеновая кислота входит в состав кофермента ацетилирования (КоА), который активирует ацетат и ацильные группы, необходимые для синтеза жирных кислот, стеролов, ацетилхолина. Пантотеновая кислота участвует в биосинтезе жирных кислот
Источник