Работа 77. Качественные реакции на витамины
Реактивы. Хлороформ; серная кислота, конц.; сульфаниловая кислота, 1%-ный раствор; нитрит натрия, 5%-ный раствор, свежеприготовленный; карбонат натрия, 10%-ный раствор; азотная кислота, конц.; диэтилдитиокарбамат натрия, 2%-ный спиртовой раствор; гидроксид натрия, 4%-ный спиртовой раствор; гидросульфит натрия, порошок; хлорид железа (III), кристаллический; тиомочевина, кристаллическая.
Оборудование. Штатив с пробирками; скальпель; весы аптечные с разновесами; беззольные фильтры; флуороскоп.
2. Токоферол, 0,1%-ный спиртовой раствор.
3. Витамин К, насыщенный раствор в 70%-ном этаноле.
4. Тиамин, порошок.
5. Рибофлавин, 0,002%-ный раствор.
6. Рибофлавинмононуклеотид, 0,1%-ный раствор в ампулах, из которого готовят 0,002%-ный раствор.
7. Флавинат, лекарственный препарат в ампулах, содержащий ФАД, 0,002%-ный раствор.
9. Витамин В12, раствор в ампулах.
а. Проба Друммонда на ретинол (витамин А). Метод основан на способности концентрированной серной кислоты отнимать воду от ретинола с образованием окрашенных продуктов.
Ход определения. В пробирку вносят 2 капли рыбьего жира, 5 капель хлороформа и 1-2 капли концентрированной серной кислоты. Появляется голубое окрашивание, переходящее в буро-красное.
б. Обнаружение кальциферола (витамин Д). Метод основан на взаимодействии кальциферола с гидрохлоридом анилина с образованием окрашенных продуктов.
Ход определения. В сухую пробирку помещают 10 капель анилинового реактива и прибавляют 5 капель рыбьего жира. Содержимое пробирки осторожно при постоянном перемешивании нагревают до кипения и кипятят в течение 30 с. В присутствии витамина Д желтая эмульсия приобретает вначале грязно-зеленое, а затем буро-красное или красное окрашивание.
в. Качественная реакция на токоферол (витамин Е). Метод основан на образовании соединений хиноидной структуры, окрашивающихся в красный цвет, при действии сильных окислителей (концентрированной азотной кислоты) на токоферол.
Ход определения. В сухую пробирку вносят 5 капель спиртового раствора токоферола и добавляют 10 капель концентрированной азотной кислоты. Встряхивают. Наблюдают за развитием красного окрашивания.
г. Качественная реакция на нафтохинон (витамин К). Метод основан на взаимодействии диэтилдитиокарбамата с витамином К в щелочной среде с образованием комплекса голубого цвета.
Ход определения. В пробирку вносят 4 капли спиртового раствора диэтилдитиокарбамата натрия и 4 капли раствора гидроксида натрия. Встряхивают и наблюдают за развитием окраски.
д. Обнаружение тиамина (витамин В1). Метод основан на способности тиамина образовывать с диазофенилсульфоновой кислотой комплекс оранжево-красного цвета в щелочной среде.
Ход определения. В пробирку вносят 5 капель раствора сульфаниловой кислоты и прибавляют 5 капель раствора нитрита натрия. К полученному диазореактиву добавляют на кончике скальпеля порошок тиамина и 5 капель раствора карбоната натрия. Встряхивают. Появляется оранжево-красное окрашивание.
е. Обнаружение рибофлавина (витамин В2 и флавиновых коферментов. Метод основан на способности окисленных форм рибофлавина и флавиновых коферментов (ФМН и ФАД) давать в ультрафиолетовом свете желто-зеленую флуоресценцию, интенсивность которой зависит от их концентрации. Восстановленные формы флавинов не флуоресцируют.
Ход определения. В одну пробирку вносят 10 капель раствора рибофлавина, в другую – рибофлавинмононуклеотида, в третью – флавината, приливают в каждую из них по 5 мл воды и перемешивают встряхиванием. Ставят пробирки в штатив флуороскопа и сравнивают интенсивность флуоресценции трех проб.
Прибавляют в каждую пробирку на кончике скальпеля порошок гидросульфита натрия (восстановитель) и наблюдают за гашением флуоресценции.
ж. Качественная реакция на рутин (витамин Р). Метод основан на взаимодействии рутина с хлоридом железа (III) с образованием комплексного соединения зеленого цвета.
Ход определения. На аптечных весах берут навеску 100 мг чая, добавляют 15 мл дистиллированной воды и кипятят в течение 3 мин. Дают остыть, отбирают в пробирку 1 мл жидкости и добавляют несколько кристалликов хлорида железа (III). Перемешивают и разводят в 2-3 раза дистиллированной водой. Развивается зеленое окрашивание.
з. Качественная реакция на цианкобаламин. Метод основан на способности кобальта, входящего в состав витамина В12, при высокой температуре взаимодействовать с тиомочевиной с образованием комплекса зеленого цвета.
Ход определения. На беззольный фильтр наносят 2-3 капли 10%-ного раствора тиомочевины, высушивают на газовой горелке, после чего наносят 1-2 капли раствора витамина В12 и снова высушивают. Образуется зеленое кольцо.
Оформление работы. Все результаты качественных реакций на витамины оформить в виде таблицы.
| № опыта | Материал | Исследуемый витамин | Реакция | Наблюдаемая окраска |
Практическое значение работы. Качественные реакции на витамины позволяют обнаружить их наличие в лекарственных препаратах и после экстракции в пищевых продуктах и лекарственных растениях. Принцип, положенный в основу качественных реакций на витамины, используется при разработке количественного определения их в различных природных объектах и лекарствах.
Работа 78. Определение содержания тиамина и рибофлавина
флуориметрическим методом в поливитаминных препаратах
Реактивы. Соляная кислота, 0,1 М раствор; окислительная смесь * ; Н-бутанол; этанол, 96%-ный; тиамин, стандартный раствор концентрации 10 мкг/мл; уксусная кислота, ледяная; перманганат калия, 4%-ный раствор; гидроксид водорода, 3%-ный раствор; гидросульфит натрия, порошок; рибофлавин, стандартный раствор концентрации 0,005 мг/мл.
Оборудование. Штатив с пробирками; пенициллиновые флакончики с полиэтиленовыми пробками; пипетки вместимостью 1 и 5 мл; мерный цилиндр вместимостью 50 мл; ступка с пестиком; флуориметр ЭФ-3 или БИАН.
Материал. Драже поливитаминов.
а. Определение содержания тиамина. Метод основан на способности тиамина окисляться гексацианоферратом (III) калия в щелочной среде в тиохром, который после извлечения его из раствора бутиловым спиртом дает в ультрафиолетовом свете сине-голубую флуоресценцию:
 |
Ход определения. Драже поливитаминов разминают в ступке, добавляя 30 мл раствора соляной кислоты, и тщательно перемешивают.
В один флакончик (контроль) вносят 5 мл соляной кислоты, во второй (опыт) – 1 мл водного экстракта драже витаминов и 4 мл дистиллированной воды, в третью (стандарт) – 5 мл раствора тиамина.
Во все флакончики приливают по 1,5 мл окислительной смеси и осторожно встряхивают их до полного перемешивания. Затем добавляют в них по 5 мл бутанола, плотно закрывают пробками и интенсивно встряхивают 5 мин. После расслоения жидкости осторожно прибавляют по 0,5 мл этанола (для просветления бутанола).
Осторожно сливают просветленный бутанольный слой в кювету флуориметра и измеряют интенсивность флуоресценции опытной и контрольной проб со стандартным раствором тиамина.
Расчет проводят по формуле
где х – содержание тиамина в драже, мг;
Еоп – показания флуориметра для опытной пробы;
Ек – показания флуориметра для контрольной пробы;
Ест – показания флуориметра для стандартной пробы;
0,01 – концентрация тиамина в стандартном растворе, мг/мл;
30 – объем экстракта драже, мл;
1 – объем экстракта, взятого на исследование, мл;
5,5 – объем пробы, просветленной этанолом, мл.
б. Определение содержания рибофлавина. Принцип метода см. работу 73, е.
Ход определения. Драже поливитаминов разминают в ступке, добавляя 30 мл раствора соляной кислоты, и тщательно перемешивают.
В одну пробирку вносят 7 мл дистиллированной воды, во вторую (опытную) – 2 мл экстракта драже и 5 мл дистиллированной воды, в третью (стандартная) – 1 мл стандартного раствора рибофлавина и 6 мл воды.
Во все пробирки приливают по 10 капель ледяной уксусной кислоты и по 1,5 мл раствора перманганата калия (для окисления посторонних флуоресцирующих веществ).
Содержимое пробирок встряхивают и добавляют по каплям (примерно 5 капель) гидроксид водорода при постоянном помешивании стеклянной палочкой до полного просветления жидкости. Растворы отстаивают 5 мин, до прекращения выделения пузырьков газа. Сливают жидкость в кюветы флуориметра и измеряют интенсивность флуоресценции всех проб.
Расчет проводят по формуле
где х – содержание рибофлавина в драже, мг;
Еоп – показания флуориметра для опытной пробы;
Ек – показания флуориметра для контрольной пробы;
Ест – показания флуориметра для стандартной пробы;
30 – объем экстракта драже, мл;
2 – объем экстракта драже, взятого на исследование, мл;
0,005 – концентрация рибофлавина в стандартном растворе, мг/мл;
7 – объем флуориметрируемых проб, мл.
Оформление работы. Рассчитать содержание исследуемых витаминов в драже и сделать вывод о возможности практического использования флуориметрического метода.
Практическое значение работы. Флуориметрические методы определения тиамина и рибофлавина применяются для определения этих витаминов в пищевых продуктах, лекарственных растениях и готовых лекарственных препаратах, а также для изучения обеспеченности ими организма. Обеспеченность этими витаминами может быть определена по их уровню в крови и по экскреции с мочой. Низкое содержание витаминов в организме наблюдается при гиповитаминозах, болезнях печени, сердечно-сосудистых заболеваниях, заболеваниях желудочно-кишечного тракта и других патологических состояниях.
Работа 79. Количественное определение аскорбиновой кислоты
в лекарственных растениях
Реактивы. Соляная кислота, 2%-ный раствор; 2,6-дихлорфенолиндофенол, 0,001 М раствор.
Оборудование. Пипетки вместимостью 5 и 10 мл; мерная колба вместимостью 100 мл; воронка; вата; аптечные весы с разновесами; микробюретка; скальпель; ступки с пестиком; стаканчики для титрования.
1. Лекарственное сырье (цветы бузины и тысячелистника, лист крапивы и сенны, кора крушины, витаминный чай, плоды шиповника).
2. Таблетки из плодов аронии черноплодной.
Метод основан на способности аскорбиновой кислоты к окислительно-восстановительным превращениям. В ходе окисления аскорбиновой кислоты происходит восстановление 2,6-дихлорфенолиндофенола с образованием его лейкоформы. На полное окисление аскорбиновой кислоты в растворе указывает появление розового окрашивания при небольшом избытке 2,6-дихлорфенолиндофенола в кислой среде:
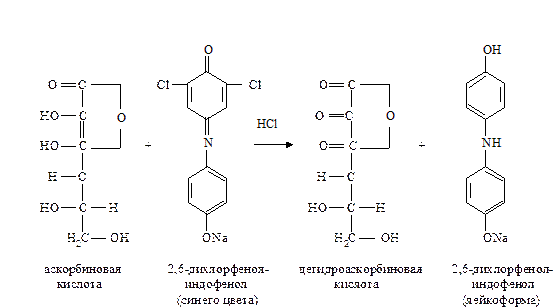 |
Ход определения. На аптечных весах берут навески лекарственного сырья: цветы бузины, лист крапивы, цветы тысячелистника, кора крушины, лист сенны, витаминный чай и плоды аронии черноплодной (или таблетки) по 0,5 г; шиповник, очищенный от семян, — 0,2 г. Исследуемый материал переносят в ступку, измельчают скальпелем и растирают в ступке с 5 мл раствора соляной кислоты.
Вытяжку фильтруют через тонкий слой ваты в мерную колбу, вместимостью 100 мл. Извлечение витамина С из той же навески повторяют три раза с таким же объемом соляной кислоты, фильтруя каждый раз полученную вытяжку в ту же мерную колбу. Содержимое колбочки доводят до метки дистиллированной водой, перемешивают.
Для определения отбирают 10 мл вытяжки в стаканчик и титруют содержимое раствором 2,6-дихлорфенолиндофенола, налитого в микробюретку, до появления розового окрашивания, не исчезающего в течение 30 с.
Расчет проводят по формуле:
где х – содержание аскорбиновой кислоты, мг/кг;
0,088 – масса аскорбиновой кислоты, соответствующая 1 мл 0,001 М раствора 2,6-дихлорфенолиндофенола, мг;
100 – разведение взятой пробы;
1000 – коэффициент пересчета на 1 кг сырья;
10 – объем жидкости, взятый для титрования, мл;
V – объем 2,6-дихлорфенолиндофенола, пошедший на титрование, мл;
b – навеска исследуемого материала, г.
Оформление работы. Полученные данные оформить в виде таблицы и сделать вывод о значении исследованного растительного материала как источника аскорбиновой кислоты. Указать в выводе о целесообразности применения растительного сырья с целью профилактики С-витаминной недостаточности.
| Материал | Навеска, г | Объем 2,6-дихлорфенолиндофенола, пошедшего на титрование, мл | Содержание аскорбиновой кислоты, мг/кг |
Практическое значение работы. Определение содержания аскорбиновой кислоты в пищевых продуктах и лекарственных растениях необходимо для составления правильного рациона, удовлетворяющего потребность организма в этом витамине. Богаты витамином С плоды шиповника, черной смородины, цитрусовых и т.д. Аскорбиновая кислота применяется для профилактики гиповитаминоза и простудных заболеваний, для лечения воспалительных процессов, атеросклероза. Она способствует усилению регенеративных процессов. Определение аскорбиновой кислоты в крови и моче используется для выявления состояния гиповитаминоза. Аскорбиновая кислота участвует в окислительно-восстановительных процессах при синтезе стероидных гормонов, обмене ароматических аминокислот, образовании соединительной ткани.
Источник
Лабораторная работа № 4 Качественные реакции на витамины
— познакомиться с классификацией и биологическим значением витаминов;
— научиться понимать состояния организма человека при разной обеспеченности его витаминами;
— в процессе эксперимента обнаружить присутствие витаминов в продуктах питания;
— провести реакции обнаружения водорастворимых витаминов в различных веществах и биологических жидкостях при помощи качественных реакций, основанных на цветных реакциях, характерных для той или иной группировки, входящей в витамин;
— Определить количественный состав витаминов в различных веществах и биологических жидкостях при помощи качественных реакций, основанных на цветных реакциях, характерных для той или иной группировки, входящей в витамин;
— провести реакции обнаружения жирорастворимых витаминов в различных веществах и биологических жидкостях при помощи качественных реакций, основанных на цветных реакциях, характерных для той или иной группировки, входящей в витамин.
Витамины – группа низкомолекулярных органических веществ различной химической природы, имеющих разнообразный состав, строение и физико-химические свойства. Они регулируют процессы жизнедеятельности, оказывая свое действие в ничтожно малых количествах (мг или мкг). Почти все витамины не синтезируются в организме человека и относятся к незаменимым пищевым факторам.
Необходимость витаминов для организма человека и животных впервые установлена русским врачом Н.И.Луниным в 1830 г. Первое вещество из этой группы было выделено в 1831 г. польским биохимиком К.Функом. Оно оказалось смесью различных веществ, содержащей азот. Функ назвал эту смесь витамином, т.е. амином, необходимым для жизни.
Витамины отличаются от всех других органических веществ пищи двумя признаками: они не входят в состав структуры органов и тканей и не используются организмом в качестве источника энергии. Отсутствие или недостаточное содержание витаминов в пище приводит к развитию тяжелых заболеваний. Нарушение обмена веществ при авитаминозах и гиповита-минозах является следствием снижения активности ферментов, поскольку многие витамины входят в состав простетических групп энзимов. Для обнаружения витаминов в пищевых продуктах, тканях и жидкостях организма и для определения их количества используются качественные реакции, основанные на образовании характерных окрашенных продуктов реакции витамина с каким-либо химическим реагентом.
В настоящее время выделено более 30 веществ, относящихся к витаминам. Обозначают витамины заглавными буквами латинского алфавита, кроме того, они имеют название, соответствующее их химическому строению. Например, витамин С – аскорбиновая кислота, витамин А – ретинол.
Обеспеченность витаминами и, прежде всего, С, В1, В2, Р является важным источником информации о состоянии метаболизма спортсменов. При отсутствии витаминов в пище развиваются тяжелые заболевания – авитаминозы, а при недостаточном содержании витаминов – гиповитаминозы (рахит, цинга, бери-бери, пеллагра, анемия и др.). Причины развития последних могут быть обусловлены рядом факторов: недостаточным поступлением витаминов с пищей, величиной и интенсивностью физических нагрузок, наличием заболеваний и т. д. Недостаточная обеспеченность организма витаминами может существенным образом отразиться на физической работоспособности, например, при недостатке тиамина накапливаются пировиноградная кислота, а-кетокислоты и др.
Введение отдельных лекарственных веществ может отрицательно сказаться на синтезе витаминов микрофлорой кишечника. Суточная потребность в витаминах возрастает при различных заболеваниях, беременности, лактации и при нарушении всасывания жирорастворимых витаминов в случае недостаточного поступления желчи в кишечник при заболевании печени.
По способности растворяться витамины делят на две группы: водорастворимые (С, В1, В2, В3, В6, В12, Вс, Р, РР и др.) и жирорастворимые (А, Е, К, Д). Такая классификация имеет физиолого-биохимическое значение, так как витамины, растворимые в жирах, могут накапливаться в организме человека и их кратковременный дефицит не имеет неблагоприятных последствий.
При избыточном приеме с пищей жиров концентрация жирорастворимых витаминов в липидах организма может существенно превышать норму, что в отдельных случаях приводит к неблагоприятным изменениям обмена или функциональным нарушениям.
Водорастворимые витамины в организме не накапливаются, и при их недостатке, либо отсутствии быстро возникают специфические нарушения обмена веществ.
Структурные аналоги витаминов, близкие к ним по строению, называют антивитаминами. Эти вещества встречаются в природе или могут быть синтезированы. Антивитамины способны соединяться с белковой частью ферментов витаминов и вызывать изменения активности ферментов и обменных процессов.
Все витамины характеризуются следующими общими свойствами:
— не синтезируются в организме человека и должны поступать с пищей. Некоторые из них (В6, В12, пантотеновая, фолиевая кислоты и др.) синтезируются микрофлорой кишечника, другие (А, Д, РР) образуются при определенных условиях;
— не являются пластическим и энергетическим материалом;
— оказывают влияние на биохимические процессы в организме. Ряд витаминов входит в состав коферментов. Обеспеченность организма человека витаминами описывается терминами:
— физиологическая норма – витамина в организм поступает достаточно, человек здоров;
— гиповитаминоз – витамина в организм поступает мало, качество жизни снижается;
— гипервитаминоз – поступление какого-либо витамина в организм превышает физиологическую норму, качество жизни снижается;
— авитаминоз – какой-то витамин полностью отсутствует в организме, что вызывает специфическое заболевание.
Из перечисленных состояний чаще всего встречаются гиповитаминозы. Причинами их могут быть:
— использование в пищу продуктов, содержащих мало витаминов;
— нарушение технологии приготовления пищи (длительная термическая обработка, многократное разогревание);
— нарушение всасывания витаминов из кишечника из-за болезней органов пищеварения;
— повышенная потребность организма в витаминах (активные занятия спортом, вредные привычки).
Для обнаружения витаминов в различных веществах или в биологических жидкостях и определения их количества существуют качественные реакции, основанные на цветных реакциях, характерных для той или иной другой группы витаминов.
1. Что такое витамины? Какова их роль в обмене веществ?
2. Как классифицируются витамины? Перечислить витамины, относящиеся к каждой группе.
3. Дать определение и привести примеры гипо -, гипер- и авитаминозов для витаминов С, А, Е, Д.
4. Как изменяется потребность в витаминах при интенсивной мышечной деятельности?
5. Что является причиной проявления гиповитаминоза в весенний период?
6. Почему избыточное потребление жирорастворимых витаминов приводит к развитию гипервитаминозов, водорастворимых – нет?
Источник