Инсулин чем опасен для здоровья

Причина, по которой инсулин так важен для организма – это то, что он действует как ключ, «открывающий двери» для глюкозы внутрь клетки. Как только человек видит еду или чувствует ее запах, его β-клетки получают сигналы к увеличению продукции инсулина. А после того, как еда попала в желудок и кишечник, другие специальные гормоны посылают еще больше сигналов бета-клеткам, чтобы они увеличили продукцию инсулина.
Бета-клетки содержат встроенный «глюкометр», который регистрирует, когда уровень глюкозы крови повышается, и отвечают, посылая правильное количество инсулина в кровь. Когда люди без сахарного диабета едят пищу, концентрация инсулина в крови резко возрастает, это необходимо для переноса глюкозы, полученной из еды, внутрь клеток. У таких людей глюкоза крови обычно не поднимается более чем на 1-2 ммоль/л после еды.

Это может показаться нелогичным, что некоторым клеткам не нужен инсулин для переноса глюкозы. Однако, в ситуациях, когда в организме низкий уровень глюкозы, продукция инсулина останавливается, тем самым сохраняя глюкозу для наиболее важных органов. Если у вас есть сахарный диабет и ваш уровень глюкозы крови высокий, инсулиннезависимые клетки будут поглощать большое количество глюкозы, и в результате это приведет к повреждению клеток и, следовательно, функционированию органа в целом.
Организму требуется небольшое количество инсулина даже между приемами пищи и в течение ночи, чтобы приспособить глюкозу, поступающую из печени. Это и называется «базальной» секрецией инсулина. У людей без сахарного диабета количество этого инсулина составляет 30-50% от количества общего суточного инсулина. Также есть «стимулированная» секреция инсулина, который вырабатывается на прием пищи.
Большое количество углеводов, поступающих к нам с едой, хранится в печени в виде гликогена (это углевод, способный быстро распадаться с образованием глюкозы).
Если человек ест больше, чем ему необходимо, то избыток углеводов трансформируется в жиры, которые хранятся в жировой ткани. Организм человека имеет почти неограниченные возможности для накопления жира.
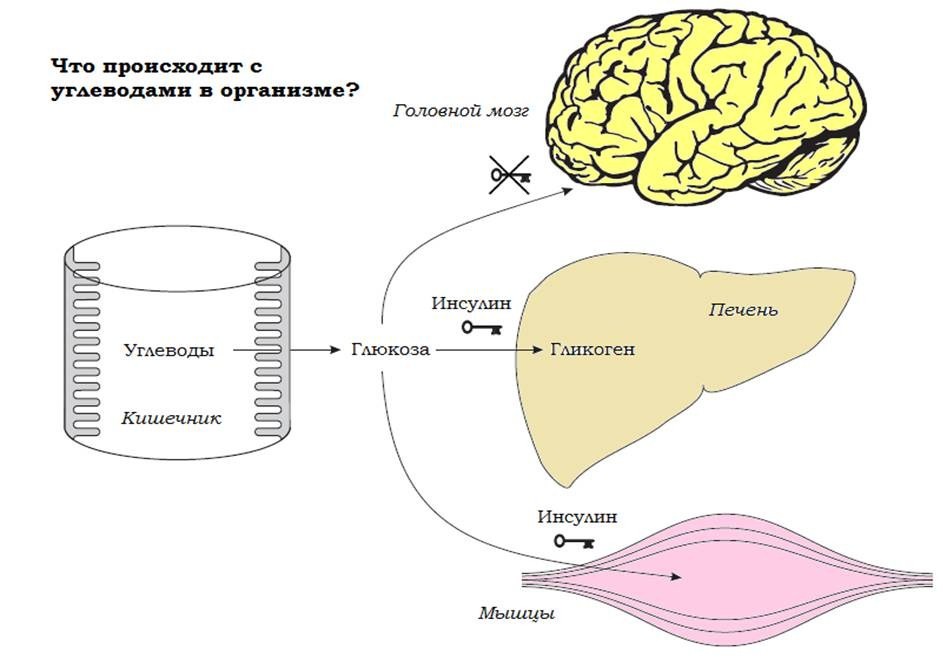
Напротив, белки (аминокислоты) могут быть использованы различными тканями организма, но у них нет никакого определенного места хранения. Печень способна синтезировать глюкозу не только из гликогена, но также и из аминокислот, например, если вы не ели в течение длительного времени. Но при этом происходит разрушение тканей, так как в организме нет определенного депо аминокислот (Рис.1).
Рис.1. Углеводы в организме (R. Hanas “Type 1 Diabetes in children, adolescents and young adults”, 3 d edition, Class publishing, London, 2007).
Поджелудочная железа
Поджелудочная железа – это непарный орган размером с ладонь, расположенный в брюшной полости, близко к желудку. Она выполняет две основные функции: производит ферменты, которые помогают переваривать пищу, и производит инсулин, который помогает контролировать уровень глюкозы крови. Пищеварительные ферменты из поджелудочной железы попадают в кишечник через проток поджелудочной железы. Он впадает в двенадцатиперстную кишку вместе с желчным протоком, который выводит желчь из печени и желчного пузыря. В поджелудочной железе находится около одного миллиона островков Лангерганса. Инсулин производится бета-клетками островков и высвобождается непосредственно в мелкие кровеносные сосуды, проходящие через поджелудочную железу.
Клеточный метаболизм
Здоровая клетка
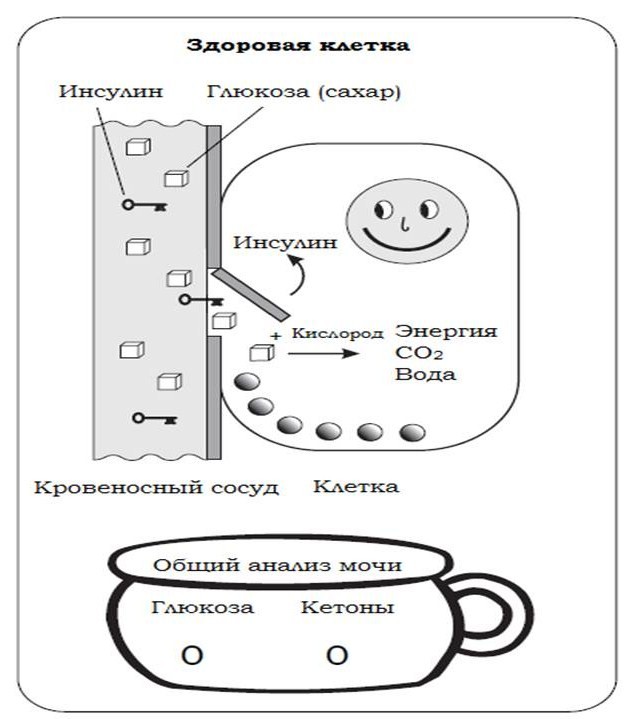
Сахар из еды всасывается в кишечнике и поступает в кровь в форме глюкозы (декстрозы) и фруктозы. Глюкоза должна зайти в клетки для того чтобы она могла быть использована для продукции энергии или других метаболических процессов. Гормон инсулин необходим для того, чтобы «открыть дверь», то есть сделать возможным транспорт глюкозы внутрь клетки через клеточную стенку. После того, как глюкоза попадает внутрь клетки, она превращается с помощью кислорода в углекислый газ, воду и энергию. Углекислый газ затем поступает в легкие, где происходит обмен его на кислород (Рис.2).
Рис. 2. Поддержание уровня глюкозы крови в норме (R. Hanas “Type 1 Diabetes in children, adolescents and young adults”, 3 d edition, Class publishing, London, 2007).
Энергия жизненно необходима клеткам для того, чтобы они функционировали должным образом. Кроме того, глюкоза в форме гликогена хранится в печени и мышцах для дальнейшего использования.
Головной мозг, однако, не способен хранить глюкозу в виде гликогена. Следовательно, он находится в постоянной зависимости от уровня глюкозы крови.
Голодание
Когда человек голодает, в крови снижается уровень глюкозы. В этом случае дверь, открытая с помощью инсулина, не окажет никакой пользы. У людей без сахарного диабета продукция инсулина останавливается почти полностью, когда уровень глюкозы крови снижается. Альфа-клетки поджелудочной железы распознают низкий уровень глюкозы крови и секретируют в кровоток гормон глюкагон. Глюкагон действует как сигнал для клеток печени, чтобы они высвободили глюкозу из своего резерва гликогена. Есть и другие гормоны, которые также могут синтезироваться, когда человек голодает (такие как адреналин, кортизол и гормон роста).

Все клетки нашего организма (за исключением головного мозга) могут использовать жирные кислоты в качестве источника энергии. Однако, только мышцы, сердце, почки и головной мозг могут использовать кетоны как источник энергии.
Во время длительного голодания кетоны могут обеспечивать до 2/3 потребности мозга в энергии. У детей кетоны образуются быстрее и достигают большей концентрации, чем у взрослых.
Несмотря на то, что клетки извлекают определенную энергию из кетонов, ее все равно меньше, чем когда они используют глюкозу.
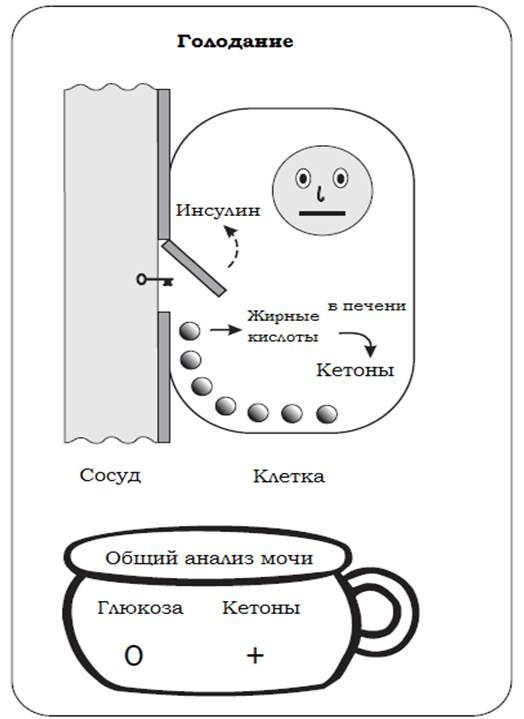
Если организм находится без еды слишком долго, то белки из мышечной ткани начинают распадаться, и превращаться в глюкозу.
Рис. 3. Поддержание уровня глюкозы во время голодания (R. Hanas “Type 1 Diabetes in children, adolescents and young adults”, 3 d edition, Class publishing, London, 2007).
Сахарный диабет 1 типа и абсолютная недостаточность инсулина. Механизм заболевания – предпосылки разъяснения.
Сахарный диабет 1 типа – это заболевание, при котором отсутствует свой инсулин. В результате этого глюкоза не может зайти в клетки. Клетки в этой ситуации действуют так, как будто они находятся в фазе голодания, описанной выше. Ваш организм будет пытаться поднять уровень глюкозы крови до еще более высоких значений, так как он считает, что причиной отсутствия глюкозы внутри клеток является низкий уровень глюкозы крови. Такие гормоны как адреналин и глюкагон посылают сигналы для выброса глюкозы из печени (активируют распад гликогена).
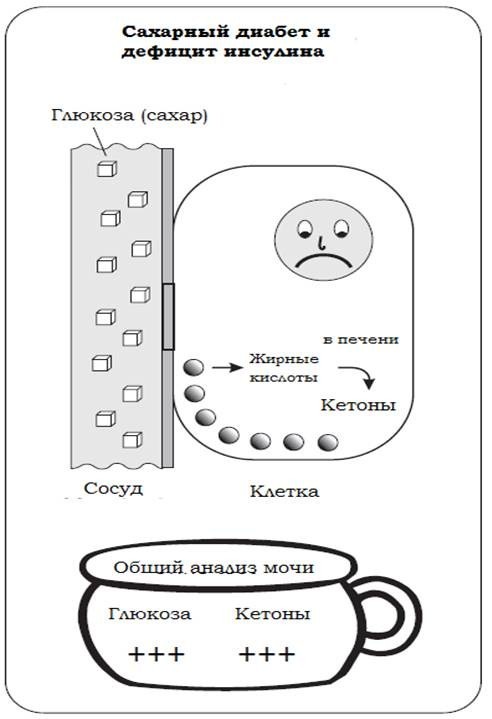
В этой ситуации, однако, голодание происходит в период изобилия, то есть высокой концентрации глюкозы крови. Организму сложно справиться с большой концентрацией глюкозы, и она начинает выходить с мочой. В это время внутри клеток происходит синтез жирных кислот, которые затем трансформируются в кетоны в печени, и они также начинают выделяться с мочой. Когда человеку назначается инсулин, его клетки начинают снова нормально функционировать и порочный круг прекращается (Рис. 4).
Рис. 4. Дефицит инсулина и сахарный диабет 1 типа (R. Hanas “Type 1 Diabetes in children, adolescents and young adults”, 3 d edition, Class publishing, London, 2007).
Источник
Инсулин чем опасен для здоровья
Клиническая классификация фармакогенных гипогликемических расстройств представлена в таблице ниже.
К диагностическим критериям сознательной передозировки инсулина относятся депрессия в анамнезе; гипогликемия, резистентная или минимально реагирующая на вливания концентрированного раствора глюкозы; существенно повышенный плазменный уровень инсулина; низкий или нормальный уровень С-пептида (при повышенном уровне инсулина); положительный анализ на антитела к инсулину (если речь не идет о злоупотреблении человеческим инсулином); эритематозные или дряблые места инъекций и острая кратковременная гепатомегалия (у детей).
Хотя экзогенный гиперинсулинизм часто возникает после случайной передозировки, он возможен также после скрываемой от врача самостоятельной инъекции, тайного введения средства посторонним лицом со злым умыслом или после терапевтического применения лекарства.
Кроме того, многие случаи инсулиновой передозировки бывают умышленно вызваны самим больным, нередко при суицидальных попытках в состоянии депрессии. Серьезные осложнения после передозировки наблюдались в первый год появления инсулина на рынке.
Распространенность вызванной такой передозировкой гипогликемии, вероятно, выше, чем принято считать. Установленные случаи, скорее всего, составляют лишь часть общего числа действительно совершаемых суицидальных попыток.
Некоторые случаи не распознаются из-за отсутствия тяжелой гипогликемии или рассматриваются как случайные гипогликемические приступы у больных с нестабильным диабетом. Из 204 тяжелых гипогликемических эпизодов, зафиксированных в течение года в одном отделении неотложной помощи, 4 относились к умышленным передозировкам инсулина.
Одно агентство за 2 года зарегистрировало 18 случаев самоотравления инсулином, приведших к смерти 4 диабетиков и необратимым поражениям головного мозга у 3 выживших. В другом центре в течение 3 лет отмечено 20 таких самоотравлений, причем 2 пациента умерли. У них в анамнезе было либо злоупотребление алкоголем, либо недоедание. Минск и Quaade сообщают о смертности в 25 % случаев при 16 зарегистрированных суицидальных попытках с использованием инсулина.
На уровень глюкозы в плазме влияют различные лекарства, способные индуцировать как гипо-, так и гипергликемию.
а) Гипогликемия и человеческий инсулин. В Великобритании некоторые пациенты, переведенные с бычьего инсулина на человеческий, стали чаще испытывать приступы гипогликемии при исчезновении ее ранних симптомов. Известно, что бычий инсулин более иммуногенен, чем свиной или человеческий.
Пациентам, получавшим ранее в день менее 100 ЕД бычьего инсулина, было рекомендовано с переходом на человеческий снизить дозу на 10 % (и даже более), а получавшим более 100 ЕД — на 25 %. В США применение человеческого инсулина сопровождалось по сравнению с другими его типами меньшим числом летальных исходов без увеличения частоты бессимптомной гипогликемии.
б) Терапевтическая доза. Доза инсулина измеряется в единицах фармакопеи США, причем обозначение U-100 соответствует 100 ЕД/мл. Терапию начинают с малых доз обычного (регулярного) инсулина (5—10 ЕД — взрослым, 2—4 ЕД — детям).
Все инсулины вводят подкожно при рутинном течении диабета, но обычный (регулярный) инсулин можно применять и внутривенно при тяжелом диабетическом кетоацидозе и коме.
в) Токсикокинетика инсулина:
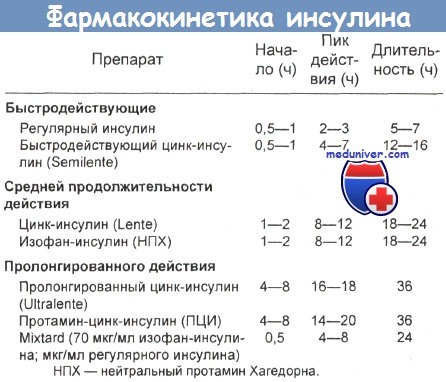
— Распределение. Инсулин распределяется по всем внеклеточным жидкостям. Его коммерческие препараты различаются по времени начала, пика и продолжительности действия после подкожного введения.
— Выведение. До 50 % инсулина метаболизируется в печени. Затем он подвергается восстановительному расщеплению двух межцепочечных дисульфидных мостиков с участием глутатиона и фермента глутатион-инсулин-трансгидрогеназы.
Период полужизни введенного внутривенно регулярного инсулина составляет 20 мин; при подкожном или внутримышечном введении он удлиняется до 2 ч. Изофан-инсулин в 3 раза снижает свою пиковую концентрацию за 9 ч.
Инсулин реабсорбируется в проксимальных канальцах (98 %); 60 % его возвращается в венозную кровь, а 50—60 % метаболизируется. В неизмененном виде выводится менее 2 %.
г) Взаимодействие лекарственных средств. Гипогликемическое действие инсулина, по-видимому, усиливается при голодании, потреблении алкоголя, применении барбитуратов и, возможно, салицилатов и бензодиазепинов. Ослабляется оно адреналином, глюкагоном, тироксином, эстрогенами, гормонами коры надпочечников и соматотропином.
д) Беременность и лактация. Потребность в инсулине может возрастать у беременных; он способен концентрироваться в плаценте. Систематических исследований по изучению его концентраций в грудном молоке не проводилось.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник