Вопрос 9 Витамин с, химическое строение, явления недостаточности, биологическая роль. Участие витамина «с» в синтезе коллагена. Реакция гидроксилирования пролина и лизина
Витамин С – аскорбиновая кислота – антискорбутный.
Основные источники: фрукты и овощи (грецкий орех, грейпфрут, черная смородина, шиповник, капуста, клюква, перец сладкий). Суточная потребность 50-100 мг. Всасывается путем простой диффузии на протяжении ЖКТ, транспортируется кровью частично в свободном, частично в связанном состоянии. В тканях окисляется до дегидроаскорбиновой, дикетогулоновой, щавелевой и др. кислот. Неизмененная аскорбиновая кислота и ее метаболиты выводятся с мочой.
Основная функция – участие в окислительно-восстановительных реакциях, а также в следующих превращениях:
Гидроксилирование триптофана в положении 5 (синтез серотонина).
Гидроксилирование ДОФА (образование норадреналина).
Гидроксилирование стероидов (синтез кортикостероидов).
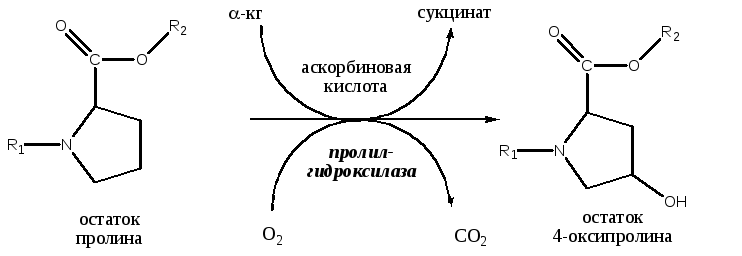
Гидроксилирование пролина и лизина в проколлагене (синтез коллагена).
Образование коферментных форм фолацина.
Кроме того, аскорбиновая кислота участвует в обмене железа: в кишечнике обеспечивает восстановление трехвалентного в двухвалентное – обязательное условие всасывания железа; высвобождает железо из связанной транспортной формы в крови (из комплекса с трансферрином), что ускоряет его поступление в ткани.
Авитаминозом витамина С является цинга. Проявления: рыхлость десен, расшатывание зубов, подкожные точечные кровоизлияния (петехии), анорексия, анемия, замедленное заживление ран, слабость, головная боль, одышка, боль в сердце, отеки, боли в ногах.
Все эти изменения обусловлены нарушением образования коллагена и хондроитинсульфата, ростом сосудистой проницаемости, снижением свертываемости крови. Анемия обусловлена нарушением образования коферментных форм фолацина, снижением синтеза ДНК в кроветворных клетках. Нарушен синтез одонто- и остеобластов.
Вопрос 10 Витамин рр, строение и биологическая роль. Над-зависимые дегидрогеназы.
Витамин РР (никотиновая кислота) синтезируется кишечными бактериями из триптофана. Никотиновая кислота и ее амид играют важную роль в организме, так как никотинамид является коферментом пиридиновых ферментов (НАД и НАДФ), которые участвуют в окислительно-восстановительных реакциях. В процессе биологического окисления НАД и НАДФ играют роль промежуточных переносчиков электронов и протонов между окисляемым субстратом и флавиновыми ферментами. При дефиците витамина РР развивается пеллагра. Для этого заболевания наиболее характерными признаками являются: симптом трёх «Д» (дерматиты, диарея, деменция). Дерматиты чаще всего возникают на тех участках, которые подвержены влиянию прямых солнечных лучей (тыльная поверхность кистей рук, шея, лицо), при этом кожа становится красной, затем коричневой и шершавой. Диарея – сопровождается анорексией, тошнотой, рвотой, болью в области живота. Специфическими для пеллагры являются также стоматиты, гингивиты, поражения языка. Деменция – нарушение нервной деятельности с симптомами головной боли, головокружением, повышенной раздражимостью, депрессией. Суточная потребность в витамине РР 18 мг.
Источник
Краткий обзор некоторых кофакторов, участвующих в синтезе коллагена
Качественные коллагеновые волокна — одна из основных составляющих здоровой кожи. Поэтому большое количество косметологических методов направлено на восстановление ее коллагенового каркаса. Как витамины и микроэлементы могут влиять на синтез коллагена? И почему для достижения стойкого эффекта необходимо учитывать их количественный состав в организме?
Ежегодно создаются новые методики и препараты для улучшения синтеза коллагена с целью профилактики инволюционных процессов в организме и уменьшения выраженности возрастных изменений.
Но за стремлением повлиять на коллагеногенез извне порой забывают о тех веществах, без достаточного количества которых в самом организме синтез коллагена крайне затруднен. Никто не будет отрицать, что продукция этого жизненно важного белка зависит от гормонов, гормоны, в свою очередь, от присутствия металлов, усвоение металлов — от витаминов; и эту цепочку можно продолжать долго, тем более что она замкнутая. Осветить все нюансы в одной статье не представляется возможным, но сделать шаг навстречу пониманию некоторых процессов — в наших силах. Синтез и процессинг (созревание) коллагена включает в себя несколько этапов:
- транскрипция генов, кодирующих коллагены, в которой участвуют десятки магнийи кальцийзависимых белков;
- синтез препроколлагена на рибосоме, поддерживаемый магний- и кальцийзависимыми белками;
- транспорт цепи препроколлагена в эндоплазматический ретикулум посредством сигнального пептида на N-концевом участке аминокислотной цепи;
- удаление сигнального пептида в препроколлагене посредством фермента пептидазы;
- гидроксилирование аминокислотных остатков пролина с участием Fe2+ и аскорбат-аниона в качестве кофакторов;
- гликозилирование моносахаридами аминокислотных остатков лизина в препроколлагене в присутствии ферментов, содержащих ионы марганца;
- сборка тройной спирали проколлагена из 3 аминокислотных цепей препроколлагена;
- внесение необходимых конформационных изменений в проколлаген посредством изомеризации остатков цистеина и пролина;
- упаковка проколлагена в транспортный везикул, перенос во внеклеточный матрикс;
- вне клетки модификация молекулы проколлагена с помощью протеиназ проколлагена, нуждающихся в ионах Zn2+ как кофакторе;
- формирование коллагеновых фибрилл из тропоколлагена посредством лизилоксидазы, кофакторами которой являются ионы Cu+ и тирозил-хинон (рис. 1) [1].
Всем известно об участии магния и кальция в синтезе соединительной ткани и коллагена, но о железе, цинке, меди, витаминах С и D часто забывают. Именно эти кофакторы рассмотрим в статье.
Железо
Железодефицитная анемия в той или иной степени присутствует у 40–60 % женщин детородного возраста по всему миру [2, 26]. И это при том, что железо — один из важнейших микроэлементов, необходимых для нормального функционирования биологических систем организма. Оно требуется для осуществления функции дыхания, кроветворения, участвует в иммунобиологических и окислительно-восстановительных реакциях.
Причины дефицита железа:
- недостаточное поступление в организм железа из-за нарушения режима питания (например, при вегетарианской диете);
- снижение всасываемости железа в кишечнике (рис. 3);
- нарушение регуляции обмена витамина С;
- избыточное поступление в организм фосфатов, оксалатов, кальция, цинка, витамина Е;
- поступление в организм железосвязывающих веществ;
- усиленное расходование железа (в периоды интенсивного роста и беременности);
- потери железа, связанные с травмами, кровопотерями во время операций, обильными менструациями, язвенными болезнями, донорством, занятиями спортом;
- нарушение функции щитовидной железы;
- различные системные и опухолевые заболевания [21].
Учитывая высокую распространенность дефицита железа в популяции, сложно говорить о нормальном синтезе коллагена при таких состояниях.
Цинк — единственный металл, представленный в небелковой части ферментов каждого класса, и никаким другим металлом цинк не может быть заменен. Несмотря на малую концентрацию цинка в крови, стабильные связи с макромолекулами делают его доступным для всех тканей организма, что в дальнейшем позволяет удовлетворять потребности в нем белков и ферментов, выполняющих различные биологические функции [28].
Распространенность дефицита цинка в мире не менее значительная, чем железа и витамина С, и составляет до 60% [29].
Для транспорта эритроцитами кислорода и углекислого газа абсолютно необходим цинк, и большая часть цинка крови содержится именно в эритроцитах в составе цинковых металлоферментов — карбоангидраз. Карбоангидразы катализируют превращения углекислого газа в угольную кислоту (угольная кислота участвует в поддержании pH крови в физиологическом диапазоне (7,25–7,35). В капиллярах легких эти процессы идут в обратном направлении: угольная кислота распадается на углекислый газ и воду, и углекислый газ удаляется наружу [18].
Без нормального дыхания ни одна клетка не способна осуществлять свои функции.
В мире распространенность дефицита меди в организме, приводящего, наряду с железом, к анемии, составляет до 30%. А ведь этот микроэлемент крайне необходим для нормальной физиологии организма.
Если говорить о коже, то медь играет ключевую роль в ангиогенезе, синтезе и стабилизации белков внеклеточного матрикса [3].
В физиологически значимых концентрациях (2 мг — средняя суточная потребность) медь ускоряет заживление ран [16].
Ионы меди, которые являются кофакторами лизилоксидазы, принимают участие в последнем этапе синтеза коллагена. Медь имеет важное значение для формирования внутри- и межмолекулярных поперечных связей в коллагене, а соответственно, и прочности коллагеновых и эластиновых фибрилл [8, 13, 15]. Недостаток меди ухудшает формирование сшивок коллагена и приводит к тяжелой патологии костей, легких и сердечно-сосудистой системы [12].
Компенсация дефицита этого микроэлемента, бесспорно, улучшает синтез коллагена, в том числе в коже (рис. 4) [7, 10].
Аскорбиновая кислота (витамин С)
Аскорбиновая кислота играет в организме фундаментальную роль — нет фактически ни одного физиологического процесса, в котором бы она не принимала участия.
Роль витамина С в организме
Аскорбиновая кислота в организме человека оказывает влияние на множество важнейших биологических процессов:
- образование кортикостероидов (при стрессе в несколько раз возрастает уровень потребления витамина С тканями и органами) [20];
- обмен тирозина (влияние на обмен гормонов щитовидной железы) [22];
- трансформация дофамина в норадреналин [25];
- превращение токсичных соединений ванадия в безвредные [23];
- превращение фолиевой кислоты в ее активную форму — тетрагидрофолат [27];
- активация мРНК ацетилхолинового рецептора [20];
- образование активных форм витамина D (транспортной формы [25(OH)D] — в печени и активной гормональной формы [1,25(ОН)2D] — в почках), что служит основным фактором профилактики остеопороза [20];
- потенцирование всасывания железа [24].
Распространенность дефицита витамина С в мире по разным данным составляет 20–40% [14, 15].
В последнее время много исследований посвящено аскорбиновой кислоте и ее биодоступности для кожи [9]. При недостатке витамина С в организме его нанесение на кожу не будет иметь ожидаемого эффекта, так как не сможет восполнить нутритивный дефицит. В ходе проведенных исследований выяснилось, что витамин С ускоряет заживление ран, участвует в активизации синтеза коллагена I типа (рис. 5) и снижении параметров окислительного стресса. Никаких значимых побочных эффектов при добавлении витамина С в питание в ходе проведенных исследований выявлено не было [5, 6].
Синтез коллагена зависит от гормонов, гормоны, в свою очередь, от присутствия металлов, усвоение металлов — от витаминов, и эту цепочку можно продолжать долго, тем более что она замкнутая.
Витамин D
Распространенность дефицита витамина D в российской популяции составляет более 90% (в мире 50–60%) [19]. Этот витамин стимулирует увеличение синтеза секретируемых белков TGF-β (регулируют деление
и дифференцировку различных типов клеток, включая фибробласты и кератиноциты) и их связывание с рецепторами на мембране клеток. Поэтому при его дефиците происходит нарушение активности сигнальных каскадов TGF-β, что ухудшает заживление кожи после любой травмы (включая косметологические манипуляции). Например, во время термолифтинга часть коллагеновых волокон дермы сжимается и уменьшается в объеме. Это приводит к повышению зернистости базального слоя и при достаточном количестве витамина D создает благоприятные условия для воздействия его активных форм на экспрессию TGF-β1, который и способствует обновлению соединительной ткани [11].
Выводы
Мы кратко обсудили лишь некоторые кофакторы, участвующие в синтезе коллагена. Но даже этот незначительный пласт информации позволяет судить о зависимости синтеза коллагена от нутритивного статуса организма, чем не следует пренебрегать, решая многие эстетические задачи. Изменение синтеза коллагена происходит постепенно и усугубляется нутритивным дефицитом [19].
Источник
1. Основные реакции обмена аминокислот:
1.1. Реакции на радикал:
а) гидроксилирование (про, лиз, фен). Механизм микросомального окисления (роль аскорбата, NADPH, цитохрома P450 и др.), примеры, биологическое значение;
б) разрыв (механизм, биологическое значение);
в) метилирование и др.
Кроме индивидуальных путей обмена, известен ряд превращений, общий почти для всех а/к. Это реакции:
1) на радикал (R): — гидроксилирование;
1. При синтезе коллагена одновременно с трансляцией происходит гидроксилирование остатков пролина и лизина, катализируется этот процесс проколлаген-гидроксилазами, имеющими в активном центре атомы железа, в качестве кофермента используется аскорбат (витамин С). Симптомы дефицита витамина С, такие, как выпадение зубов, кровоточивость десен или повреждения кожи (цинга), объясняются нарушением биосинтеза коллагенов. Гидроксилирование пролина и лизина происходит в микросомальной дыхательной цепи при помощи цитохрома Р450, при этом один атом кислорода включается в вещество, а другой, связывая водород из среды, входит в состав воды (см. микросомальную дыхательную цепь)
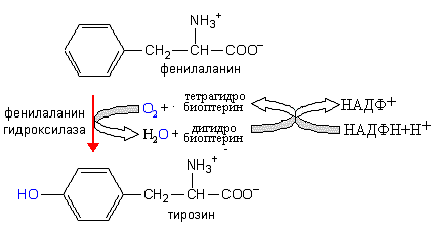
2. При гидроксилировании фенилаланина образуется аминокислота тирозин. Эта реакция катализируется фенилаланингидроксилазой.
Нарушение функции фенилаланин гидроксилазы – причина фенилкетонурии.
Метионин на пути своего распада взаимодействует с АТФ с образованием S-аденозилметионина (SАМ). Эту молекулу называют «активный метионин», поскольку он является донором метильной группы в синтезе многих важных для клетки соединений.
П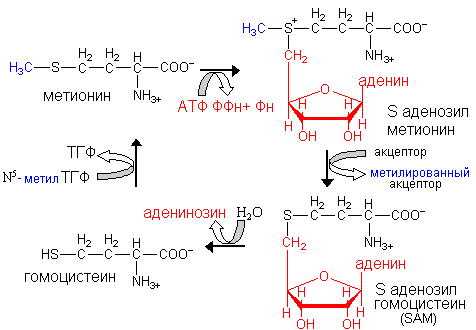
Реакции разрыва цепи можно рассмотреть на примере триптофана и аригинина:
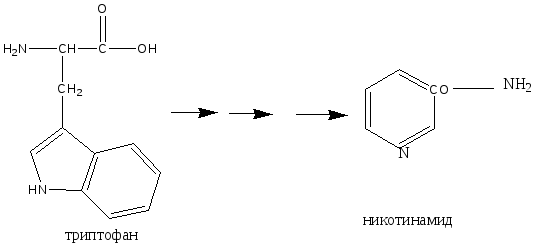
Распад молекулы триптофана до промежуточных продуктов проходит в основном по кинуренин-антранилатному пути, в результате которого после ряда реакций из триптофана образуется никотинамид (витамин РР).
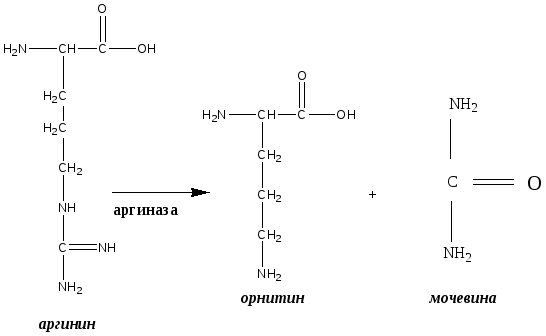
Разрыв цепей аргинина приводит к образованию орнитина и мочевины в цикле синтеза мочевины:
2. Реакции на карбоксильную группу:
а) декарбоксилирование (на примере гис, тир, трп, глу) – механизм, ферменты, биологическая роль;
б) восстановление – ферменты, биологическая роль.
Общая схема процесса декарбоксилирования:
В живых организмах открыто 4 типа декарбоксилирования:
1. Альфа-декарбоксилирование (отщепляется COO-группа, стоящая по соседству с альфа-углеродным атомом.
2. Омега- декарбоксилирование (характерно для микробов).
Таким путем из АСП образуется альфа-аланин.
3. Декарбоксилирование, связанное с трансаминированием.
COOH COOH H COOH
альдегид новая а/к
4. Декарбоксилирование, связанное с конденсацией молекул.
Реакции декарбоксилирования в отличие от других процессов обмена а/к являются необратимыми. Они катализируются специфическими ферментами — декарбоксилазами а/к, каждая из которых состоит из белковой части и простетической группы, представленной пиридоксальфосфатом.
Реакции декарбоксилирования аминокислот лежат в основе образования биогенных аминов. Продукты декарбоксилирования ароматических аминокислот и глутаминовой кислоты выполняют роль нейромедиаторов:
г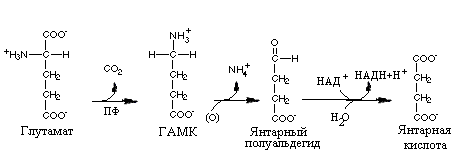
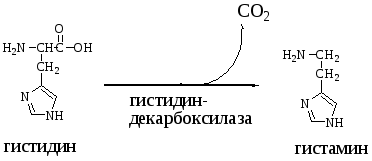
В животных тканях с высокой скоростью протекает реакция декарбоксилирования гистидина, катализируемая специфической гистидиндекарбоксилазой:
Гистамин — вазодилятатор, образуется в области воспаления, вызывая расширения сосудов в очаге воспаления, тем самым ускоряет приток лейкоцитов, участвует в секреции HCl, является медиатором боли.
В животных тканях с высокой скоростью декарбоксилируются цистеиновая и цистеинсульфиновая кислоты.
Источник