МЕТАБОЛИЧЕСКАЯ ФУНКЦИЯ ПОЧЕК
1. Образование активной формы витамина D3. В почках в результате микросомального окисления происходит заключительный этап созревания активной формы витамина D3 – 1,25-диоксихолекальциферола, который синтезируется в коже под действием ультрафиолетовых лучей из холестерина, и затем гидроксилируется: сначала в печени (в положении 25), а затем в почках (в положении 1). Таким образом, участвуя в образовании активной формы витамина D3 , почки оказывают влияние на фосфорно-кальциевый обмен в организме. Поэтому при заболеваниях почек, когда нарушаются процессы гидроксилирования витамина D3 , может развиться остеодистрофия.
2. Регуляция эритропоэза. В почках вырабатывается гликопротеин, названный почечным эритропоэтическим фактором (ПЭФ или эритропоэтин). Это гормон, который способен оказывать воздействие на стволовые клетки красного костного мозга, являющиеся клетками-мишенями для ПЭФ. ПЭФ направляет развитие этих клеток по пути эритропоэза, т.е. стимулирует образование эритроцитов. Скорость выделения ПЭФ зависит от обеспечения почек кислородом. Если количество поступающего кислорода снижается, то увеличивается выработка ПЭФ – это ведет к увеличению количества эритроцитов в крови и улучшению снабжения кислородом. Поэтому при заболеваниях почек иногда наблюдается почечная анемия.
3. Биосинтез белков. В почках активно идут процессы биосинтеза белков, которые необходимы другим тканям. Здесь синтезируются также компоненты системы свертывания крови, системы комплемента и системы фибринолиза.
В почках синтезируются фермент ренин и белок кининоген, участвующие в регуляции сосудистого тонуса и артериального давления.
4. Катаболизм белков. Почки участвуют в катаболизме некоторых белков, имеющих низкую молекулярную массу (5-6 кДа), и пептидов, которые фильтруются в первичную мочу. Среди них гормоны и некоторые другие биологически активные вещества. В клетках канальцев под действием лизосомальных протеолитических ферментов эти белки и пептиды гидролизуются до аминокислот, которые затем поступают в кровь и реутилизируются клетками других тканей.
Большие затраты АТФ почками связаны с процессами активного транспорта при реабсорбции, секреции, а также с биосинтезом белков. Основной путь получения АТФ – это окислительное фосфорилирование. Поэтому ткань почки нуждается в значительных количествах кислорода. Масса почек составляет 0,5% от общей массы тела, а потребление кислорода почками — 10% от всего поступающего кислорода.
7.4. РЕГУЛЯЦИЯ ВОДНО-СОЛЕВОГО ОБМЕНА
И МОЧЕОБРАЗОВАНИЯ
Объем мочи и содержание ионов в ней регулируется благодаря сочетанному действию гормонов и особенностям строения почки.
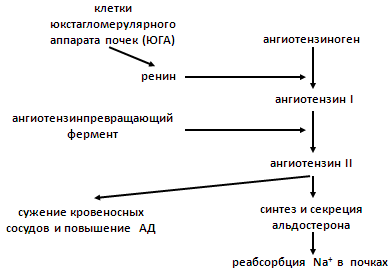
Ренин-ангиотензин-альдостероновая система. В почках, в клетках юкстагломерулярного аппарата (ЮГА), синтезируется ренин – протеолитический фермент, который участвует в регуляции сосудистого тонуса, превращая ангиотензиноген в декапептид ангиотензин I путем частичного протеолиза. Из ангиотензина I под действием фермента карбоксикатепсина образуется (тоже путем частичного протеолиза) октапептид ангиотензин II. Он обладает сосудосуживающим эффектом, а также стимулирует выработку гормона коры надпочечников — альдостерона.
Альдостерон – это стероидный гормон коры надпочечников из группы минералкортикоидов, который обеспечивает усиление реабсорбции натрия из дистальной части почечного канальца благодаря активному транспорту. Он начинает активно секретироваться при значительном снижении концентрации натрия в плазме крови. В случае очень низких концентраций натрия в плазме крови под действием альдостерона может происходить практически полное удаление натрия из мочи. Альдостерон усиливает реабсорбцию натрия и воды в почечных канальцах – это приводит к увеличению объёма крови, циркулирующей в сосудах. В результате повышается артериальное давление (АД) (рис. 19).
Рис. 19. Ренин-ангиотензин-альдостероновая система
Когда молекула ангиотензина-II выполнит свою функцию, она подвергается тотальному протеолизу под действием группы специальных протез – ангиотензиназ.
Выработка ренина зависит от кровоснабжения почек. Поэтому при снижении АД выработка ренина увеличивается, а при повышении – снижается. При патологии почек иногда наблюдается повышенная выработка ренина и может развиваться стойкая гипертензия (повышение АД).
Гиперсекреция альдостерона приводит к задержке натрия и воды – затем развивается отек и гипертония, вплоть до сердечной недостаточности. Недостаточность альдостерона приводит к значительной потере натрия, хлоридов и воды и уменьшению объема плазмы крови. В почках одновременно нарушаются процессы секреции H + и NH4 + , что может приводить к ацидозу.
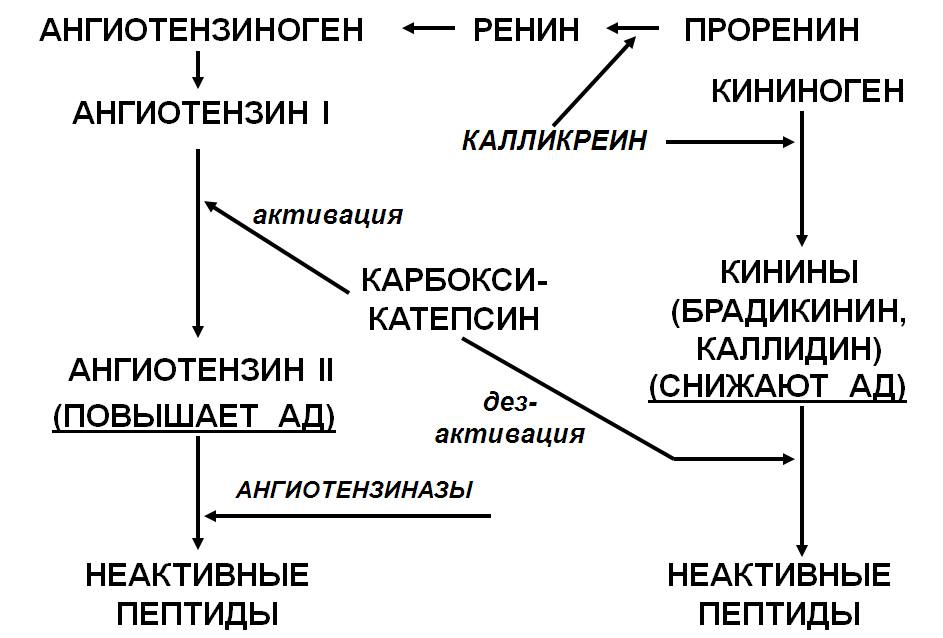
Ренин-ангиотензин-альдостероновая система работает в тесном контакте с другой системой регуляции сосудистого тонуса калликреин-кининовой системой, действие которой приводит к понижению АД (рис. 20).
Рис. 20. Калликреин-кининовая система
В почках синтезируется белок кининоген. Попадая в кровь, кининоген под действием сериновых протеиназ — калликреинов превращается в вазоактиные пептиды — кинины: брадикинин и каллидин. Брадикинин и каллидин обладают сосудорасширяющим эффектом – понижают АД.
Инактивация кининов происходит при участии карбоксикатепсина – этот фермент одновременно влияет на обе системы регуляции сосудистого тонуса, что приводит к повышению АД (рис. 21). Ингибиторы карбоксикатепсина применяются в лечебных целях при лечении некоторых форм артериальной гипертензии. Участие почек в регуляции АД связано также с выработкой простагландинов, которые обладают гипотензивным эффектом.
Рис. 21. Взаимосвязь ренин-ангиотензин-альдостероновой
и калликреин-кининовой систем
Вазопрессин – пептидный гормон, синтезируемый в гипоталамусе и секретируемый из нейрогипофиза, имеет мембранный механизм действия. Этот механизм в клетках-мишенях реализуется через аденилатциклазную систему. Вазопрессин вызывает сужение периферических сосудов (артериол), в результате повышается АД. В почках вазопрессин повышает скорость реабсорбции воды из начальной части дистальных извитых канальцев и собирательных трубочек. В результате увеличивается относительная концентрация Na, C1, P и общего N. Секреция вазопрессина увеличивается при повышении осмотического давления плазмы крови, например, при повышении потребления соли или обезвоживании организма. Считается, что действие вазопрессина связано с фосфорилированием белков апикальной мембраны почки, в результате чего увеличивается ее проницаемость. При поражении гипофиза, в случае нарушения секреции вазопрессина наблюдается несахарный диабет – резкое увеличение объема мочи (до 4-5 л) с низким удельным весом.
Натрийуретический фактор (НУФ) – пептид, который образуется в клетках предсердия в гипоталамусе. Это гормоноподобное вещество. Его мишени – клетки дистального отдела почечных канальцев. НУФ действует через гуанилатциклазную систему, т.е. внутриклеточным посредником его является цГМФ. Результатом влияния НУФ на клетки канальцев является снижение реабсорбции Na + , т.е. развивается натрийурия.
Паратгормон – гормон паращитовидной железы белково-пептидной природы. Он имеет мембранный механизм действия через цАМФ. Влияет на удаление солей из организма. В почках паратгормон усиливает канальцевую реабсорбцию Ca 2+ и Mg 2+ , увеличивает экскрецию К + , фосфата, НСО3 — и уменьшает экскрецию H + и NH4 + . В основном это происходит благодаря снижению канальцевой реабсорбции фосфата. Одновременно в плазме увеличивается концентрация кальция. Гипосекреция паратгормона приводит к обратным явлениям – увеличению содержания фосфатов в плазме крови и к снижению содержания Ca 2+ в плазме.
Эстрадиол – женский половой гормон. Стимулирует синтез
1,25-диоксикальциферола, усиливает реабсорбцию кальция и фосфора в почечных канальцах.
На задержку некоторого количества воды в организме оказывает гормон надпочечников кортизон. В этом случае происходит задержка выделения из организма ионов Na и как следствие – задержка воды. Гормон тироксин приводит к падению массы тела за счет усиленного выделения воды, главным образом через кожу.
Эти механизмы находятся под контролем ЦНС. В регуляции водного обмена участвуют промежуточный мозг и серый бугор мозга. Возбуждение коры головного мозга приводит к изменению работы почек в результате либо прямой передачи соответствующих импульсов по нервным путям, либо путем возбуждения некоторых эндокринных желез, в частности, гипофиза.
Нарушения водного баланса при различных патологических состояниях могут приводить либо к задержке воды в организме, либо к частичному обезвоживанию тканей. Если задержка воды в тканях имеет хронический характер, обычно развиваются различные формы отёков (воспалительные, солевые, голодные).
Патологическое обезвоживание тканей обычно является следствием выделения через почки повышенного количества воды (до 15-20 л мочи в сутки). Такое усиленное мочеотделение, сопровождающееся сильнейшей жаждой, наблюдается при несахарном диабете (diabetes insipidus). У больных, страдающих несахарным диабетом на почве недостатка гормона вазопрессина, почки утрачивают способность концентрировать первичную мочу; моча становится очень разбавленной и имеет низкий удельный вес. Однако ограничение питья при этом заболевании может провести к несовместимому с жизнью обезвоживанию тканей.
Контрольные вопросы
1. Охарактеризуйте экскреторную функцию почек.
2. В чем заключается гомеостатическая функция почек?
3. Какую метаболическую функцию выполняют почки?
4. Какие гормоны участвуют в регуляции осмотического давления и объема внеклеточной жидкости?
5. Опишите механизм действия ренин-ангиотензиновой системы.
6. В чем заключается взаимосвязь ренин-альдостерон-ангиотензиновой и калликреин-кининовой систем?
7. Какие нарушения гормональной регуляции могут быть причиной гипертензии?
8. Укажите причины задержки воды в организме.
9. Что является причиной несахарного диабета?
Источник
Функция почек синтез ренина синтез витаминов
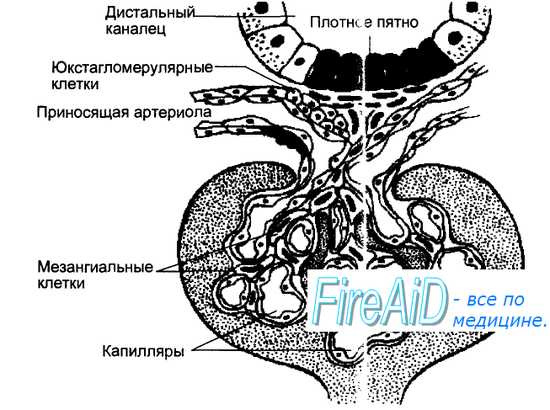
Ренин образуется в виде г роренина и секретируется в юкстагломерулярном аппарате (ЮГА) (от латинских слов juxta — около, glomerulus — клубочек) почек миоэпителиоидными клетками приносящей артериолы клубочка, получившими название юкстагломерулярных (ЮГК). Структура ЮГА приведена на рис. 6.27. В ЮГА кроме ЮГК также входит прилегающая к приносящим артериолам часть дистального канальца нефрона, многослойный эпителий которого образует здесь плотное пятно — macula densa. Секреция ренина в ЮГК регулируется четырьмя основными влияниями. Во-первых, величиной давления крови в приносящей артериоле, т. е. степенью ее растяжения. Снижение растяжения активирует, а увеличение — подавляет секрецию ренина. Во-вторых, регуляция секреции ренина зависит от концентрации натрия в мочедистального канальца, которая воспринимается macula densa — своеобразным Na-рецептором. Чем больше натрия оказывается в моче дистального канальца, тем выше уровень секреции ренина. В-третьих, секреция ренина регулируется симпатическими нервами, ветви которых заканчиваются на ЮГК, медиатор норадреналин через бета-адре-норецепторы стимулирует секрецию ренина. В-четвертых, регуляция секреции ренина осуществляется по механизму отрицательной обратной связи, включаемой уровнем в крови других компонентов системы — ангиотен-зина и альдостерона, а также их эффектами — содержанием в крови натрия, калия, артериальным давлением, концентрацией простагландинов в почке, образующихся под влиянием ангиотензина.
Кроме почек образование ренина происходит в эндотелии кровеносных сосудов многих тканей, миокарде, головном мозге, слюнных железах, клубочковой зоне коры надпочечников.
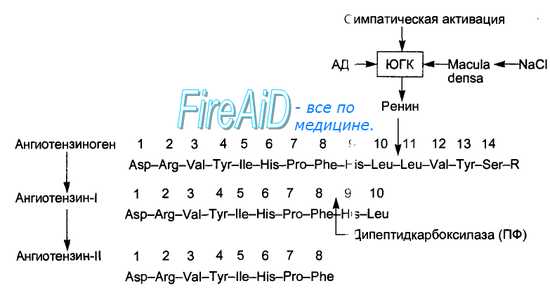
Секретированный в кровь ренин вызывает расщепление альфа-глобулина плазмы крови — ангиотензиногена, образующегося в печени. При этом в крови образуется (рис. 6.1-8) малоактивный декапептид ангиотензин-I, который в сосудах почек, легких и других тканей подвергается действию превращающего фермента (карбоксикатепсин, кининаза-2), отщепляющего от ангиотензина-1 две аминокислоты. Образующийся октапептид ангиотензин-II обладает большим числом различных физиологических эффектов, в том числе стимуляцией клубочковой зоны коры надпочечников, секретирующей альдостерон, что и дало основание называть эту систему ренин-ангиотензин-альдостероновой.
Ангиотензин-II, кроме стимуляции продукции альдостерона, обладает следующими эффектами:
• вызывает сужение артериальных сосудов,
• активирует симпатическую нервную систему как на уровне центров, так и способствуя синтезу и освобождению норадреналина в синапсах,
• повышает сократимость миокарда,
• увеличивает реабсорбцию натрия и ослабляет клубочковую фильтрацию в почках,
• способствует формированию чувства жажды и питьевого поведения.
Таким образом, ренин-ангиотензин-альдостероновая система участвует в регуляции системного и почечного кровообращения, объема циркулирующей крови, водно-солевого обмена и поведения.
Источник
Ренин
Ренин (от лат. Ren — «почка») — протеолитический фермент позвоночных животных и человека. Впервые термин был предложен Тигерштедта и Бергманом в 1898 г.. Для обозначения прессорного вещества, присутствовала в сьольовому экстракте почек кролика. Ренин производится специализированными клетками юкстагломерулярного комплекса и выделяется непосредственно в кровь, однако не является гормоном в полном смысле. Он представляет собой высокоактивную протеазу, которая, действуя на белок плазмы крови ангиотензиноген, начинает образование гормона ангиотензина-II и выделение гормона надпочечников альдостерона. Первый является чрезвычайно активным судинозвужувачем, а второй — регулятором обмена натрия и калия в организме.
Синтез
Синтез ренина состоит из нескольких этапов, начинающиеся с транслции рениновой мРНК в препроренин. N-конечная последовательность препроренина (с 23 аминокислотных остатков) направляет белок в эндоплазматический ретикулюм, где отщепляется с формированием проренина. Проренина гликозилюеться в аппарате Гольджи и либо прямо секретируется в кровь нерегуляторных путем, или упаковывается в секреторные гранулы где превращается в ренин, состоящий из 340 аминокислот, с молекулярной массой 37кДа.
Секреция
Ренин производится юкстагломерулярного клетками стенок афферентных артериол почечных клубочков и отсюда поступает в кровь и лимфу в ответ на три стимулы:
- Снижение артериального давления (которое может быть связано с уменьшением объема крови), что определяется барорецепторами (чувствительные к давлению клеток).
- Снижение уровня хлорида натрия в ультрафильтрате нейрона. На такое изменение реагирует плотное пятно юкстагломерулярного комплекса.
- Деятельность симпатической нервной системы, которая также контролирует кровяное давление, действуя через β1-адренорецепторы.
Хотя по месту синтеза ренин можно отнести к гормонам, он не является, поскольку не имеет клеточной мишени, а влияет на другой белок крови. Кроме того секреция ренина в значительной степени контролируется традиционным эндокринным механизмом обратной связи.
Регуляция секреции
Ингибитором ренина является производное фосфатидилсерину, содержащийся в плазме крови. Содержание ренина в плазме крови (активность в норме — 0,9-3,3 нг / мл / ч) бывает повышен в людей, больных эссенциальной гипертензией. Почки выделяют в кровь ренин в повышенном количестве в условиях гипоксии. Содержание ренина повышается также при применении эстрогенов, фуросемида, этакриновой кислоты и аридных диуретиков, пероральных контрацептивов и снижается под влиянием ангиотензина, дезоксикортикостерона, калия, β-адреноблокаторов.
Ренин-ангиотензиновая система (РАС)
Главным действующим фактором РАС является ангиотензин-II. Цепь реакций образования ангиотензина-II начинается в юкстагломерулярном комплексе. Ренин, там синтезируется, гидролизует α-глобулин ангиотензиноген, который синтезируется в печени под влиянием глюкокортикоидов и эстрогенов. Ренин отщепляет от α-глобулина N-концевой неактивный декапептид — ангиотензин I, который под действием специального ангиотензин-1-превращающего фермента (содержится во всех тканях, больше всего — в легких и плазме крови) превращается в октапептид — ангиотензин II. Последний превращается в гептапептид — ангиотензин ИИИ. Ангиотензин II вызывает сокращение гладких мышц сосудов, снижение интенсивности кровообращения в почках, уменьшение выделения из организма жидкости и солей, а также усиление секреции альдостерона корковым слоем надпочечников; в высоких концентрациях оказывает сильное сосудосуживающее действие и повышает АД.
Стимулом для увеличенного выделения почками ренина и запуска РАС является снижение артериального давления и ухудшение почечного кровоснабжения. Так же активизируется РАС раздражением симпатических нервов или некоторых участков гипоталамуса.
Источник