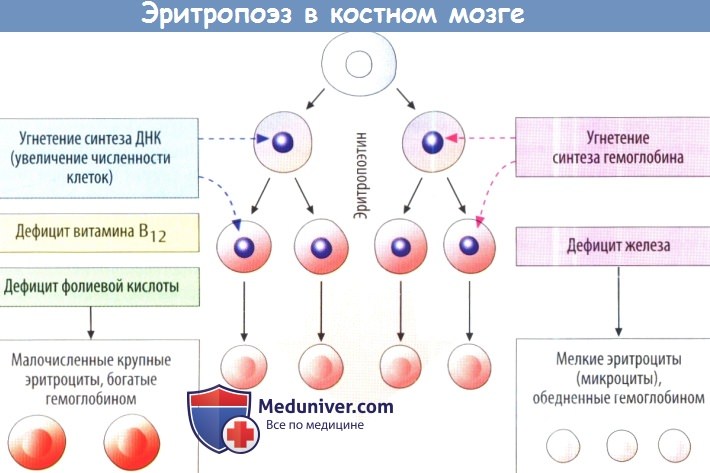
Эритропоэз с участием витамина
Витамин В12 и фолиевая кислота (витамин В9) необходимы для синтеза нуклеопротеинов в разных тканях организма, созревания и деления ядер эритроидных клеток в кроветворной ткани. При дефиците витаминов В12 и В9 в наиболее интенсивно делящейся ткани организма — эритроидной — раньше, чем в других, возникают нарушения, вызывающие анемию. При дефиците витамина В12 в костном мозге появляются большие ядросодержащие эритроидные клетки — мегалобласты, которые образуют с замедленной скоростью большие эритроциты — мегалоциты с резко укороченным периодом жизни. Замедление поступления эритроцитов в кровь и быстрое их разрушение ведет к анемии. Дефицит витамина В12 возникает в организме при утрате париетальными клетками желудка способности продуцировать «внутренний фактор» — гликопротеин (молекулярная масса 60 000). Фактор связывает витамин В12, поступающий с пищей, и предохраняет его от расщепления пищеварительными ферментами. Эти нарушения возникают при атрофии слизистой оболочки желудка, эпителия двенадцатиперстной кишки, часто наблюдающейся, например, у стариков. И хотя запаса витамина В12 в печени достаточно взрослому человеку на 1—5 лет, постепенное его истощение приводит к заболеванию. Суточная потребность в витамине В,2 — 5 мкг, содержание в плазме крови — 150—450 мкг/л. В кишечнике комплекс гликопротеин—витамин В12 фиксируется специальными рецепторами слизистой оболочки тонкого кишечника, далее витамин поступает в интестинальные клетки, затем в кровь и переносится с помощью особых молекул — транскобаламинов (I, II, III типов). Транскобала-мины I и III типа продуцируются лейкоцитами, II — макрофагами. Поэтому при выраженном лейкоцитозе отмечается гипервитаминоз В12. Витамин В12 содержится в больших количествах в печени, почках, куриных яйцах.
Фолиевая кислота (витамин В9) поддерживает синтез ДНК в клетках костного мозга, благодаря обеспечению этого процесса одним из нуклеоти-дов — диокситимидилатом, образующимся в результате митилирования ди-оксиуридиловой кислоты в присутствии тетрагидрофолата (одной из редуцированных форм фолиевой кислоты). При дефиците витамина В9 в пище у человека уже через 1—6 мес нарушается синтез ДНК и деление эритроидных клеток, ускоряется разрушение эритроцитов, что ведет к анемии. Суточная потребность организма человека в фолиевой кислоте 500—700 мкг. Ее резерв в организме равен 5—10 мг, 1/3 которого находится в печени. Фолиевой кислотой богаты овощи (шпинат), дрожжи, молоко.
1,2,5-дигидроксивитамин D3 и ретиноловая кислота (производное витамина А) участвуют в организме человека в дифференциации кроветворных клеток до их зрелых форм. Витаминами А и D богаты печень трески, тунца, сельдь, коровье молоко и сливочное масло.
Витамин В6 (пиридоксин) является кофактором (т. е. дополнительным фактором активности) фермента — синтетазы 5-аминолевулиновой кислоты (АЛК-синтетазы), участвующей в образовании гема в эритроидных клетках в ткани костного мозга (см. рис. 7.2). Дефицит витамина В6 в организме человека нарушает синтез гемоглобина и вызывает анемию. Витамином В6 богаты зерна злаков, капуста, картофель, молоко.
Витамин С поддерживает основные этапы эритропоэза, способствуя метаболизму фолиевой кислоты в эритробластах. Он участвует в метаболизме железа, повышая как его абсорбцию в желудочно-кишечном тракте, так и мобилизацию депонированного в клетках железа.
Витамин Е (токоферол) и витамин РР защищают фосфатидилэтанол амин мембраны эритроцитов от усиливающего их гемолиз перекисного окисления.
Защиту гемоглобина и мембраны эритроцитов от окисления осуществляет и витамин РР, являющийся одной из составляющих пиридиннуклео-тидов НАД и НАДФ.
Дефицит витамина В2, участвующего в окислительно-восстановительных реакциях, вызывает у человека анемию вследствие замедленного образования эритроцитов в костном мозге.
Источник
Роль витаминов, микроэлементов и эритропоэтина в кроветворении
VIII. РОЛЬ ВИТАМИНОВ И МИКРОЭЛЕМЕНТОВ В КРОВЕТВОРЕНИИ.
Железо не является единственным микроэлементом, участвующим в кроветворении. Велика роль и других незаменимых микроэлементов. Кроме того, имеются данные, свидетельствующие о том, что нарушения в обмене железа сказываются на метаболизме других металлов и других важных медиаторов клеточной функции. Особенное значение это имеет при беременности, когда развивающийся плод уязвим к недостаточности микроэлементов.
МЕДЬ — является одним из основных незаменимых микроэлементов, входящих в состав важнейших ферментов, опосредующих в организме жизненно важные процессы, например, дыхание и эритропоэз .Медь находится в тесной связи с изменениями в обмене железа. Медь необходима для эритро- и гранулоцитопоэза. Она участвует в созревании и стимуляции ретикулоцитов и других гемопоэтических клеток, путём активации цитохромоксидазы. Медь способствует устойчивости мембраны клеток и мобилизации железа, его транспорту из ткани в костный мозг. Медь считается основным активатором гемоглобина. В составе супероксиддисмутазы она принимает участие в функционировании антиоксидантной системы. При дефиците меди нарушаются эритро- и гранулоцитопоэз, что способствует развитию гипохромной анемии и нейтропении. Во время недостаточности меди, значительно понижается продолжительность жизни эритроцитов, однако ещё не известен механизм этого явления.
МАРГАНЕЦ — является одним из незаменимых микроэлементов, служит кофактором многих мультиферментных систем, в свою очередь, детерминирующих важнейшие биохимические и физиологические процессы в организме, а именно, синтез нуклеиновых кислот, метаболизм различных гормонов. Имеются также данные об участии марганца в синтезе функционально способных молекул гемоглобина.
ЦИАНКОБАЛАМИН (В12) — обеспечивает нормальный гемопоэз путем активации созревания эритроцитов.
ФОЛИЕВАЯ КИСЛОТА (В9 ) — влияет на биосинтез ДНК в клетках костного мозга;стимулирует эритро-, лейко- и тромбопоэз.
АСКОРБИНОВАЯ КИСЛОТА (С) — облегчает всасывание железа в желудочно-кишечном тракте; влияет на включение железа в синтез гема в костном мозге; участвует в процессе высвобождения железа из депо.
РЕТИНОЛ (A) — участвует в мобилизации железа из депо.
РИБОФЛАВИН (В2 ). При дефиците рибофлавина в организме увеличивается экскреция железа с мочой.
ПИРИДОКСИН (В6 ). Дефицит пиридоксина отражается на состоянии аминокислотного обмена (лизина, гистидина, метионина) специфически участвующих в процессе всасывания железа в кишечнике и синтезе Hb.
В2 и В6 — являясь коэнзимами окислительно-восстановительных процессов, оказывают влияние на гемопоэтическую функцию костного мозга.
ЭРГОКАЛЬЦИФЕРОЛ (D) — участвуют в переносе железа из депо в костный мозг и его абсорбции из крови.
РОЛЬ ЭРИТРОПОЭТИНА В ЭРИТРОПОЭЗЕ.
Эритропоэтин (ЭПО) — белок, фактор роста. Занимает центральное место в регуляции эритропоэза. Вырабатывается в почках. Является физиологическим регулятором продукции эритроцитов и играет ключевую роль в приспособлении этой продукции к метаболическим потребностям в кислороде. Оказывает стимулирующий эффект на костный мозг. Способствует пролиферации ранних эритроидных предшественников, поддерживает их выживание при созревании (препятствует апоптозу), оказывает стимулирующий эффект на синтез Hb и на включение железа клетками костного мозга.
На основе многолетних исследований, проведенных в 1995-2005 гг. в лаборатории клинической биохимии ГУ НЦАГиП РАМН (руководитель проф. В.А.Бурлев) был разработан алгоритм диагностики, профилактики и лечения ЖДС у беременных.
Источник
Эритропоэз с участием витамина
Эритропоэз и механизмы его регуляции
В эмбриональном периоде кроветворение осуществляется вначале в кровяных островках желточного мешка, затем примерно спустя 5 недель эмбрионального развития – в печени. Селезенка включается в процесс кроветворения с 16 недели внутриутробного развития. Первые гемопоэтические элементы появляются в костном мозге на 2-ом месяце эмбрионального развития, однако миелоидный период кроветворения начинается на 4-5-м месяцах эмбрионального развития, вытесняя постепенно кроветворение в печени и селезенке. Костномозговой эритропоэз осуществляется вне синусов, в строме костного мозга, то есть эктраваскуляторно. К моменту рождения ребенка костный мозг развивается полностью, а экстрамедуллярное кроветворение практически завершается. Постэмбриональный период кроветворения начинается после рождения ребенка и продолжается на протяжении всей жизни. Гемопоэз осуществляется в специализированных гемопоэтических тканях: миелоидной (эпифизы трубчатых костей и полости многих губчатых костей) и лимфоидной (тимус, селезенка, лимфатические узлы). В миелоидной ткани образуются эритроциты, лейкоциты, тромбоциты. В лимфоидной ткани идет дальнейшая дифференцировка и созревание лимфоцитов, а также плазматических клеток – основных продуцентов антител.
Постэмбриональный гемопоэз обеспечивает процессы физиологической регенерации крови, то есть её обновление, что компенсирует физиологические процессы разрушения дифференцированных клеток крови.
В условиях нормы функциональная активность органов кроветворения и кроверазрушения строго сбалансирована, что обеспечивает относительное постоянство содержания эритроцитов и других клеток в периферической крови. Разрушение эритроцитов происходит примерно после 120-дневного пребывания их в системной циркуляции при участии тканевых макрофагов селезенки, лимфатических узлов, печени. Гемоглобин, освобождающийся в процессе распада эритроцитов, трансформируется в билирубин в клетках моноцитарно-макрофагальной системы, а затем в гембилирубин (непрямой билирубин), вступая во взаимодействие с белками крови или липопротеидами. Гембилирубин в свою очередь элиминируется из системного кровотока печеночными клетками, где превращается в прямой билирубин (соединение билирубина с глюкуроновой кислотой). Прямой билирубин вместе с желчью поступает в кишечник, постепенно превращается в другие желчные пигменты (стеркобилиноген, уробилиноген) которые, выделяясь с калом и мочой, придают им окраску. При внутриклеточном разрушении эритроцитов основным продуктом, образующимся после распада гемоглобина, является билирубин, а при внутрисосудистом гемолизе большие количества гемоглобина соединяются с α2-гликопротеином-гаптоглобином, который не проникает в мочу.
Основным регулятором эритропоэза является эритропоэтин – гликопротеид, интенсивно вырабатывающийся в условиях гипоксии. При гипоксических состояниях различного генеза концентрация эритропоэтина возрастает в десятки раз по сравнению с нормой. Основным источником синтеза эритропоэтина являются почки (до 90 %), печень (около 10 %), а также макрофаги костного мозга и селезенки. Для эритропоэтина характерен мембранный тип рецепции эритропоэтинчувствительными клетками костного мозга с последующими активацией митоза и дифференцировки клеток, в частности, стимуляцией транспорта железа в эритрокариоцитах, синтеза цепей глобина, ферментов образования гема, синтеза мембранных белков и эритроцитарных антигенов.
Эритропоэз стимулируется под влиянием катехоламинов, глюкокортикоидов, андрогенов, гормонов щитовидной железы, инсулина, плацентарного пролактина, ИЛ-3, ИЛ-6, ИЛ-9, ИЛ-11, КСФ, фолиевой кислоты, витаминов С, В12, железосодержащих препаратов.
Эритропоэз угнетается при повышенной оксигенации тканей, когда снижается образование эритропоэтина, а также под влиянием эстрогенов, глюкагона, ацетилхолина, интерферонов, ФНО-а, ИЛ-1, ИЛ-5, эритроцитарных кейлонов.
После рождения у ребенка в течение нескольких дней отмечают эритроцитоз – содержание эритроцитов составляет 5,5⋅1012/л, в то же время имеется высокое содержание гемоглобина (156-200 г/л). В течение первого года жизни изменяется антигенная структура эритроцитов, возникает прогрессирующее снижение фетального гемоглобина. К концу первого года жизни содержание фетального гемоглобина не превышает 1 %.
Общая характеристика эритроцитов
Эритроциты – самая многочисленная популяция клеток крови, обладающих разнообразными функциями, в частности дыхательной, трофической, детоксицирующей. Количество эритроцитов довольно вариабельно в условиях нормы: так, у женщин оно колеблется от 3,7⋅1012/л до 4,7⋅1012 /л, а у мужчин – от 4,5⋅1012/л до 5,5⋅1012 /л. Сдвиг этих показателей до нижней или верхней границы нормы может быть одним из признаков болезни.
Около 85 % всех эритроцитов имеют форму двояковогнутого диска, то есть являются дискоцитами. Форма эритроцита определяет цепь ауторегулирующих процессов, направленных на поддержание движения крови, её реологических свойств. В условиях патологии появляются эритроциты различной формы, такие состояния именуют пойкилоцитозом. Среди аномальных по форме эритроцитов различают овалоциты, аннулоциты, сфероциты, акантоциты, стоматоциты, щизоциты и другие формы, имеющие в ряде случаев определённое диагностическое значение.
Обычная в условиях нормы форма дискоцита значительно увеличивает площадь диффузии газов, электролитов и других субстратов. Средний диаметр эритроцита (нормоцита) в области краёв составляет 7,5 мкм, а максимальная толщина эритроцита в области краёв составляет 2 мкм. Эритроциты с диаметром от 2 до 6 мкм – микроциты, а с диаметром от 9 до 16 мкм – макроциты. Количество макро- и микроцитов в крови здорового человека в среднем составляет 15–20 %. Резкое увеличение содержания в крови микро- и макроцитов, именуемое анизоцитозом, является одним из признаков нарушения гемопоэза, характерным для анемий, лейкоцитозов, заболеваний инфекционно-аллергической природы. За время свой жизни в периферической крови эритроцит совершает кругооборот более 1 млн. раз, что вызывает развитие механических и метаболических изменений в эритроцитах. Эритроциты обладают пластичностью, то есть способностью к деформации при прохождении через узкие извитые капилляры диаметром 2,5–7,5 мкм. По мере старения их способность к деформации снижается, они застревают в капиллярах красной пульпы селезенки и там разрушаются в процессе фагоцитоза тканевыми макрофагами. Эластичность эритроцитов определяется особенностями структуры белка спектрина, гемоглобина, а также соотношением различных фракций липидов в мембране клеток.
Эритроциты играют важную роль в регуляции кислотно-основного состояния организма, в процессах свертывания крови и фибринолиза за счет адсорбции на их мембране разнообразных ферментных факторов этих систем. Эритроциты являются регуляторами водно-солевого обмена в связи со способностью депонировать воду и минеральные соли при нахождении их в венозной крови. Одной из главных функций эритроцитов является участие в иммунологических реакциях организма за счет наличия в мембранах эритроцитов комплекса полисахаридо-аминокислотных соединений, обладающих свойствами антигенов. Следует помнить, что суммарный объем эритроцитов приблизительно в 160 раз превышает таковой лейкоцитов и тромбоцитов, а потому кровь можно рассматривать как двухфазную систему, представляющую собой взвесь (суспензию) эритроцитов в плазме. При этом эритроцит подвергается в токе крови действию напряжения сдвига – оно более значительно у края и направлено в сторону стенки и менее выражено в центре сосуда. Разница действующих векторов силы у разных краёв обеспечивает вращательное движение эритроцитов в текущей жидкости, что при столкновении с тромбоцитами, имеющими меньший размер и худшую деформируемость по сравнению с эритроцитами, приводит к отбрасыванию кровяных пластинок к стенке сосуда. Благодаря этому пристеночный слой оказывается обогащенным тромбоцитами. Указанный эффект обусловлен величиной гематокрита, размером эритроцитов и тромбоцитов и ригидностью их мембран. Увеличение любого из указанных параметров сопровождается усилением передвижения кровяных пластинок к стенке сосуда, а при наличии повреждения эндотелия – адгезией к субэндотелию.
Буферные свойства эритроцитов. Как известно, на единицу объема эритроцит связывает в 60 раз большее количество О2, чем плазма крови. О2 хорошо растворим в воде, поэтому диффузия его в растворе происходит очень быстро. Связывание О2 с эритроцитами определяется парциальным давлением газа в плазме и сорбционными свойствами Нв. В капиллярах легких, где давление О2 высоко (рО2 = 133 гПа), высоко и сродство Нв к О2, что обеспечивает трансмембранный перенос газа и связывание его с гемоглобином. В капиллярах тканей, где рО2 равно 40-50 гПа, сродство Нв к О2 резко снижается. При этом происходит выход кислорода из эритроцитов.
Транспорт СО2 через мембрану эритроцита также осуществляется за счет диффузного давления (в капиллярах легких рСО2 = 53гПа, а в капиллярах тканей – 61 гПа). Диффузия СО2 в растворах происходит примерно в 20 раз быстрее, чем О2.
Высокая скорость равновесия содержания СО2 в системе эритроцит – плазма крови обеспечивается наличием в эритроцитах особого фермента – карбоангидразы, катализирующего реакции трансформации СО2 и Н2О в углекислоту (Н2СО3), а также мощными системами трансмембранного обмена анионами.
При понижении концентрации СО2 в эритроцитах возникает отрицательный заряд Нв, что приводит к уменьшению содержания внутриклеточной воды, а при увеличении содержания СО2 в эритроцитах – они набухают.
Известно, что осмотическое давление в эритроцитах несколько выше, чем в плазме крови, что связанно с высокой внутриклеточной концентрацией белков по сравнению с плазмой крови. При этом содержание низкомолекулярных осмотически активных веществ (ионов натрия) в эритроцитах значительно меньше, чем в плазме крови. Величина осмотического давления в эритроцитах обеспечивает достаточный или нормальный тургор этих клеток. Осмотическое давление плазмы и эритроцитов в условиях нормы находится в динамическом равновесии, что обуславливает стабильность структуры эритроцитов.
При помещении эритроцитов в коллоидно-осмотическую среду с более низким осмотическим давлением (гипотонические растворы) может наступить осмотический или коллоидно-осмотический гемолиз. Последний обусловлен тем, что вода поступает в эритроциты до того момента, пока не разрывается мембрана и гемоглобин выходит в окружающую среду.
В умеренногипотонической среде эритроциты приобретают сферическую форму, их называют в связи с этим сфероцитами. Способность эритроцитов сохранять свою структуру при развитии гипоосмотических состояний или в гипоосмотической среде получила название осмотической устойчивости, или резистентности эритроцитов. Верхняя граница резистентности или максимальная устойчивость эритроцитов соответствует примерно 0,5–0,4 % раствора хлорида натрия.
При помещении эритроцитов в гипертоническую среду происходит их сморщивание в связи с потерей воды и уменьшением объема.
Эритроцитам свойственна способность к оседанию. Удельная масса цельной крови в норме для взрослого составляет в среднем 1,05–1,06. Удельная масса эритроцитов (1,085–1,096) выше, чем плазмы крови (1,02–1,027), поэтому эритроциты в пробирке с кровью, лишенной возможности свертываться, способны медленно оседать на дно. Скорость оседания эритроцитов в значительной мере определяется белковым составом плазмы крови, в частности уровнем мелкодисперсных белков-альбуминов. В связи с этим важная роль в обеспечении величины СОЭ отводится соотношению альбуминово-глобулиновых фракций белков крови. СОЭ у мужчин в среднем составляет 1–10 мм/ч, у небеременных женщин 2-15 мм/ч. При некоторых патологических процессах и заболеваниях, а также во второй половине беременности СОЭ повышается, так как увеличивается содержание в крови грубодисперсных белков глобулиновой фракции, получивших название аггломеринов, а также за счет усиления образования фибриногена.
При замедлении скорости кровотока и повышении вязкости крови эритроциты проявляют способность к агрегации. Вначале агрегация носит обратимый характер, при этом образуются ложные агрегаты, или монетные столбики. В случае быстрого восстановления кровотока они распадаются на полноценные клетки с сохраненной мембраной и внутриклеточной структурой.
Пластичность или деформируемость – это способность эритроцитов к обратимой деформации при прохождении через узкие извитые капилляры, микропоры. Данное свойство определяется особенностями структуры мембраны эритроциты, наличием в ней особого белка спектрина.
Таким образом, основными физиологическими и физико-химическими свойствами эритроцитов являются следующие:
– способность к оседанию;
– способность к агрегации;
– деструкция после определенного периода циркуляции в кровотоке.
1. Дыхательная функция заключается в захвате и переносе кислорода к тканям и экскреции СО2 из организма. Это обеспечивается содержащимся в эритроцитах белком гемоглобином. Гемоглобин – сложный белок состоит из групп гема и белкового остатка – глобина. Содержание гемоглобина у мужчин составляет 130-160 г/л, у женщин 120-140 г/л.
2. Трофическая функция эритроцитов связана с их способностью транспортировать аминокислоты, нуклеотиды, пептиды к различным органам и тканям, способствуя обеспечению репаративных процессов. В ряде случаев эту функцию называют транспортной.
3. Детоксиксицирующая функция эритроцитов обусловлена их способностью адсорбировать токсические продукты эндогенного или экзогенного происхождения и частично инактивировать их.
4. Участие в процессах свертывания крови за счет адсорбции на их мембране плазменных факторов свертывания крови
5. Участие в регуляции кислотно-основного состояния организма (буферная функция) за счет гемоглобина обеспечивающего до 70 % буферной ёмкости крови.
6.– Ферментативная функция связана с наличием в эритроцитах большого количества ферментов, в частности карбоангидразы, метгемоглобинредуктазы, ферментов гликолиза.
Источник